PESTICIDI ATTUALI: PIRETROIDI E NEONICOTINOIDI E LORO IMPATTO SULLA SICUREZZA ALIMENTARE
“È sapiente solo chi sa di non sapere, non chi s’illude di sapere e ignora così perfino la sua stessa ignoranza.” (Socrate)

Università degli Studi dell’Aquila
Dipartimento di Medicina Clinica, Sanità Pubblica, Scienze della Vita e dell’Ambiente
CLM Scienze delle Professioni Sanitarie della Prevenzione
TESI DI LAUREA
PESTICIDI ATTUALI: PIRETROIDI E NEONICOTINOIDI E LORO IMPATTO SULLA
SICUREZZA ALIMENTARE
RELATORE
Chiar.ma Prof.ssa Gabriella FONTECCHIO
CANDIDATO
Adamo Conti
Matr.249936
Anno Accademico 2017/2018
Sommario
PREFAZIONE
CAPITOLO 1. ALIMENTI E CONTAMINANTI 7
-
- LA QUALITÀ DI UN ALIMENTO 7
- IL CONCETTO DI CONTAMINANTE LUNGO LA CATENA ALIMENTARE 10
- CONTAMINANTI DA FONTI ANTROPICHE 12
- FARMACI AD USO VETERINARIO 16
- I PRODOTTI CHIMICI PER L’AGRICOLTURA 17
CAPITOLO 2. PESTICIDI 19
-
- CLASSIFICAZIONE DEI PESTICIDI 19
- CLASSIFICAZIONE IN BASE ALL’ORGANISMO BERSAGLIO 19
- CLASSIFICAZIONE CHIMICA 21
- INSETTICIDI ORGANOCLORURATI (OC) 26
- IL DDT (PARA-DICLORODIFENILTRICLOROETANO) 27
- INSETTICIDI ORGANOFOSFORICI (OP) 30
- INSETTICIDI CARBAMMATI 33
- PIRETROIDI E PIRETRINE 34
CAPITOLO 3. I NEONICOTINOIDI 38
-
- CARATTERISTICHE GENERALI 40
- MODALITÀ D’AZIONE 43
- EFFETTI SULLE API QUALI INDICATORI BIOLOGICI 45
- DISPERSIONE NELL’AMBIENTE 49
- LA CONCIA DELLE SEMENTI 50
- DESTINO AMBIENTALE 51
- SEMINA E POLVERI 51
- LA GUTTAZIONE FOGLIARE E LA DISTRIBUZIONE NELLE PIANTE 52
- PERSISTENZA, DEGRADAZIONE E DESTINO AMBIENTALE 55
- LEGISLAZIONI RIGUARDANTI I NEONICOTINOIDI E ALTRI INSETTICIDI 58
- TOSSICITÀ ACUTA E CRONICA DEI PESTICIDI 62
- DETERMINAZIONE DEI VALORI DI TOSSICITÀ ACUTA E CRONICA 67
- DOSI SOGLIA DI ESPOSIZIONE PER L’UOMO 67
- VALUTAZIONE DEL RISCHIO CRONICO 69
- LA VALUTAZIONE DEL RISCHIO ACUTO 70
- VALUTAZIONE DEL RISCHIO PER IL CONSUMATORE 71
- IL FATTORE DI SICUREZZA PER LA DEFINIZIONE DELLE SOGLIE DI
ESPOSIZIONE PER L’UOMO 72
3.9 PRINCIPALI STUDI TOSSICOLOGICI PER LA VALUTAZIONE DELL’IMPATTO SULLA SALUTE RICHIESTI NEL PROCESSO DI AUTORIZZAZIONE DI UN PRODOTTO FITOSANITARIO 73
CAPITOLO 4.SICUREZZA ALIMENTARE E CONTROLLI UFFICIALI 74
-
- ORGANISMI CENTRALI E TERRITORIALI DEL SISTEMA DEI CONTROLLI PER LA SICUREZZA ALIMENTARE 76
- D.M. 23 DICEMBRE 1992 – PROGRAMMAZIONE NAZIONALE DEL CONTROLLO UFFICIALE DEI RESIDUI DI PRODOTTI FITOSANITARI NEGLI ALIMENTI 78
- IL REGOLAMENTO (CE) 396/2005 – PROGRAMMA COORDINATO COMUNITARIO PLURIENNALE 80
- D.M. 23 LUGLIO 2003 – METODI DI CAMPIONAMENTO AI FINI DEL CONTROLLO UFFICIALE DEI RESIDUI DI ANTIPARASSITARI NEI PRODOTTI ALIMENTARI DI ORIGINE VEGETALE E ANIMALE 95
CAPITOLO 5. PIANO REGIONALE DI CAMPIONAMENTO AZIENDA SANITARIA UNICA REGIONE MARCHE ANNO 2017 98
-
- ASUR MARCHE – CONTROLLO RESIDUI ANTIPARASSITARI SU E NEI PRODOTTI ALIMENTARI ANNO 2017 100
- PREMESSA 101
- CAMPIONAMENTO 101
- DETERMINAZIONE ANALITICHE 103
- ESITO CONTROLLO RESIDUI ANTIPARASSITARI SU E NEI PRODOTTI ALIMENTARI ANNO 2017 108
5.5 REPERTI ANALITICI 110
CONSIDERAZIONI CONCLUSIVE 115
RIFERIMENTI NORMATIVI e BIBLIOGRAFICI 119
SITOGRAFIA 127
RINGRAZIAMENTI 128
Il tema della sicurezza alimentare (food security) è un concetto complesso e multidisciplinare, rappresentando un punto centrale per quanto concerne la tutela della salute pubblica. In generale, la sicurezza alimentare, attenendoci alla definizione della FAO (Food and Agriculture Organization of the United Nations: Organizzazione delle Nazioni Unite per l’alimentazione e l’agricoltura) proposta in occasione del vertice mondiale sull’alimentazione (World Food Summit, tenutosi a Roma nel 1996), è quello di “assicurare a tutte le persone e in ogni momento una quantità di cibo sufficiente, sicuro e nutriente per soddisfare le loro esigenze dietetiche e le preferenze alimentari per una vita attiva e sana”.
Molto più sintetica, ma carica di significato, risulta invece la definizione dell’Unione Europea e dell’Organizzazione Mondiale della Sanità(OMS): “la sicurezza alimentare è una responsabilità condivisa dal campo alla tavola”. Appare pertanto di fondamentale importanza il ruolo del controllo lungo tutta la filiera produttiva e distributiva degli alimenti, soprattutto ora che la globalizzazione dei mercati, i rapporti bi/multilaterali fra Stati e la complessità dei processi produttivi e conservativi permettono, nell’insieme, di portare in tavola cibi provenienti da tutto il mondo e in ogni stagione.
Lo scopo di questa tesi, quindi, è quello di chiarire gli aspetti salienti della food security relativamente al rischio chimico dovuto a residui di pesticidi con particolare riferimento alla classe (di ultima sintesi) dei Neonicotinoidi che, grazie alla loro elevata efficacia di azione e “inizialmente” (v. quanto riportato nel paragrafo 3.8)bassa tossicità riscontrata
nei confronti dell’ambiente e dei mammiferi, si ritrovano attualmente in commercio
insieme ai cosiddetti e ben noti Piretroidi. Tuttavia sono crescenti i dati di letteratura che dimostrano come gli insetticidiNeonicotinoidi siano in grado di provocare danni alla salute umana, anche con risvolti in ambito ambientale. Entrambi, Neonicotinoidi e Piretroidi, stanno sostituendo numerosi insetticidi appartenenti ad altre classi (carbammati, organoclorurati, organofosforici) e in gran parte ad oggi messi al bando (perlomeno nei Paesi più avanzati) per tre ragioni fondamentali: 1)sviluppo di resistenza da parte degli insetti infestanti, implicante la ricerca di nuovi principi attivi; 2)documentato nesso di causa – effetto tra l’utilizzo di sementi di mais, colza, girasole, barbabietola da zucchero, per non citare altrenumerose coltivazioni ortofrutticole trattate con tali principi edevidente morìa delle api (fenomeno noto con l’acronimo SSA, Sindrome da Spopolamento degli Alveari): l’ape rappresenta, infatti, uno fra i più sensibili bioindicatori (organismi sentinella)degli effetti nocivi/tossici per l’ambiente conseguenti ad un uso estensivo, spesso improprio, degli agrofarmaci, come più approfonditamenteargomentato in seguito; 3) chiare evidenze di tossicità cronica riscontrate nell’uomo, tanto in qualità di consumatore quanto di produttore e utilizzatore di prodotti trattati con fitofarmaci.
CAPITOLO 1. ALIMENTI E CONTAMINANTI
LA QUALITÀ DI UN ALIMENTO
La qualità è definita come “l’insieme delle proprietà e caratteristiche di un prodotto o servizio che gli conferiscono l’attitudine a soddisfare bisogni espressi o impliciti” (con riferimento alla norma UNI EN ISO 8402).
Accanto alla qualità richiesta dal consumatore (qualità percepita) vi è anche una qualità definita dalle industrie e dalla GDO (Grande Distribuzione Organizzata) che è focalizzata sulla tecnologia e la sicurezza alimentare (qualità oggettiva).
Pertanto, alla base del concetto di qualità, sia per il consumatore sia per il produttore e il distributore, vi è la sicurezza alimentare, resa obbligatoria dalla normativa vigente e che, in primo luogo, dipende dalla rispondenza dell’alimento a requisiti tanto igienico- sanitari quanto tossicologici. Nello specifico, la qualità dei prodotti agroalimentari può essere compromessa da numerosi fattori, fra i quali lapresenza di sostanze contaminanti, ossia inquinanti ambientali imputabili in primis ad attività antropiche. Numerosi contaminantisono infatti aggiunti volontariamente agli alimenti, come additivi,aromi, coloranti o stabilizzanti, per prolungarne la durata o per renderli più gradevoli alla vista o al gusto; la loro presenza è solitamente indicata nelle etichette dei prodotti, ma ciò non sempre accade.
Ma non basta: innumerevoli altre sostanze, quali i prodotti fitosanitari, sono utilizzati ampiamente per la difesa dalle malattie degli animali (a protezione degli stessi) o
deiprodotti ortofrutticoli destinati all’alimentazione, al fine soprattutto di garantirne una resa che soddisfi le richieste di mercato.
I fitofarmaci alquanto spesso permangono come residui nell’alimento; pressoché tutti sono in grado di esercitare attività tossiche croniche che vanno, ad esempio, da semplici congiuntiviti allergiche ainsufficienze renali ed epatopatie, fino addirittura all’instaurarsi di fenomeni mutagenici e all’insorgenza di neoplasie, e quant’altro, ciò dipendentemente da pericolosità intrinseca, durata del contattoe dose assunta quotidianamente del composto “incriminato”; in tal senso, il rischio di tossicità cronicada esposizione ad agrofarmaci sussiste tanto per la popolazione generale che per i lavoratori esposti (questi ultimi anche a rischio di tossicità acuta per introduzione accidentale).
Sostanze contaminanti possono, tuttavia, essere presenti nelle materie prime alimentari, anche se non intenzionalmente aggiunte. Esse derivano dall’ambiente come conseguenza, ad esempio, di svariati processi industriali, emissioni da inceneritori, incendi accidentali o dolosi di materie plastiche con rilascio di diossine, traffico veicolare, idrocarburi policiclici aromatici (IPA), policlorobifenili (PCB), metalli pesanti, e non sono sempre evitabili.
Il quadro normativo esistente in Italia assicura che gli alimenti posti sul mercato siano sicuri e non contengano sostanze chimiche e contaminanti a livelli che pongano a rischio la salute. In questo senso risulta oltremodo utile il Codex Alimentarius, presentato nel paragrafo 1.2.
I contaminanti possono essere introdotti in qualsiasi punto della filiera produttiva di un alimento e in base alla loro natura possono dar vita a diversi tipi di contaminazione:
- chimica, dovuta a residui derivanti da pratiche agro-alimentari (ricorso ad erbicidi, insetticidi, antibiotici, ecc.), inquinanti ambientali (già menzionati), sostanze rilasciate dai contenitori (MOCA: Materiali e Oggetti a Contatto con gli Alimenti)o prodotte in seguito alla trasformazione o preparazione degli alimenti (acroleina, benzo[a]pirene o IPA nei processi di affumicatura);
- fisica, causata principalmente dalla presenza di corpi estranei nell’alimento (vetro) o a residui radioattivi;
- biologica, correlata alla presenza di svariate sostanze prodotte dal metabolismo di microrganismi patogeni indesiderati; il caso più eclatante è quello del botulino (Clostridium botulinum), un batterio anaerobico la cui tossina botulinica può contaminare gli alimenti (accanto a prodotti industriali, le conserve domestiche: verdure, marmellate, insaccati) rendendoli particolarmente pericolosi per la salute umana in quanto causa di emesi, vertigini, perdita dell’equilibrio, difficoltà respiratorie, fino alla paralisi.
In questo documento verrà piuttosto dato spazio allo studio del rischio chimico da residui di pesticidi negli alimenti confrontando i dati nazionali ed europei con quelli regionali della Regione Marche ottenuti a seguito di indagine effettuata dallo scrivente e riferita all’Anno 2017.
IL CONCETTO DI CONTAMINANTELUNGO LA CATENA ALIMENTARE
I contaminanti ambientali rappresentano, dunque, un grave rischio (NB: non “pericolo”, in quanto l’uomo, al pari degli esseri viventi bersaglio di essi, ne sono costantemente a contatto, quotidianamente e per l’intera vita) per la salute umana e animale. Nel corso degli anni è stato affrontato il concetto di “contaminante”ed è stata universalmente accolta la seguente definizione del CodexAlimentarius: “qualsiasi sostanza non intenzionalmente aggiunta all’alimento, ma che sia presente in essocome risultato del processo produttivo e dei processi di fabbricazione, trasformazione, preparazione, trattamento, imballaggio, trasporto o conservazione di tale alimento, o in seguito alla contaminazione ambientale. Non rientrano in questa definizione le materie estranee, quali frammenti di insetti, peli di animali ecc.” Si tiene a precisare in questa sede che il così detto “CodexAlimentarius”(di cui significato, compiti ed impiego sono ben elucidati in figura)consiste essenzialmente in un organismo delle Nazioni Unite (creato nel 1962 dalla FAO -Organizzazione per l’Alimentazione e l’Agricolturae dall’OMS – Organizzazione Mondiale della Sanità) deputato a proteggere la salute dei consumatori e assicurare pratiche eque nel commercio degli alimenti, elaborando norme atte a disciplinare produzione nonché commercio dei prodotti alimentari, allo scopo di: a) favorire gli scambi internazionali, garantendo in tal modo accordi commerciali leali; b) garantire ai consumatori un prodotto sano e igienico, non adulterato e correttamente proposto, ovvero adeguatamente etichettato. Numerosi sono, attualmente, i Paesi
membri della Commissione del CodexAlimentarius, i quali rappresentano più del 98% della popolazione mondiale.
 www.codexalimentarius.net/pestres/data
www.codexalimentarius.net/pestres/data
Associazione tra i governi del mondo, che si riuniscono per decidere e per codificare (quindi il Codex) le procedure di produzione, i livelli di sostanze inquinanti “ammesse”, gli additivi, l’etichettatura e in genere il modo di produrre e di trattare gli alimenti (quindi Alimentarius). E’ un insieme di linee guida e codici di buone pratiche che contribuisce al miglioramento della sicurezza, qualità e correttezza del commercio mondiale di alimenti. I consumatori sono tutelati e gli importatori hanno sempre più garanzie nei loro scambi sul fatto che il cibo che hanno ordinato sarà conforme alle loro specifiche richieste. La Commissione del Codex Alimentarius, è l’organo delle Nazioni Unite deputato a deliberare sugli standard di salubrità e qualità alimentare.
Pesticide Residues in Food and Feed PESTICIDES DATABASE SEARCH
A fianco: Database per la ricerca dei
Search
valori LMR: livelli massimi di residui
Infatti, la legislazione (sia europea che nazionale) stabilisce un limite massimo di residuo di pesticida riscontrabile in un alimento. Si tratta di limiti superiori legalmente autorizzati della concentrazione di residui dei pesticidi all’interno o sulla superficie di alimenti o mangimi. Se su un determinato alimento viene riscontrato un residuo di pesticida inferiore al LMR, il prodotto è considerato sicuro per la sicurezza del consumatore.
In sintesi, è possibile definire contaminante alimentare “una sostanza estranea alla composizione naturale dell’alimento, ovvero la presenza di ben noti microrganismi dannosi per la salute umana”.
L’attività di valutazione del rischio degli inquinanti nella catena alimentare si basa sull’ esame tecnico delle categorie dei contaminanti alimentari e su taluni composti specifici dotati di attività tossica comprovata da studi sperimentali, epidemiologici e report di interventi ispettivi; data la continua evoluzione nel campo della sintesi chimica di nuovi pesticidi, contestualmente al degrado ambientale strettamente correlato al loro utilizzo, il monitoraggio e lo studio dei contaminanti ambientali rappresenta attualmente una delle priorità per la comunità scientifica internazionale allo scopo di poter prevedere le
emergenze sanitarie (quindi pianificare attività di prevenzione e gestione del rischio), ivi incluse quelle riguardanti, in particolare, la Sicurezza degli Alimenti (Food Safety).
CONTAMINANTI DA FONTI ANTROPICHE
Rivolgendo l’interesse all’alimentazione umana, è d’obbligo ribadire che la contaminazione dei cibi da sostanze chimiche estranee (altrimenti dette “xenobiotici”: dal greco “xenos” estraneo e “bios” vita, ossia sostanza estranea al metabolismo di qualsivoglia organismo vivente – droga, farmaco, pesticida -) deriva perlopiù da fonti antropiche (riferibili alle attività dell’uomo)e si pone qualeinesorabile conseguenza di tre essenziali aspetti:
- l’aumento della popolazione
- la concentrazione della popolazione in grossi agglomerati urbani
- il crescente fenomeno dell’industrializzazione
L’ aumento della popolazione ha reso indispensabile non solo uno sforzo di maggiore produzione di derrate alimentari, ma anche e soprattutto l’adozione di trattamenti chimici delle colture allo scopo di proteggerle dall’attacco di insetti e parassiti d’ogni specie. Da qui l’uso crescente di antiparassitari e diserbanti presenti in tracce in pressochétutti gli alimenti e nelle acque.
La concentrazione della popolazione in agglomerati urbani ha reso indispensabile la conservazione degli alimenti per lungo tempo e quindi l’uso degli additivi.
Per inciso, gli additivi chimici sono fonte di preoccupazione per il consumatore poiché, sommati tra loro nel corso dei pasti quotidiani, diventano responsabili dell’aumento del 5% delle allergie alimentari. Non solo, nitrati e nitriti di sodio e potassio, contenuti nellecarni conservate e nei salumi, possono modificare il funzionamento della tiroide o trasformarsi in composti cancerogeni. I solfiti, presenti in crostacei, vino, frutta secca e candita, funghi secchi, ecc., possono causare asma e orticaria. I fosfatiaddizionati ad esempio a budini, gelati, latte concentrato o prosciutto cotto, possono determinare osteoporosi. Alla luce di quanto esposto, sebbene non risulti corretto attribuire l’avvelenamento cronico (di questo si tratta) dei consumatori ai soli pesticidi, questi ultimi risultano tuttavia i principali xenobiotici operanti ai danni della salute umana, senza sottovalutare gli effetti additivi/sinergici con altri composti inquinanti dell’aria, del suolo e dell’ecosistema acquatico.
In aggiunta, l’avvicendamento di una crescente industrializzazione ha sollevato problemi di inquinamento con l’immissione nell’ambiente di quantità anche smisurate di prodottichimici, spesse volte rivelatisi tossici e, di conseguenza, rintracciabili negli alimenti.
Non è infrequente che studi laboristici su colture batteriche, cellulari e su modelli animali siano condotti mediante somministrazione di dosi elevate dello xenobiotico in esame, non rispondenti a quelle cui è esposta la popolazione, o terminati in tempi troppo brevi se andiamo a considerare che la stessa popolazione ne verrà esposta per l’intero arco di vita. Inoltre, una vasta gamma di pubblicazioni su riviste scientifiche internazionali non riferiscono dati concordanti circa gli effetti espletati da xenobiotici oggetto di studio: dati
scientifici contrastanti fra loro non offrono una certezza sulla innocuità (assenza di effetti nocivi e/o tossici) di composti di nuova sintesi da immettere in commercio. Quanto asserito sta infatti accadendo per i Neonicotinoidi. Inoltre, i meccanismi metabolici e la responsività a sostanze xenobiotiche da parte di animali di laboratorio non sonoperfettamente estrapolabili all’uomo. Prova ne è la vasta pubblicazione di letteratura di danni causati, a lungo termine, sull’uomo da parte svariati insetticidi, a distanza di anni dalla loro sperimentazione, come esposto a seguire.

L’uomo si nutre oramai di prodotti ortofrutticoli “integrati” con pesticidi. Ciò è
inevitabile e l’esposizione è continua; le patologie rivelantisi a lungo termine a
seguito di introduzione di detti xenobiotici è in crescendo stando ai dati di
letteratura; ne consegue che una attività ispettiva in campo agronomico si rende
sempre più necessaria e puntuale, perlomeno per garantire il rispetto delle norme
vigenti e dei valori limite dei residui di pesticidi negli alimenti e nei mangimi, in
quest’ultimo caso con cognizione dei processi di bioconcentrazione e
biomagnificazione che hanno luogo nella catena trofica
Nello specifico, quanto detto, e tema della presente tesi, per quanto concerne gli
insetticidi appartenenti alla classe di di insetticidi nuova sintesi, ossia quella dei
neonicotinoidi, successiva a quella dei piretroidi, le criticità sembrano accentuantisi.
FARMACI AD USO VETERINARIO
Gli allevamenti intensivi di animali hanno posto due gravi problemi di ordine ambientale
:
- lo smaltimento dei liquami;
- la possibile contaminazione delle carni e delle altre produzioni zootecniche,dovuta all’uso sconsiderato dei farmaci utilizzatinella cura degli animali.
La contaminazione da farmaci è molto più pericolosa di quanto comunemente si pensi poiché tali sostanze vengono somministratequasiquotidianamente agli animali da allevamento. Inoltre, come sta accadendo per gli antibiotici,l’assunzione attraverso gli alimenti sta provocando una lenta assuefazione ai farmaci (antibiogrammi positivi)con il risultato dello sviluppo di agenti patogeni sempre più resistenti. Ciò senza considerare i fenomeni di bioconcentrazione e biomagnificazione cui vanno incontro i pesticidi assunti dagli animali di allevamento. Anche l’impiego di antiparassitari per animali domestici, contenenti taluni il Fipronil (neonicotinoide) altri Imidacloprid(neonicotinoide) in associazione con Permetrina (piretroide), si stanno rivelando tossici per somministrazione cronica; in cani sono stati osservati convulsioni, spasmi, nefro- ed epato-tossicicità, aumento della mortalità della prole, evidenze di cancro alla tiroide e numerosi sono i casi denunciati di cancro alla vescica.
I PRODOTTI CHIMICI PER L’AGRICOLTURA
I pesticidi sono i soli prodotti chimici concepiti dall’uomo e intenzionalmente liberati nell’ambiente con azione abbattente o repellente nei confronti degli organismi infestanti. Tutta la grande famiglia dei pesticidi, è identificabile dal suffisso “cida” (erbicida, fungicida, ecc.), che deriva dal latino “cœdere”, che significa “uccidere” o “abbattere”. Quindi pesticidi, secondo l’etimologia, sono sterminatori di “pesti” (dal latino “pestis” che indica un flagello o una malattia contagiosa). Ecco perché nel mondo industriale si evita accuratamente di parlare di pesticidi, preferendo la dicitura prodotti fitosanitari, o l’ancor più edulcorato “prodotti fitofarmaceutici”, il che non è un solo gioco di prestigio semantico che rassicura tutti, ma mira proprio ad ingannare prima i coltivatori e poi noi consumatori. Essi possono essere inorganici, oppure organici naturali e di sintesi e possono venir utilizzati in pieno campo, nella fase di conservazione dei prodotti vegetali e anche come fisiofarmaci per influire sui processi vitali dei vegetali, come i fitoregolatori e i biostimolanti.
Ogni pesticida è immesso sul mercato sottoforma di varie formulazioni ed è composto da tre componenti essenziali:
- Il principio attivo, ossia la sostanza che esplica l’azione diretta nei confronti del patogeno, ed è pertanto dotato di tossicità intrinseca.
- I coadiuvanti, che sono sostanze che vengono aggiunte al principio attivo al fine di migliorare la sua azione e la sua persistenza.
- Le sostanze inerti, composti privi di azione specifica, ma con la funzione di
diluire il principio attivo favorendo la buona riuscita della formulazione.
Sebbene l’impiego di pesticidi inorganici quali zolfo, rame e arsenico risalga all’antichità e che alcuni prodotti chimici di sintesi siano stati introdotti negli anni ‘30 del secolo scorso, la produzione industriale di agrofarmaci è in fondonata dopo la seconda guerra mondiale.
Negli anni ‘40 vennero messi in commercio insetticidi organoclorurati come il DDT, brevettato nel 1944. Lo studio e la sperimentazione degli insetticidi organofosforici era iniziato durante la seconda guerra mondiale a scopi bellici, così che sempre nel1944 si scoprì l’attività insetticida del Parathion. E sempre nei primi anni ‘40 vennero scoperti i primi erbicidi ormono-simili come l’ MCPA (acido 2-metil-4-cloro-fenossiacetico) e il 2,4- D (acido 2,4-diclorofenossiacetico).
Dal 1945 l’industria degli fitofarmaci si è costantemente sviluppata a livello mondiale permettendo l’espansione della moderna agricoltura estensiva.
Attualmente, i composti organoclorurati, organofosforici e carbammati risultano essere messi al bando per la loro pericolosità, ad eccezione di Paesi in cui sussistono problemi di ordine sanitario (malaria, peste, ecc.) o per garantire una elevata resa di produzione a causa della elevata concentrazione demografica (fenomeno della convergenza e della crescita della popolazione nei centri di una regione geografica).
CAPITOLO 2. PESTICIDI
CLASSIFICAZIONE DEI PESTICIDI
I pesticidi possono essere classificati seguendo diversi criteri. Una classificazione può essere formulata in base:
- al meccanismo d’azione nei confronti del bersaglio
- all’organismo bersaglio cui è rivolta l’azione del principio attivo
- alla struttura o al gruppo chimico
- agli effetti sulla salute umana
- al rischio per l’uomo e altre specie animali e vegetali, particolarmenteper l’ambiente acquatico.
CLASSIFICAZIONE IN BASE ALL’ORGANISMO BERSAGLIO
In funzione dell’organismo bersaglio fitosanitari possono essere divisi in :
- Acaricidi : il principio attivo è diretto ad eliminare gli acari. Gli acaricidi sono classificati a sua volta in funzione dello stadio di sviluppo dell’infestante che colpiscono in :
ovicidi
-
- nematocidi
- adulticidi
Generalmente gli acari sono presenti in diversi stadi di sviluppo, quindi per effettuare un trattamento acaricida efficace è opportuno miscelare vari principi attivi.
Questa classe di agrofarmaci è molto vasta e comprende carbammati, organofosfati, formamidine, regolatori di crescita e molti altri.
- Anticrittogamici o Fungicidi: il principio attivo è diretto alla lotta contro i funghi. Il fungicida può essere di tipo preventivo, curativo o antisporulante (impedisce la riproduzione). L’azione del fungicida può essere specifica contro un solo patogeno, o ad ampio spettro cioè rivolta a più patogeni. I fungicidi, in funzione della loro capacità di penetrare nella pianta ed essere traslocati, possono essere classificati in:
Fungicidi di contatto
-
- Fungicidi sistemici
- Fungicidi citotropici
- Fungicidi traslaminari
- Diserbanti o erbicidi: utilizzati contro le erbe infestanti. In funzione della loro capacità di colpire tutte o in parte le specie vegetali presenti, sono classificati in:
Totali
-
- Selettivi
- Fitormoni o Fitoregolatori: agiscono sulla fisiologia e morfologia dei vegetali trattati.
- Insetticidi: esplicano la loro azione tossica nei confronti degli insetti. Anch’essi come i fungicidi possono essere classificati in relazione al loro comportamento nella pianta in:
Insetticidi di contatto
-
- Insetticidi sistemici
- Insetticidi citotropici
- Insetticidi translaminari
- Nematocidi: utilizzati contro i nematodi.
- Rodenticidi: utilizzati contro i roditori.
- Molluschicidi o limacidi: utilizzati contro i limacidi.
CLASSIFICAZIONE CHIMICA
Dal punto di vista chimico è possibile suddividere i pesticidi in 3 grandi gruppi:
- Prodotti inorganici: sono molecole costituite dal elementi inorganici.
- Prodotti organometallici: sono prodotti formati da metalli in coordinazione con composti organici. I composti metallorganici presentano tossicità maggiore rispetto ai corrispondenti prodotti non organometallici, in quanto negli organometallici sono in grado di penetrare molto facilmente le pareti cellulari.
- Prodotti organici naturali e di sintesi: sono tutti derivati del carbonio. Possono essere monofunzionali o polifunzionali. I prodotti organici vengono raggruppati secondo classi omogenee per:
Struttura chimica e proprietà chimico–fisiche: i composti appartenenti alla stessa
famiglia presentano uno o più gruppi funzionali caratteristici che possono influenzare una serie di parametri di importanza fondamentale: proprietà chimico-fisiche della molecola, stabilità chimica, degradazione da parte di microrganismi del suolo o delle
radiazioni solari (foto labilità), meccanismo d’azione, metabolismo, mobilità, tossicità e degradazione.
Si pone, al riguardo, il seguente esempio, anticipando taluni aspetti del capitolo dedicato a tale classe di agrofarmaci:
gli insetticidi di maggior uso comune attualesono, come detto, i piretroidi. Essi sono derivati di sintesi chimica che mimano le proprietà dei corrispettivi naturali, noti e impiegati fin dall’antichità. Di fatto, la “polvere persiana” (di piretro) altro non era che un estratto disseccato dei capolini floreali del Chrisanthemum cinerariefolium, noto alle popolazioni dell’epoca antica per possedere proprietà antiparassitarie. Già nel 1845 vennero identificate le proprietà pesticide in Chrisanthemum cinerariaefolium.
Nel corso della prima guerra mondiale i soldati usavano cospargersi con un unguento preparato estraendo la polvere dei capolini floreali con kerosene per combattere i pidocchi. In seguito, con l’avvento di tecnologie laboratoristiche avanzate, venne scoperto che la polvere di piretro altro non era che una miscela di sei componenti: Piretrina 1 e 2, Cinerina 1 e 2, Yasmolina 1 e 2. Essendo i piretri degli esteri, essi sono formati dalla condensazione di un alcool e di un acido. Fissa la funzione alcoolica, alle denominazione 1 appartengono le piretrine il cui gruppo acido è il crisantemico, mentre alla classe 2 confluiscono le piretrine dotate di gruppo acido denominato piretrico. Tuttavia, tali composti naturali erano dotati di durata di azione alquanto breve (1-2 gg), insufficiente a mantenere in tempi adeguati le attività insetticide. Intervenne, pertanto, l’industria chimica a rintracciare,modellare e sintetizzare (mediante specifiche tecniche
di molecular modelling e molecular dynamics)composti di sintesi denominati piretroidi,
provvisti di caratteristiche tali da prolungarne la durata di azione e la efficacia (potenza di abbattimento dell’organismo parassita).
La criticità dei pesticidi in generale risiede proprio nel fatto di trovare un equilibrio tra durata di azione (strettamente correlata alla persistenza nell’ambiente) e potere abbattente: maggiore è la durata della attività insetticida più è elevata la probabilità di rintracciare residui negli alimenti i quali, a causa dei processi di bioconcentrazione e biomagnificazione, pervengono all’uomo in dosi elevate.
Ciò è quanto è stato dimostrato per il piretro cipermetrina (in figura):l’introduzione di un gruppo ciano (-CN) ne ha potenziato la stabilità, dunque l’efficacia e la persistenza ambientale, ma per esso (e suoi congeneri) si stanno via via incrementando,nel corso del tempo,non esclusivamente per cipermetrina, osservazioni sperimentali sulla manifestazione di patologie implicanti gli organi riproduttivi (ponendosi quale interferente endocrino) accompagnate da evidenze di citotossicità, genotossicità e “probabile” cancerogenicità (ancora in fase di valutazione). Alcuni articoli scientifici dimostrano quanto anzi riportato.
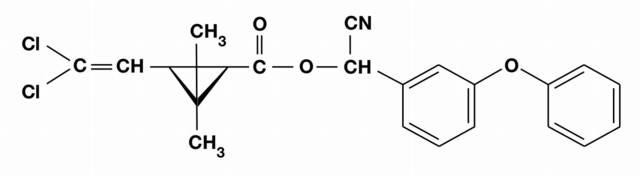
Alkahtane AAet al. Cytotoxicity and Genotoxicity of Cypermethrin in Hepatocarcinoma Cells: A Dose- and Time- Dependent Study.Dose Response. 16, (2018)
Abstract
“Most of the agricultural workers are potentially exposed to pesticides through different routes. Inhalation exposures may result in numerous diseases that can adversely affect an individual’s health and capacity to perform at work. The aim of this study was to determine the cytotoxic potential of cypermethrin pesticide on cultured human hepatocarcinoma (HepG2) cells. The HepG2 cells were exposed to cypermethrin (0, 5, 15, 40 ng/mL) for 24 and 48 hours. We observed that cypermethrin caused cell death of HepG2 cells using 3-(4, 5-dimethylthiozolyl-2)-2,5-diphenyl tetrazolium bromide (MTT) and lactate dehydrogenase tests. Furthermore, cypermethrin reduced HepG2 cells viability in a time and dose dependent basis, that was probably mediated through the induction of reactive oxygen species (ROS) and apoptosis. An increase in ROS generation with a concomitant increase in expression of the proapoptotic protein Bcl-2 and cytochrome c and decrease in the antiapoptosis protein Bax suggested that a mitochondria-mediated pathway was involved in cypermethrin-induced apoptosis. These findings provide insights into the underlying mechanisms involved in cytotoxicity of cypermethrin in HepG2 cells”.
Sharma P. et al. Cypermethrininducedreproductivetoxicity in maleWistar rats: protective role of Tribulus terrestris.J. Environ. Biol. 34,857-62, (2013).
Abstract
The present study was designed to investigate role of ethanolic extract of Tribulus terrestris (EETT) against alpha- cypermethrin induced reproductive toxicity in male Wistar rats. 24 male Wistar rats weighing about 250-300g were divided in four groups. Group-I was control. alpha-cypermethrin (3.38 mg kg-1b.wt.) was given to group-IlI for 28 days. In Group-Ill, alpha-cypermethrin and EETT (100 mg kg -1b.wt.) were administered in combination for 28 days. Rats in group-IV were given EETT for 28 days. At the end of the experiment, rats were sacrificed, testes and epididymis were removed and sperm characteristics, sex hormones and various biochemical parameters were studied. Decrease in weight of testes and epididymis, testicular sperm head count, sperm motility, live sperm count, serum testosterone (T), follicle stimulating hormone (FSH), leutinizing hormone (LH), catalase (CAT), superoxide dismutase (SOD), glutathione S transferase (GST), glutathione reductase (GR), glutathione peroxidase (GPx), total protein content and increase in sperm abnormalities and lipid peroxidation (LPO) level was observed in rats exposed to cypermethrin. In combination group-Ill, EETT treatment ameliorated alpha-cypermethrin induced damage. EETT treatment in group- IV increased testes and epididymis weight, sperm head counts, sperm motility, live sperm counts, testosterone, FSH, LH, GSH, CAT, SOD, GST, GR, GPx and total protein content. The study suggested that Tribulus terrestris plant possess reproductive system enhancement and antioxidant activity.
Madsen C. et al. Immunotoxicity of the pyrethroid insecticides deltametrin and alpha-cypermetrin.Toxicology. 107,219-27, (1996).
Abstract
The synthetic pyrethroids deltametrin and alpha-cypermetrin were studied for effects on the immune system in 28- day studies in F344 male rats. Sixteen rats per group were dosed with either deltametrin 0, 1, 5, or 10 mg/kg body wt./day or alpha-cypermertin 0, 4, 8, or 12 mg/kg body wt./day in soy bean oil by gavage. Haematology, bonemarrow cell counts, tests for natural killer (NK) cell activity and mitogen response (Con A and STM) as well as quantitation of lymphocyte subpopulations were performed. Spleen cells from immunized animals (six animals/group) were tested for antibody production (SRBC-PFC). Volumes of lymphoid compartments of mesenteric lymph nodes and thymus were estimated using stereological methods. In the deltametrin study an effect was found in the groups receiving 5 or 10 mg/kg body wt. The effects were: increased weight of mesenterial lymph nodes, decreased thymus weight in immunized animals and an increase in numbers of SRBC-PFC and splenic NK cell activity. An effect on relative adrenal weight was seen in the 10 mg/kg body wt. group. No severe effects on the immune system was found. The lowest effect level of alpha-cypermetrin was 12 mg/kg body wt./day based on increased relative adrenal weight.
Attività biologica: taluni xenobiotici esibiscono il medesimo meccanismo d’azione e
producono sintomi sovrapponibili. Ad esempio i composti organofosforati o esteri fosforici sono insetticidi che agiscono tutti neutralizzando l’acetilcolinesterasi, un enzima fondamentale per il trasferimento degli stimoli nervosi da un neurone all’altro. Anche tra i fungicidi vi sono alcune classi di prodotti che hanno attività biologica simile ma struttura chimica molto diversa. Ad esempio gli inibitori della biosintesi degli steroli (IBS) pur appartenendo a famiglie chimiche diverse (triazoli, morfoline, ecc.) hanno lo stesso meccanismo d’azione inibendo la sintesi degli steroli.
Analogamente, per i Piretroidi la modalità di azione riproduce quella del DDT (organo fosforico): essi provocano la mancata chiusura dei canali del Na+, con conseguente mancata ripolarizzazione e blocco della conduzione dell’ impulso nervoso, responsabile della paralisi, con morte, degli insetti.
INSETTICIDI ORGANOCLORURATI (OC)
La definizione raggruppa un largo numero di composti, molto diversi per struttura, proprietà ed impieghi, di tre diversi tipi:
-
-
- DDT e composti simili (diclorodifeniletani);
- ciclodieni clorurati (ad esempio, aldrina, edrina, endosulfan II, eptacloro);
- benzeni clorurati cicloesani (esaclorobenzene);
-
In generale gli insetticidi organoclorurati sono solidi stabili che presentano le seguenti caratteristiche:
- Stabilità verso la decomposizione e degradazione ambientale.
- Solubilità estremamente bassa nell’acqua, a meno che nelle molecole non siano presenti anche ossigeno e azoto.
- Solubilità elevata in mezzi simili agli idrocarburi, come le sostanze grasse presenti nella materia vivente.
- Tossicità relativamente elevata verso gli insetti ma alquanto bassa per l’uomo.
Il meccanismo d’azione degli OC è multiplo, perché va ad agire su diversi punti cruciali per il funzionamento cellulare. Modifica la permeabilità allo ione potassio, altera i canali dello ione sodio, inibisce le ATPasi (Sodio-Potassio e Calcio-Magnesio), e favorisce il legame tra lo ione calcio e la calmodulina, che è una proteina intracellulare che permette al calcio di andare a modificare il rilassamento e la contrazione. Tutti questi meccanismi hanno una caratteristica, che è quella di mantenere la cellula in uno stato eccitato (depolarizzazione). A livello del SNC e del SNP si avranno quindi degli effetti avversi,
che si manifestano con un esteso e generalizzato tremore fino ad arrivare ad uno stato convulsivo.
Gli effetti acuti di un’intossicazione da OC sono tremori, eccessiva risposta a stimoli normali e danni a livello del SNC. Gli effetti cronici dovuti ad un contatto prolungato con gli OC sono possibili danni al fegato, al sistema riproduttivo (funzione pro-estrogenica) e maggiore incidenza di tumori epatici (promotore del tumore).
In caso di intossicazione da OC si deve assumere una resina a scambio ionico che è la colestiramina. La funzione di questa resina è di aumentare l’escrezione dell’OC. Oltre al trattamento con la resina, si può intervenire con la somministrazione di un GABAergico (acido γ-amminobutirrico), come una benzodiazepina (diazepam), che riduce il tremore esteso e generalizzato causato dalla sostanza organoclorurata (in questo caso il diazepam come sostanza anticonvulsivante).
IL DDT (PARA-DICLORODIFENILTRICLOROETANO)
Le proprietà insetticide del DDT (para-diclorodifeniltricloroetano) furono scoperte da Paul Müller della Ciba-Geigy, nel 1939.
Esso infatti era estremamente efficace verso le zanzare che veicolano la malaria e la febbre gialla, verso i pidocchi che possono essere il veicolo del tifo esantematico (epidemico o petecchiale) e verso le pulci, insetti veicoli della peste. L’Organizzazione Mondiale della Sanità (OMS o WHO) ha stimato che i programmi di controllo e abbattimento della
malaria, di cui una delle principali componenti era appunto l’uso del DDT, avevano
salvato la vita di oltre cinque milioni di persone. Purtroppo è stato fatto un uso smodato del DDT, soprattutto in agricoltura, nella quale si è consumato l’80% della produzione. Come conseguenza si è assistito a un rapido innalzamento della concentrazione ambientale di questo prodotto a causa della sua persistenza, dovuta alla bassa tensione di vapore e alla conseguente lenta evaporazione, alla sua limitata reattività nei confronti della luce e delle sostanze chimiche presenti nell’ambiente ed infine alla sua bassissima solubilità in acqua.
Strutturalmente, il DDT è un etano sostituito in cui i tre atomi di idrogeno legati a uno dei due atomi di carbonio sono sostituiti da atomi di cloro, mentre due dei tre atomi di idrogeno legati al secondo atomo di carbonio sono sostituiti ciascuno da un anello benzenico); ciascun fenile contiene un atomo di cloro in posizione para.
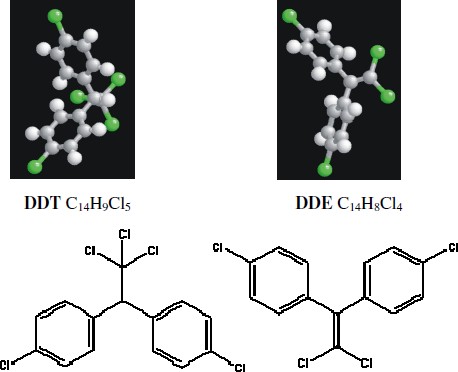
Molte specie animali riescono a metabolizzare il DDT mediante eliminazione di HCl: un
atomo di idrogeno viene rimosso da uno dei due atomi di carbonio dell’etano e un atomo di cloro dall’altro atomo di carbonio, con conseguente formazione di un derivato
dell’etano detto DDE (diclorodifenildicloroetano). Il DDE è prodotto lentamente anche nell’ambiente per effetto della degradazione dei DDT in condizioni alcaline e dagli insetti resistenti, che detossificano così il DDT.
La maggior parte del DDT accumulato nel tessuto adiposo umano è in realtà il DDE contenuto negli alimenti al momento della ingestione e derivato dalla trasformazione del DDT originariamente presente nell’ambiente. Purtroppo il DDE risulta poco biodegradabile ed è estremamente solubile nei tessuti adiposi, e pertanto rimane nel nostro organismo per lungo tempo.
La riduzione della popolazione di numerose specie avicole è ascrivibile al DDE, il quale interferisce con un enzima deputato a regolare la distribuzione del Ca, per cui gli animali cronicamente intossicati producono uova il cui guscio (formato da carbonato di calcio) ha uno spessore insufficiente a sopportare il peso del genitore durante la cova.
Attualmente, per ragioni ambientali, l’uso dei DDT è proibito nella maggior parte dei Paesi industrializzati occidentali; in ogni modo, la sua efficacia si è ridotta con il tempo per la comparsa di popolazioni di insetti resistenti, in grado di metabolizzare il DDT nel DDE privo di funzioni insetticide, rendendolo quindi inattivo. Negli insetti suscettibili, il DDT svolge un’azione letale danneggiando gravemente il sistema nervoso.
I livelli ambientali del DDT e del DDE sono sensibilmente diminuiti nelle regioni dove il loro impiego è stato limitato o del tutto abolito, tuttavia queste sostanze inquinano ancora qualsiasi ambiente come conseguenza del trasporto aerogeno a lunga distanza dalle zone in via di sviluppo dove il DDT viene ancora impiegato per il controllo di malattie come la malaria e il tifo esantematico e murino o per scopi agricoli.
I pesticidi clorurati nel loro complesso sono strutture estremamente stabili a livello ambientale con una persistenza media nel suolo superiore a 18 mesi. L’elevata stabilità dei clorurati nei tessuti degli esseri viventi è alla base del fenomeno della bioconcentrazione.
E’ stato recentemente dimostrato che i pesticidi clorurati interferiscono con i recettori degli ormoni sessuali. Il maggiore metabolita del DDT, il DDE, inibisce il legame degli androgeni al loro recettore e riesce ad inibire l’attività di trascrizione delle proteine androgeno mediate. Questi risultati suggeriscono che il DDT possa avere una azione anti- androgenica interferendo con la maturazione sessuale e l’efficienza riproduttiva maschile.Infine, ulteriori studi (Wetterauer B. et al. Toxicity, dioxin-likeactivities, and endocrine effects of DDT metabolites……Environ Sci Pollut Res Int. 19(2), 403-15, 2012),riferiscono che il DDT ed i suoi metaboliti, oltre a risultare interferenti endocrini, possiedono una marcata attività citotossica.
La IARC ha classificato il DDT tra i possibili cancerogeni per l’uomo (gruppo 2B)
INSETTICIDI ORGANOFOSFORICI (OP)
Il capostipite degli organofosforici è il PARATHION. Quest’ultimo dev’essere bioattivato per esplicare le proprie attività tossiche. Dal PARATHION si è tentato di generare degli altri composti di sintesi molto più selettivi e meno tossici per l’uomo. Uno di questi prodotti di nuova sintesi è il MALATHION.
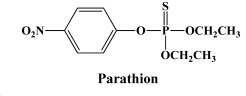
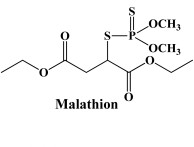
Il meccanismo d’azione è l’inibizione dell’AChE (acetilcolinesterasi). L’antidoto per eccellenza è la PRALIDOSSIMA, che è in grado di staccare l’organofosforico dal sito esterasico. La pralidossima deve essere somministrata nel più breve tempo possibile, perché l’enzima va in contro ad invecchiamento rendendo molto stabile il legame tra gruppo fosforico e sito esterasico. L’inibizione dell’AChE (l’insetticida vi rimane legato per ore) impedisce la degradazione del neurotrasmettitore acetilcolina (ACh) il quale, pertanto, permane a lungo nello spazio sinaptico andando a stimolare oltremodo i recettori postsinaptici. Gli effetti tossici degli organofosforiciconsistono in:
- negli insetti: alterazioni degli impulsi nervosi essenziali per il coordinamento dei
processi vitali, fino alla paralisi e morte.
- nell’uomo:(dipendentemente dalla dose assunta e da una esposizione acuta o cronica):
- Alterazioni sensoriali, del comportamento e incoordinazione motoria.
- Maggiore attività delle ghiandole (maggiore salivazione, sudorazione e lacrimazione);
- Pupille a punta di spillo;
- Incapacità di messa a fuoco gli oggetti;
- Aumento della peristalsi intestinale;
- Ipotensione e bradicardia;
- Broncocostrizione e stimolazione delle secrezioni bronchiali;
- Contrazione involontaria dei muscoli scheletrici.
- Nei casi più gravi si può giungere a depressione respiratoria e paralisi.
Questi composti OP sono molto lipofili, non sono considerati teratogeni e/o cancerogeni e sono maggiormente allontanabili dall’ambiente rispetto agli OC.
Il contatto tra organismo ed OP può avvenire per via orale, per via inalatoria e per via cutanea. La morte per insufficienza respiratoria, se non si interviene tempestivamente, subentra nell’arco delle 24 ore.
Il trattamento in caso di intossicazione da organofosforici:
- Monitoraggio cardiaco;
- Respirazione artificiale;
- ATROPINA, un bloccante dei recettori muscarinici (fino a 5 mg e.v. ogni 20 minuti) ed è l’antagonista per eccellenza dell’acetilcolina. La somministrazione dell’atropina avviene solamente nei casi più gravi di intossicazione.
- PRALIDOSSIMA somministrata velocemente prima che l’enzima invecchi.
La IARC ha classificato il PARATHION come “possibile cancerogeno” per l’uomo (gruppo 2B), sulla base di evidenze di cancerogenicità negli animali da laboratorio, l’insetticida MALATHION è stato classificato come “probabile cancerogeno” per
l’uomo (gruppo 2A).
Per l’insetticida MALATHION, vi è limitata evidenza di cancerogenicità nell’uomo per linfoma non-Hodgkin e cancro alla prostata, derivante da studi, pubblicati a partire dal 2001, sull’esposizione in agricoltura negli Stati Uniti, in Canada e in Svezia. Il MALATHION inoltre causa tumori nei roditori, provoca danni al DNA e ai cromosomi, nonché a livello ormonale.
INSETTICIDI CARBAMMATI
I carbammati hanno più o meno lo stesso effetto degli organofosforici. In seguito al loro ingresso nell’organismo, infatti, l’enzima aceticolinesterasi (AChE) viene carbamilato, di conseguenza reso inattivo. Il legame tra enzima e carbammato, però, non è così resistente come quello tra AChE ed organofosforici. L’enzima, infatti, viene reso di nuovo disponibile dopo qualche ora, quindi il legame che si è formato è di tipo reversibile e non va in contro ad invecchiamento.
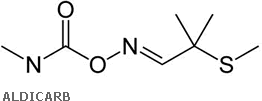
In caso di intossicazione da carbammati si impiega il prodotto bloccante muscarinico per eccellenza, che è l’atropina.
Il composto più tossico appartenente alla categoria dei carbammati è l’ALDICARB. Quest’ultimo possiede una DL50 per via orale di 1mg/Kg nel ratto o nel topo.
Come gli OP, sono facilmente degradabili da molti agenti chimici e biochimici e non presentano in genere problemi di persistenza.
La tossicità acuta per l’uomo è di rilievo, ma poiché la loro stabilità chimica è modesta e la degradazione biologica rapida, ne deriva tuttora un notevole impiego. Sono composti tossici come gli organofosforici ma poiché la dose letale (DL) per via transcutanea è più elevata rispetto a quella degli OP, risultano meno pericolosi da maneggiare.
La IARC ha classificato gli OP nel Gruppo 3 (non classificati per cancerogenicità sull’uomo).
PIRETROIDI E PIRETRINE
Il Piretro viene estratto dai fiori del Chrysanthemumcinerariaefolium (Asteraceae), una pianta erbacea perenne originaria dell’Iran, successivamente diffusa in diverse parti del mondo a diverse latitudini.

La quasi totalità degli insetticidi attualmente in
commercio sono a base di piretrine e piretroidi
PIRETRINE

Crisanthemum c.
 Le piretrine agiscono attaccando il sistema nervoso degli insetti a livello dei gangli nervosi e delle sinapsi, bloccando i canali del sodio. L’effetto sugli insetti è riassumibile in: rapida mancanza di coordinazione dei movimenti, convulsioni e conseguente paralisi. L’azione tossica è comunque di breve durata e spesso insufficiente a provocare la morte dell’insetto, in quanto il principio attivo viene rapidamente metabolizzato. Quando le piretrine non sono presenti ad una concentrazione letale, esse mostrano un effetto repellente. Per aumentare la stabilità dei formulati, il Piretro viene comunemente miscelato con il Piperonylbutossido, un estratto dall’olio di sassofrasso. Questo esercita un’azione sinergizzante bloccando il sistema di detossificazione degli insetti. Lo spettro di attività del Piretro è molto ampio e risulta efficace contro un’ampia gamma di insetti. I settori di impiego di questo insetticida naturale sono molteplici e vanno dalla frutta ai vegetali, dalle piante ornamentali e forestali, alla disinfestazione delle sementi e
Le piretrine agiscono attaccando il sistema nervoso degli insetti a livello dei gangli nervosi e delle sinapsi, bloccando i canali del sodio. L’effetto sugli insetti è riassumibile in: rapida mancanza di coordinazione dei movimenti, convulsioni e conseguente paralisi. L’azione tossica è comunque di breve durata e spesso insufficiente a provocare la morte dell’insetto, in quanto il principio attivo viene rapidamente metabolizzato. Quando le piretrine non sono presenti ad una concentrazione letale, esse mostrano un effetto repellente. Per aumentare la stabilità dei formulati, il Piretro viene comunemente miscelato con il Piperonylbutossido, un estratto dall’olio di sassofrasso. Questo esercita un’azione sinergizzante bloccando il sistema di detossificazione degli insetti. Lo spettro di attività del Piretro è molto ampio e risulta efficace contro un’ampia gamma di insetti. I settori di impiego di questo insetticida naturale sono molteplici e vanno dalla frutta ai vegetali, dalle piante ornamentali e forestali, alla disinfestazione delle sementi e
all’impiego domestico.
Le piretrine risultano essere moderatamente tossiche per i mammiferi, la dose letale acuta orale nei ratti (DL50) è compresa tra 350 e 500 mg/kg, mentre il prodotto tecnico è considerevolmente meno tossico (vedi tabella 2.1). Nonostante questo principio attivo sia estremamente fotolabile e quindi facilmente degradato alla luce solare, in alcune colture mostra una certa persistenza probabilmente perché le piretrine, penetrando nelle cere epicuticolari, vengono protette dalla fotodegradazione. Inoltre le piretrine vengono anche utilizzate per proteggere le granaglie durante la conservazione nei silos. Uno studio condotto su grano duro ha mostrato che nelle normali condizioni di conservazione questi composti sono molto stabili, infatti i tempi di semivita delle piretrine erano rispettivamente di 46 e 72 giorni. Ciò dipende probabilmente dal fatto che le piretrine, durante la fase di conservazione, non subiscono gli effetti degradativi legati alla radiazione solare. I Piretroidi che ritroviamo sul mercato, invece, sono analoghi sintetici delle piretrine (composti naturali), sviluppati soprattutto con lo scopo di aumentarne la durata di azione.
Basandosi sui sintomi prodotti sugli animali i piretroidi si distinguono in due categorie: di tipo I e di tipo II.
Sono entrambi lipofili e pertanto i loro target sono le membrana biologiche. Mentre i piretroidi di tipo I agiscono sui canali del sodio localizzati nelle membrane neuronali e muscolari producendo ripetuti impulsi nervosi, quelli di tipo II producono invece lunghi ritardi nei canali del sodio inattivando la via che porta ad una persistente depolarizzazione delle membrane senza scariche ripetute. In aggiunta a questo la sindrome del tipo II implica anche il sistema nervoso centrale, mentre il primo tipo porta
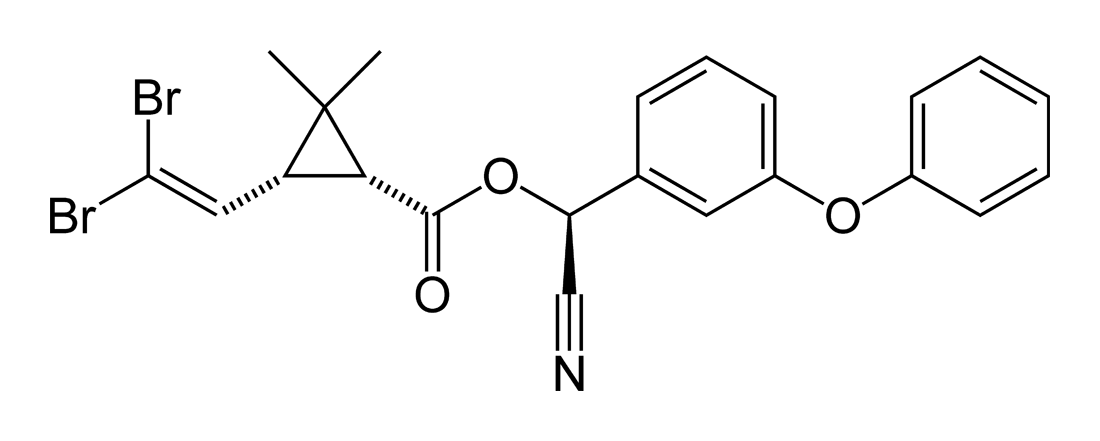 ad un’involuzione del sistema nervoso periferico. Per citarne alcuni, sono piretroidi di tipo I: piretrina, alletrina, resmetrina, tetrametrina, permetrina; al tipo II appartengono cipermetrina, deltametrina, fenvalerato.
ad un’involuzione del sistema nervoso periferico. Per citarne alcuni, sono piretroidi di tipo I: piretrina, alletrina, resmetrina, tetrametrina, permetrina; al tipo II appartengono cipermetrina, deltametrina, fenvalerato.
La Deltametrina è un piretroide sintetico di tipo II.
Altra fondamentale differenza tra i piretroidi di tipo I e II e che in questi ultimi è stato introdotto un gruppo ciano (-CN) che ne aumenta ulteriormente la potenza d’azione (fino a 7 volte quella del tipo I), senza dar luogo nell’uomo a intossicazioni di tipo cianidrico in quanto gran parte dei metaboliti ritrovati sono costituiti da tiocianati, innocui.
Numerosi studi hanno mostrato che i piretroidi causano alterazioni nei sistemi biochimici del sangue e della riproduzione, mentre sono limitati gli studi che descrivono lo stress ossidativo nella tossicità indotta con i piretroidi. Nell’uomo vengono metabolizzati molto rapidamente, molto più di quanto accade negli insetti, con conseguente riduzione della tossicità.
Dopo l’inalazione d’insetticidi piretroidi possono essere osservati alcuni sintomi quali: tosse, affanno, mancanza di fiato, naso chiuso o con secrezioni mucose, dolori al petto e
difficoltà respiratorie. Il contatto con la pelle può causare eruzioni cutanee, prurito e vesciche. Per quelli che contengono un gruppo CN sono stati inoltre descritti episodi di tossicità sistemica caratterizzati da parestesie (secondarie al blocco dei canali del sodio), nausea, vomito, fascicolazioni, alterazioni dello stato mentale, coma, convulsioni ed edema polmonare.
Per quanto riguarda i composti di origine naturale, non sono descritti casi di intossicazione sistemica. Questi composti, tuttavia, in caso di ingestione possono provocare nausea, vomito e diarrea.
CAPITOLO 3. I NEONICOTINOIDI
L’uomo ha da sempre cercato di controllare la diffusione degli insetti infestanti sia per questioni di salute pubblica che per la protezione dei raccolti. A questo scopo i solfuri sono
stati i primi insetticidi ad essere usati per il controllo dei parassiti e sono tuttora utilizzati in vaste regioni della California e in altre aree del mondo.
Negli ultimi vent’anni il mercato degli insetticidi è stato dominato da tre classi chimiche principali; come già discusso in precedenza nel testo, la prima è quella degli Organofosfati che agiscono analogamente ad una neurotossina, la seconda classe chimica è costituita dai Carbammati che causano un avvelenamento degli inibitori della colinesterasi e l’ultima classe è formata dai Piretroidi che agiscono anche come inibitori di un enzima epatico dei parassiti. La loro abilità nel controllare gli insetti infestanti è andata però scemando nel tempo poiché questi ultimi hanno sviluppato una resistenza verso queste tre classi di insetticidi costringendo quindi l’uomo a sviluppare nuovi composti adatti allo scopo prefissato.
Anche la sicurezza dell’ambiente è diventata una prerogativa sempre più importante. Iconsumatori con il passare del tempo richiedevano un insetticida con minor impatto ambientale ma sempre più efficace nel combattere i parassiti. Molti insetticidi sono stati sviluppati cercando di soddisfare queste due richieste, ma quelli che hanno avuto più successo sono stati i neonicotinoidi grazie alla loro eccellente efficacia e alla loro relativamente (inizialmente) bassa tossicità nei confronti dell’ambiente e dei mammiferi. Il loro maggior pregio, rispetto ai pesticidi di vecchia concezione, è la selettività poiché mentre sono fortemente attivi nei confronti degli insetti essisembravano esserloin maniera quasi trascurabile nei confronti dei mammiferi.“Sembravano esserlo” perché, come affrontato in seguito, a distanza di anni anche per essi sono emerse evidenze di tossicità.
La storia dei neonicotinoidi inizia nel 1970, anno in cui la Shell Chemical Company intraprende una ricerca volta alla sintesi di nuovi insetticidi. Inizialmente, l’attenzione è puntata sul composto 2-dibromonitrometil-3-metilpiridina, sul quale vengono effettuati vari test da cui emerge che la molecola è dotata di una blanda azione insetticida.Vengono, quindi, apportate delle modifiche alla struttura della 2-dibromonitrometil-3- metilpiridina e nasce la nitiazina, un nitrometilene eterociclico con buona attività insetticida ma fotosensibile, caratteristica che non lo rende utilizzabile in agricoltura.
Nel 1983, la Nihon Bayer introdusse come sostituente un gruppo eteroarilmetilecontenente azoto e questo fece aumentare notevolmente l’attività insetticida di questo prodotto durante i loro esperimenti. Questo composto, grazie ad ulteriori studi, portò alla
scoperta dell’Imidacloprid, seguito poi dal Nitenpyram nel 1987, dall’Acetamiprid nel 1989 e dal Thiamethoxam scoperto in Giappone dal gruppo Ciba nel 1992. Successivamente molte altre molecole neonicotinoidi furono sintetizzate fra cui le più importanti sono state ilThiacloprid da parte della Bayer, il Clothianidin da parte della Takeda e il Dinotefuran dalla MitshuiChemicals.
CARATTERISTICHE GENERALI
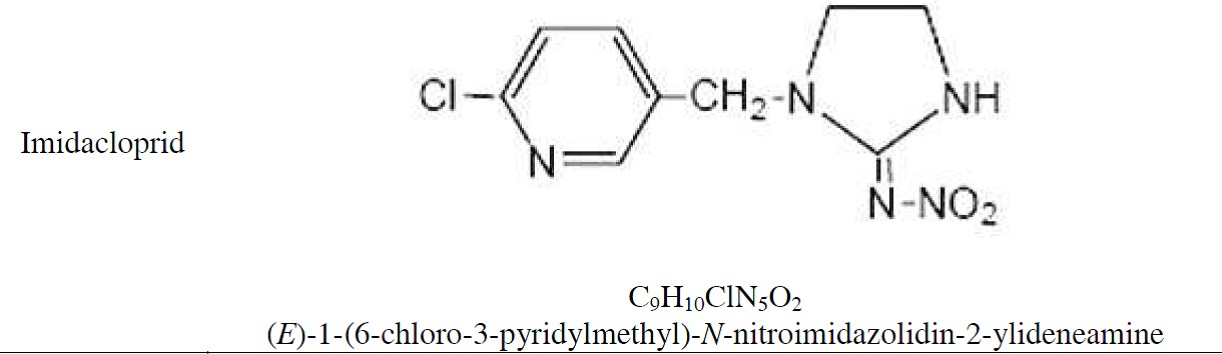
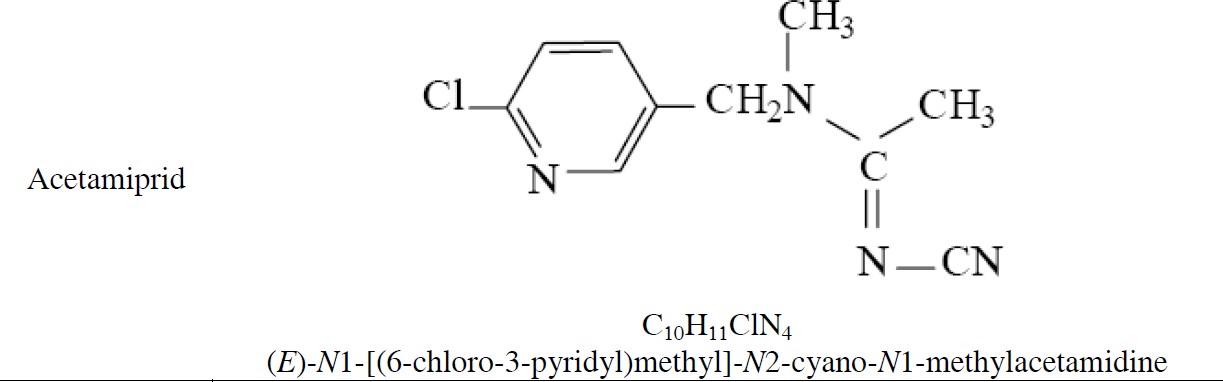
Sono di seguito riportate, alcune informazioni riguardanti i principi attivi insetticidi. Tabella 1: Formula di struttura, formula chimica e nome IUPAC dei p.a. indagati


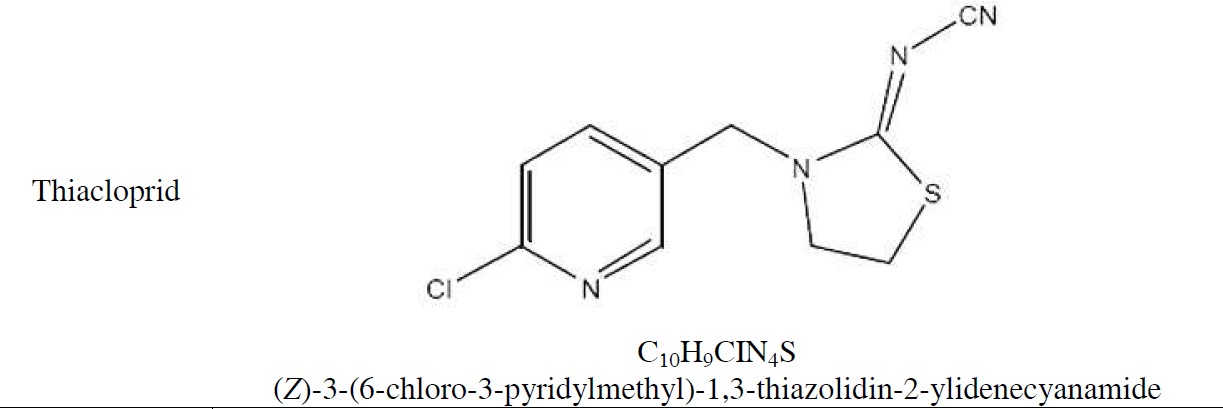
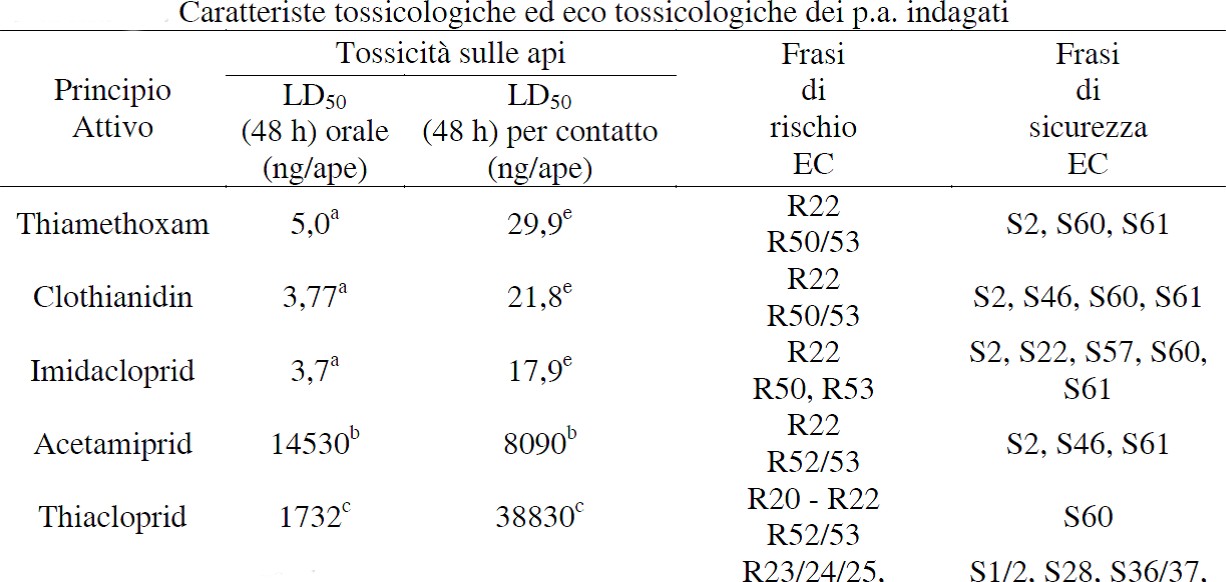
MODALITÀ D’AZIONE
I neonicotinoidi agiscono come agonisti sui recettori postsinaptici nicotinici dell’acetilcolina (nAChR) bloccando la normale azione di scambio di ioni attivata dall’acetilcolina.L’acetilcolina (ACh) è infatti l’agonista endogeno e il neurotrasmettitore del sistema nervoso colinergico. Le neurotrasmissioni attraverso le sinapsi sono mediate in due passaggi come descritto in figura 1; prima l’acetilcolina è rilasciata dalla membrana presinaptica tramite esocitosi e interagisce con il sito di legame localizzato nel dominio extracellulare del complesso costituito dal canale ionico del recettore nicotinico dell’acetilcolina. Nel secondo passaggio una modificazione conformazionale della molecola del recettore porta all’apertura del canale, permettendo l’ingresso di cationi Na+ extracellulare e l’uscita di cationi K+ intracellulare per mantenere lo stato di equilibrio del potenziale di membrana. Negli insetti i recettori nicotinici dell’acetilcolina sono predominantemente distribuiti nella regione del neuropilo del sistema nervoso centrale (SNC).
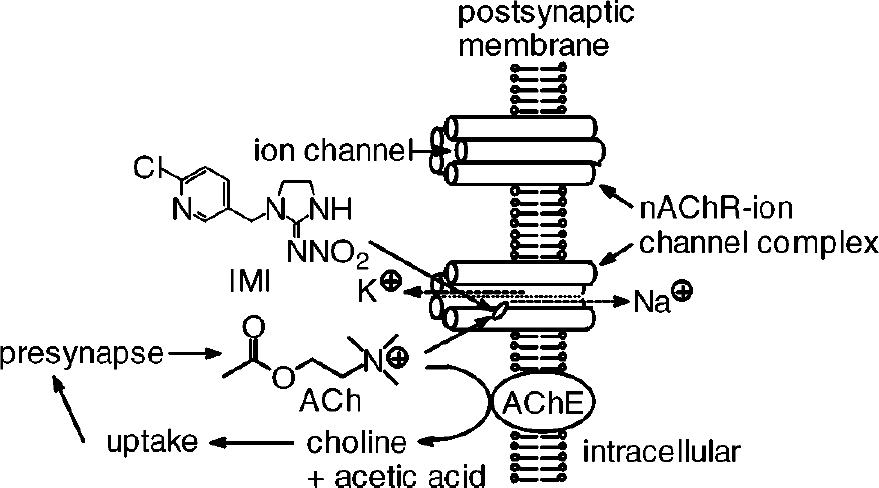
Figura 1: Neurotrasmissioni colinergiche mediate dal recettore nicotinico dell’acetilcolina (nAChR) sulla membrane postsinaptica. Il neurotrasmettitore ACh rilasciato dalla presinapsi si lega al nAChRportando all’attivazione del canale ionico. L’acetilcolina è successivamente idrolizzata dall’enzima acetilcolinesterasi (AChE).
Il grande vantaggio degli insetticidi neonicotinoidi è la selettività. La caratteristica decisiva per la selettività dei neonicotinoidi rispetto all’nAChR degli insetti sembra essere la zona carica negativamente del gruppo nitro o ciano presente nei neonicotinoidi stessi. Questa carica infatti è in grado di formare legami ad idrogeno o interazioni di tipo elettrostatico con i residui cationici degli amminoacidi presenti in quella zona quali la lisina, l’arginina o l’istidina.
Nei recettori nicotinici dell’acetilcolina dei mammiferi, invece, la zona dove si andrebbero a posizionare i gruppi carichi negativamente dei neonicotinoidi è anch’essa negativa e causerebbe quindi una repulsione dei neonicotinoidi stessi da quel sito che non viene quindi da loro occupato.
Tuttavia, a partire dagli anni ’90 si è osservato un incremento della mortalità delle api che va sotto il nome di Sindrome da Spopolamento degli Alveari (SSA). In aggiunta, le api rivestono il ruolo di principale insetto impollinatore, perciò se il fenomeno della SSA comporta problematiche di interesse prettamente economico legate a una ridotta produzione qualitativa e quantitativa del miele ed altri prodotti apistici, resta il fatto che esse rappresentano bioindicatori estremamente sensibili rispetto allo stato di contaminazione da pesticidi in un determinato ecosistema e di cui tener debitamente conto.
EFFETTI SULLE API QUALI INDICATORI BIOLOGICI
Come già anticipato in Prefazione, la Sindrome da Spopolamento degli Alveari (SSA; in inglese altrimenti nota come CCD = Colony Collapse Disorder) non solo è indicativa di un impatto ambientale negativo imputabile alla presenza di uno o più xenobiotici, bensì incide negativamente sulle aziende apistiche (spesso a conduzione familiare) altamente penalizzate dal punto di vista della produzione mellifera.
Gli effetti subletali dei neonicotinoidi sulle api si possono dividere in due categorie: quelli fisiologici e quelli comportamentali. Per quanto riguarda quelli fisiologici vi sono in primo luogo gli effetti a livello dei recettori nicotinici dell’acetilcolina descritti in precedenza e in secondo luogo un aumento dell’attività della Citocromo Ossidasi (CO) che controlla la respirazione e l’attività enzimatica celebrale. Inoltre, si osserva una perturbazione nello sviluppo neurale delle larve, una longevità delle api adulte decisamente ridotta e un danneggiamento dei tessuti dell’intestino.
Per quanto concerne invece gli aspetti comportamentali, molti di questi sono dipendenti dagli effetti neuronali precedentemente indicati. Si è osservato che per bassissimi dosaggi (fino ad 1,25 ng/ape di Imidacloprid) l’attività motoria delle api risulta aumentata mentre aumentando le dosi di pesticida fornito alle api (da 2,5 a 20 ng/ape) queste tendono a diminuire sempre più i loro movimenti.
Un secondo effetto comportamentale è quello legato alla navigazione e all’orientamento che dipendono dalle trasmissioni nervose e sono legati alla vista dell’ape; si è verificato che le api, una volta contaminate con questi principi attivi, acquisiscono in maniera
sfalsata le immagini perdendo totalmente o in parte l’orientamento e ciò le porta a vagare
senza riuscire più a ritornare all’arnia. I molti esperimenti effettuati hanno infatti dimostrato come il recupero del cibo da parte delle api richiedesse da parte loro un tempo sempre maggiore all’aumentare del dosaggio di neonicotinoide, causando inoltre una variazione nei percorsi e addirittura la perdita dell’ape o per alcune ore o per giorni o peril resto della sua esistenza.
Un terzo aspetto di queste modificazioni è la difficoltà nell’approvvigionamento del cibo.Questa è causata da una ridotta capacità olfattiva che si spiega con delle alterazioni nei riflessi di estensione della proboscide (PER, Proboscis Extension Reflex) nonché dalla ridotta sensibilità delle antenne a percepire le fonti di saccarosio. Essendo il PER deputato alla memorizzazione di gusti ed odori, se esso non funziona correttamente le api bottinatrici non sono più in grado di riconoscere il cibo, di portarlo all’arnia e di sfamare le altre api e loro stesse. Questa perdita di memoria è stata verificata in molti studi e si è osservato che la parte di memoria intaccata in dosi subletali per questo tipo di insetticidi è quella a breve emedio termine. Altri studi hanno verificato una riduzione o una totale sparizione della comunicazione tra ape ed ape sui luoghi dove recuperare il cibo, effettuata, nel caso di api in salute, attraverso la cosiddetta “waggling dance”. Questa danza consiste normalmente in un movimento ad “otto” effettuato con una determinata angolazione e con un preciso numero di vibrazioni dell’addome come si può vedere in figura 1.1. In particolare la direzione della parte vibratoria della waggling dance fornisce informazioni rispetto all’angolazione con il sole della risorsa di cibo, mentre la sua durata fornisce informazioni rispetto alla distanza che si è stabilito corrispondere a circa 1 km per ogni secondo di vibrazione.
Di seguito sono proposti due, tra i più recenti articoli, alquanto esemplificativi, pubblicati
su riviste internazionali relativi ad osservazioni sulle api e loro alterato comportamento,
come conseguenza dell’impiego intensivo di agrofarmaci.
- P. Chronic Toxicity of clothianidin, imidacloprid, chlorpyrifos, and dimethoate to Apis mellifera L. larvae reared in vitro.Pest Manag Sci. 2018, (ahead of print)
Abstract
“The effects of chronic exposure to two neonicotinoids (clothianidin and imidacloprid) and two organophosphates (chlorpyrifos and dimethoate) on survival, developmental rate and larval weight of honey bee larvae reared in vitro were determined. Diets containing chemicals were fed to larvae with the range of concentrations for each compound based on published acute toxicity experiments and residues found in pollen and nectar, both components of the larval diet.
RESULTS:
Four concentrations of each compound and controls were tested: chlorpyrifos: 0.5, 0.8, 1.2, 8 mg/L; clothianidin: 0.1, 0.4, 2, 10 mg/L; dimethoate: 0.02, 1, 6, 45 mg/L; imidacloprid: 0.4, 2, 4, 10 mg/L; positive control: dimethoate (45 mg/L); solvent control: acetone or methanol; and negative control. A significant decrease in survival, relative to the solvent control, occurred in the 0.8, 1.2 and 8 mg/L chlorpyrifos, 0.4, 2 and 10 mg/L clothianidin, and 45 mg/L dimethoate diets, but not the imidacloprid diets.
CONCLUSION:
The treatment of larval diets with clothianidin, dimethoate and imidacloprid did not affect survival, developmental rate, or weight of immature honey bees; however, treatment with chlorpyrifos did. Overall, our results are valuable for evaluating the chronic toxicity of these pesticides to developing honey bees.
- Li G. et al. The Wisdom of Honeybee Defenses Against Environmental Stresses, Front Microbiol, 1,9, 722, (2018)
Abstract
As one of the predominant pollinator, honeybees provide important ecosystem service to crops and wild plants, and generate great economic benefit for humans. Unfortunately, there is clear evidence of recent catastrophic honeybee colony failure in some areas, resulting in markedly negative environmental and economic effects. It has been demonstrated that various environmental stresses, including both abiotic and biotic stresses, functioning singly or synergistically, are the potential drivers of colony collapse. Honeybees can use many defense mechanisms to decrease the damage from environmental stress to some extent. Here, we synthesize and summarize recent advances regarding the effects of environmental stress on honeybees and the wisdom of honeybees to respond to external environmental
stress. Furthermore, we provide possible future research directions about the response of honeybees to various for of stressor.
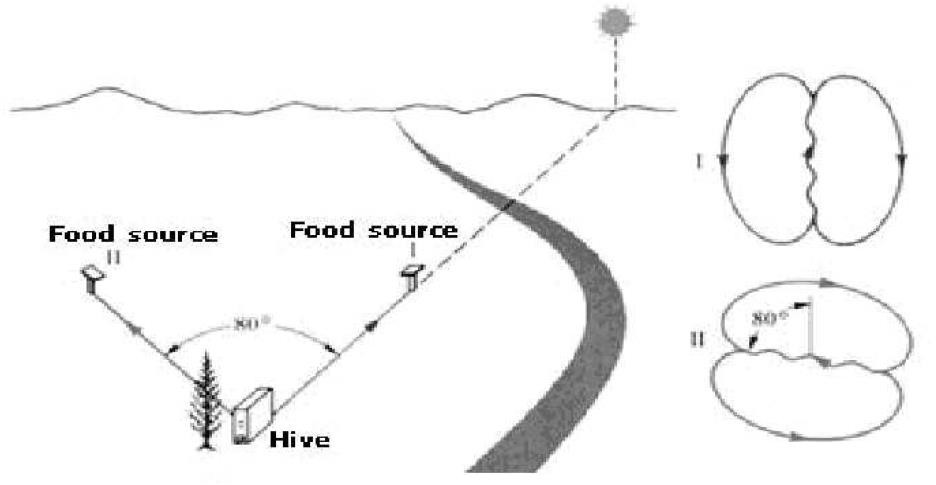
Figura 1.1 Diversa orientazione della direzione della waggling dance aseconda della posizione della fonte di cibo rispetto all’asse sole
– alveare.
Questa interruzione delle comunicazioni fa si che un numero sempre maggiori di api sia costretto a lasciare l’arnia alla ricerca di cibo senza però conoscerne già l’ubicazione, portando così in breve tempo ad uno spopolamento dell’alveare e a un successivo drastico declino della colonia vista la penuria di cibo. Altri effetti osservati e riportati in letteratura sono l’apatia, la respirazione affannosa, la perdita di coordinazione e le convulsioni.
Dosi letali di questi principi attivi generano stati di eccitazione permanente che portano poi alla morte per paralisi.
DISPERSIONE NELL’AMBIENTE
I principi attivi neonicotinoidi sono comunemente utilizzati su semi (come concianti), sui suoli coltivati e sui prati (sparsi in formulazione granulare o tramite spray), su strutture (per la loro disinfestazione dalle termiti), nei frutteti tramite l’uso di spray ed infine come trattamentotopico sugli animali domestici per l’eliminazione delle pulci. Per quanto riguarda uno diquesti principi attivi come l’Imidacloprid sono stati registrati nel solo Connecticut 247prodotti a base di questo principio attivo e ciò può dare un’idea, seppur parziale, della loroestrema diffusione. Il loro massiccio utilizzo in agricoltura è effettuato per laprotezione delle colture da parassiti quali la diabrotica e le larve di scarafaggio, ma anche perle locuste e altri insetti succhiatori, come gli afidi, e masticatori come le cavallette e gliscarafaggi. Nonostante questa loro utilità nella salvaguardia delle colture sia messa indubbio da alcuni studi, il giro d’affari per il 2008 della Bayer solo per quanto riguarda ilClothianidin è dell’ordine dei 240 milioni di euro all’anno, mentre il suo reparto sementiha avuto globalmente nel 2007 un giro d’affari pari a 5,8 miliardi di euro.Per quanto concerne il mercato internazionale dei prodotti concianti si è passati dagli iniziali 155 milioni di euro registrati nel 1990, ai 535 milioni di euro registrati nel 2005, di cui il 77% del totale dovuti all’utilizzo di principi attivi neonicotinoidi.
E’ facile quindi intuire che gli interessi su questi principi attivi sono notevoli.
LA CONCIA DELLE SEMENTI
L’operazione di concia delle sementi è una pratica sviluppata da più di una quindicina d’anni che consiste nell’avvolgere il seme da piantare in una pellicola contenente una certa dose difitofarmaco. Tale composto, se agisce in modo sistemico come nel caso dei neonicotinoidi,viene portato all’interno dei tessuti della pianta una volta che questa inizia il suo processo disviluppo proteggendola quindi su gran parte dei tessuti ed assicurando una buona persistenzadella protezione sia dai principali fitofagi radicali, sia dai principali insetti fitofagi e fitomiziche attaccano i tessuti aerei della pianta. Questa modalità di impiego degli agrofarmaci haportato ad una forte riduzione delle quantità di questi prodotti necessarie per un’adeguataprotezione delle colture nei campi rispetto alle precedenti tecniche agronomiche utilizzate.Queste prevedevano infatti l’uso massiccio di geodisinfestanti o di prodotti irrorati con spray.Con questa modalità di somministrazione si sono così ridotte drasticamente le quantità di p.a.disperse nell’ambiente con relativi vantaggi sia economici che ambientali.
L’uso dei concianti, nel tempo, è stato esteso oltre che al mais anche a molte altre colture quali il cotone, la colza, il girasole e la barbabietola da zucchero.
DESTINO AMBIENTALE
SEMINA E POLVERI
Anche se la pratica della concia delle sementi sembrava ridurre i problemi di dispersione dovuti all’impiego di prodotti di sintesi, prendeva consistenza l’ipotesi che tali principi attiviutilizzati nelle conce fossero la cause dello spopolamento degli alveari.
In particolare, studi effettuati in Italia fra il 2004 ed il 2006 e coordinati dal Consiglio per la Ricerca e la Sperimentazione in Agricoltura (CRA-API) ed alcune Università italianeverificarono come la semina con seminatrici pneumatiche di sementi di mais contenentifitofarmaci fosse la causa del rilascio nell’ambiente di una notevole percentuale in massa ditali prodotti sotto forma di polveri create con l’abrasione meccanica dei semi che avvieneall’interno del macchinario.
Ulteriori studi a livello regionale o di istituti privati hanno confermato come le semine dimais conciato con principi attivi insetticidi potessero essere responsabili della morte di molteapi ritrovando, in campioni di api morte fornite da singoli apicoltori o raccolti da istitutiveterinari regionali, dosi rilevanti di diversi principi attivi insetticidi utilizzati nella concia delmais.
Seppur esistano studi effettuati dalla Bayer che cercano di negare che la morte delle apipossa in qualche modo essere riconducibile all’abrasione delle sementi conciate e allasuccessiva dispersione di queste nell’aria, numerose ricerche scientifiche bendocumentate hanno comprovato come invece questo rapporto esista e sia particolarmenteforte. In particolare, da tali ricerche si è evidenziato che vi possono essere
due tipi diinterazione tra le api e le polveri prodotte dalle seminatrici: una diretta, causata dal passaggiodelle api nei campi durante i periodi di semina e una indiretta dovuta alla deposizione diqueste polveri sulla flora circostante i campi in questione con cui le api possono venire acontatto nei giorni successivi alla semina.
Proprio in Italia Moreno Greatti del Laboratorio Apistico Regionale, Dipartimento di Biologia applicata alla Difesa delle Piante, Università di Udine, nel2003 aveva già evidenziato nel suo studio “Risk of environmentalcontamination by the activeingredientimidaclopridused for cornseeddressing. Preliminary results”), come i principi attivi neonicotinoidi, sotto forma di una polvere generata dall’abrasione del seme conciato durante le fasi di semina, venissero dispersi come nube dalle seminatrici durante il lavoro e potessero perdurare nell’ambiente fino ad 8 giorni dalla semina, aumentando cosìnotevolmente i tempi per una possibile contaminazione delle api rispetto ad un evento disostanziale breve durata come la semina.
Le moderne seminatrici sono per la quasi totalità di tipo pneumatico ad alta precisione epermettono di seminare a distanze regolabili un determinato numero di semi per metroquadrato.
LA GUTTAZIONE FOGLIARE E LA DISTRIBUZIONE NELLE PIANTE
Negli stadi giovanili di alcune specie di piante terrestri si osserva un particolare fenomenodi fuoriuscita di acqua, localizzato soprattutto alle estremità fogliari, chiamato
“guttazione”. Tale processo fisiologico, da non confondere con la normale traspirazione fogliare, permettead un’aliquota d’acqua di uscire attraverso specifici fori posizionati lungo i lembi fogliari,denominati idatodi.
 La guttazione ha luogo quando l’elevata pressione radicale dell’acqua non riesce ad esser controbilanciata totalmente dalla traspirazione fogliare e perciò una frazione di quest’acquaviene dirottata all’esterno attraverso gli idatodi. Tale situazione si verifica quindi in piante conelevate disponibilità d’acqua nel terreno ed in situazioni di chiusura degli stomi fogliari conlimitata traspirazione. Per questo motivo il fenomeno della guttazione si manifestasoprattutto durante la notte quando gli stomi sono prevalentemente chiusi per la ridotta attivitàmetabolica ed il livello d’umidità atmosferica risulta più elevato. Le gocce di guttazione(figura 1.2) sono quindi ben visibili sulle foglie il mattino ma questo processo si puòosservare durante tutto l’arco della giornata seppur in misura inferiore.
La guttazione ha luogo quando l’elevata pressione radicale dell’acqua non riesce ad esser controbilanciata totalmente dalla traspirazione fogliare e perciò una frazione di quest’acquaviene dirottata all’esterno attraverso gli idatodi. Tale situazione si verifica quindi in piante conelevate disponibilità d’acqua nel terreno ed in situazioni di chiusura degli stomi fogliari conlimitata traspirazione. Per questo motivo il fenomeno della guttazione si manifestasoprattutto durante la notte quando gli stomi sono prevalentemente chiusi per la ridotta attivitàmetabolica ed il livello d’umidità atmosferica risulta più elevato. Le gocce di guttazione(figura 1.2) sono quindi ben visibili sulle foglie il mattino ma questo processo si puòosservare durante tutto l’arco della giornata seppur in misura inferiore.
Figura 1.2: Particolare di gocce di guttazione sull’estremità di una foglia di mais
La produzione di acqua di guttazione da parte delle piante di mais è un fenomeno che siverifica limitatamente alle prime tre settimane di vita. La produzione da ogni singola pianta siattesta su volumi che variano tra gli 0,1 ml e i 0,3 ml al giorno nei periodi iniziali di forteproduzione, diminuendo a volumi inferiori agli 0,1 ml durante gli ultimi giorni in cui questofenomeno ha luogo.
In campo, l’acqua di guttazione fogliare può fornire comunque volumi d’acqua nonindifferenti, soprattutto se addizionata all’eventuale rugiada. Durante stagioni primaverili edestive secche, le gocce di guttazione provenienti da piante di mais possono costituire unafonte sicura d’acqua per gli insetti che ne richiedano elevate quantità per il loro metabolismo,come le api. L’utilizzo diretto di acqua di guttazione fogliare da parte di api è statogià verificato in letteratura ed è maggiormente verificabile in ambienti caratterizzati damonocolture di mais diffuse.
Le piante, se sono conciate o trattate con composti sistemici quali i neonicotinoidi,possono secernere gocce di guttazione contenenti concentrazioni estremamente elevate (anchea livelli di 350 mg/l) di principio attivo, molto più che sufficienti per uccidere un’apeche dovesse per necessità berle.
Poiché i neonicotinoidi sono dei composti sistemici che si distribuiscono moltovelocemente all’interno di tutti i tessuti della pianta attraverso l’apparato xilematico, essicontaminano a livelli di concentrazione più o meno consistenti anche il polline delle piante
trattate con questi pesticidi. La raccolta di questo polline da parte delle api e lasua conservazione all’interno delle arnie fa sì che l’azione tossica e la somministrazione diquesto polline contaminato continui nel tempo e possa portare alla morte le api anche inperiodi apparentemente slegati da quelli di infiorescenza delle piante trattate.
PERSISTENZA, DEGRADAZIONE E DESTINO AMBIENTALE
Data la loro bassissima volatilità, la loro presenza nell’ambiente si può riscontrare solo nei suoli, nelle acque enegli eventuali esseri viventi con cui vengono in contatto.
 Alcune delle caratteristiche di degradazione ambientale per questi principi attivi sono riportate in Tabella.
Alcune delle caratteristiche di degradazione ambientale per questi principi attivi sono riportate in Tabella.
Tabella: dati di degradazione dei principi attivi indagati e relativi coefficienti di ripartizione suolo/acqua espressi come μg di p.a. per grammo di carbone attivo
Come si può vedere la persistenza di questi principi attivi nell’ambiente è moderatamente lunga. Se si osserva in particolare la persistenza nel suolo, luogo in cui vengono solitamente posti i semi conciati con questi principi attivi, si vedono tempi di dimezzamento che vanno dal giorno e mezzo ai 545 giorni e, anche se le stime di alcuni
autori azzardano tempi di dimezzamento superiori ai 1000 giorni, la loro reale persistenza nell’ambiente può perdurare per più di due – tre anni a seconda dei tipi di terreno e della presenza di acqua, rimanendo così sempre disponibili per il prelievo da parte dell’apparato radicale delle piante.
Analisi sulle foglie di mais hanno verificato una persistenza dei principi attivi all’interno delle stesse in concentrazioni apprezzabili anche dopo 60 – 80 giorni dalla semina. I valori relativamente bassi della costante di assorbimento su carbone attivo fanno capirecome questi principi attivi abbiano una mobilità, una volta rilasciati nell’ambiente, sufficientemente elevata. Essendo infatti questi principi attivi molto o discretamente solubili in acqua, essi possono diffondere non solo nei terreni adiacenti ai campi seminati ma anche nei fiumi e persino nelle falde acquifere; esempi in tale senso sono stati registrati sia in Florida che a New York.
Una visione schematica della degradazione di uno di questi principi attivi (l’Imidacloprid) nel suolo e in acqua è riportata nelle figura: come estrapolabile a tutti gli xenobiotici noti, le intossicazioni acute/croniche possono essere biochimicamente rivelabili, in brevi tempi, eseguendo analisi sulle urine degli operatori esposti, sulla base degli specifici metaboliti terminali riferibili a composti noti.

Figura: Schema di degradazione dell’Imidacloprid in acqua. Con le frecce di spessore maggiore sono indicati i cammini più probabili.
Oltre ai cammini degradativi di tipo chimico e fisico vi sono da considerare quelli di tipobiologico. Molti batteri comunemente presenti nei terreni e nelle acque sono in grado di biotrasformare questi composti in tempi relativamente brevi nei loro comuni metaboliti; questi, si è osservato, sono spesso più tossici per gli insetti dei principi attivi stessi. Studi sulle api, effettuati utilizzando Imidacloprid in bassi dosaggi, hanno poi portato a comprendere che le api, già dopo 20 minuti dall’assunzione, sono in grado di metabolizzare ben il 70% di questo principio attivo e sono i metaboliti prodotti da loro stesse a decretarne la morte. Alcuni tra i metaboliti più comuni per questi principi attivi insetticidi sono riportati in tabella.

Tabella: Metaboliti principali prodotti nel suolo a partire dai p.a. insetticidi indagati
LEGISLAZIONI RIGUARDANTI I NEONICOTINOIDI E ALTRI INSETTICIDI
A livello italiano il primo provvedimento preso per affrontare il problema della moria delle api è stato il Decreto Ministeriale del 17 settembre 2008, che disponeva la
sospensione all’autorizzazione alla vendita e d’impiego di sementi conciate con le sostanze attive insetticide, Thiamethoxam, Clothianidin, Imidacloprid, Acetamiprid e Thiaclopridin virtù di un possibile nesso di causa – effetto tra l’utilizzo di sementi di mais, colza, girasole e barbabietola da zucchero conciate con tali principi e la moria delle api. Successivamente, il D.M. del 26 gennaio 2009 del Ministero del Lavoro, della Salute edelle Politiche Sociali precisava i limiti temporali di questa sospensione, fissandoli al 20 settembre 2009.
In un secondo tempo, in considerazione delle particolari caratteristiche agronomiche e di confettatura del seme della barbabietola da zucchero, è stato emanato l’ulteriore Decreto Ministeriale 27 gennaio 2009 che revocava la sospensione dell’autorizzazione d’impiego per la concia di sementi di barbabietola da zucchero, dei prodotti fitosanitari contenenti le sostanze attive citate, da sole o in miscela con altre sostanze attive e riammetteva quindi l’impiego di sementi di barbabietola da zucchero conciate con prodotti contenenti tali principi.
Ad un anno circa dalla prima sospensiva, con il Decreto dirigenziale del 14 settembre 2009, il Ministero del Lavoro, della Salute e delle Politiche Sociali ha prorogato fino al 20 settembre 2010la sospensione d’impiego dei quattro principi attivi nella concia di sementi.
Infine, con un ulteriore provvedimento del 16 settembre 2010, lo stesso Ministero ha prorogato il termine della sospensione al 30 giugno 2011, legando questa proroga alla necessità di attendere la conclusione del progetto APENET, finanziato per valutare l’efficacia e gli effetti del decreto di sospensione dei neonicotinoidi nella concia delle
sementi di mais e fornire risposte alle problematiche legate ai fenomeni di mortalità e di spopolamento delle colonie di api.
Nel 2012 sono stati pubblicati due studi di alto profilo che hanno dimostrato che l’esposizione ai neonicotinoidi nel polline e nel nettare potrebbe avere gravi effetti sulla navigazione e la sopravvivenza individuale (Henry et al., 2012 ) e sullo sviluppo delle colonie e della regina (Whitehorn et al.,2012 ). In risposta al crescente corpo di lavoro, l’Autorità Europea per la Sicurezza Alimentare (EFSA), l’organismo con supervisione regolamentare per i prodotti chimici agricoli, è stato incaricato di produrre una valutazione del rischio sui tre neonicotinoidi agricoli più ampiamente usati (clothianidin, imidacloprid e thiamethoxam) e il rischio che hanno posto alle api (EFSA 2013a , b , c ). Sulla base degli elementi disponibili, l’EFSA ha raccomandato una moratoria sull’uso dei neonicotinoidi sulle colture trattate, che è stata accettata e attuata dalla Commissione dell’Unione Europea (UE) alla fine del 2013 (Regolamento di esecuzione (UE) n. 485/2013 della Commissione del 24 maggio 2013 e che vieta l’uso e la vendita di sementi conciate con prodotti fitosanitari contenenti tali sostanze attive).
Questa moratoria è attualmente oggetto di una nuova valutazione. Uno degli obiettivi specificati era consentire ulteriori ricerche sull’impatto dei neonicotinoidi sulle api al fine di informare le successive decisioni normative. Dal 2013 è stato pubblicato un gran numero di studi che prendono in considerazione l’impatto dei neonicotinoidi sulle api e anche una vasta gamma di altri taxa non bersaglio. Utilizzando i dati di Web of Science, gli studi sui neonicotinoidi pubblicati negli anni 2013-2016 rappresentano il 52,4% di tutti i documenti su neonicotinoidi dal 1995. La proporzione è ancora maggiore per studi più
specializzati, come neonicotinoidi e api ( neonicotinoide * + ape *, 59,4%), neonicotinoidi e residui (neonicotinoidi * + residui, 60,9%), neonicotinoidi e acqua (neonicotinoidi * + acqua, 61,7%) e neonicotinoidi e terreno (neonicotinoidi * + suolo, 63,7%). Sono state pubblicate anche molte recensioni sull’impatto dei neonicotinoidi su organismi non bersaglio, ad esempio Nuyttens et al. ( 2013 ) sulla polvere contaminata da neonicotinoidi, Godfray et al. ( 2014 , 2015 ) sui rischi che i neonicotinoidi pongono agli impollinatori, Bonmatin et al. ( 2015 ) sul destino ambientale e l’esposizione ai neonicotinoidi, Pisa et al. ( 2015 ) e Gibbons et al. ( 2015 ) sugli impatti dei neonicotinoidi sugli organismi terrestri non bersaglio e Morrissey et al. ( 2015 ) sulla contaminazione degli ecosistemi acquatici con i neonicotinoidi e il loro impatto sugli organismi acquatici.
Lo scopo di questa revisione è di considerare le prove scientifiche pubblicate dal 2013 che
coprono l’impatto dei neonicotinoidi su organismi selvatici non bersaglio (quindi escludendo l’ape domestica) e di riunirli in un unico luogo per aiutare il processo decisionale informato. Non si tratta di una valutazione formale del rischio, anche se si effettueranno confronti con la base di conoscenze utilizzata nelle valutazioni del rischio dell’EFSA in modo specifico e ciò che era noto nel 2013 più in generale. I risultati saranno di interesse per coloro che considerano l’impatto più ampio del consumo di pesticidi neonicotinoidi nel valutare il loro uso futuro in ambienti agricoli.
TOSSICITÀ ACUTA E CRONICA DEI PESTICIDI, con particolare
riguado verso i Neonicoinoidi
“Tutte le sostanze sono tossiche, solola dose le rende non tossiche”. Questo affermò nel 1538 TheophrastusPhilippusAureolusBombastus von Hohenheim(1493 -1541), meglio noto come Paracelso. A questa frase si fa risalire la nascita della moderna tossicologia, ed esprime un concetto fondamentale: ovvero che gli organismi sono in grado di gestire senza soffrire di effetti tossici (o avversi), la presenza di sostanze, purché non sia superata una certa quantità (dose). Su questo principio si basa la possibilità di stabilire le condizioni che ci permettono di accettare la presenza di elementi “estranei”negli alimenti. Ovvero, una volta valutatele caratteristiche tossicologiche dellasostanza, determiniamo la quantità (dose) che non causa effetti tossici o avversi osservabili, e quindi definiamo accettabile l’esposizione che è inferiore a questa quantità senza effetti. Il processo con il quale si giunge alla definizione della dose che riteniamo accettabile è definito valutazione del rischio. Nel caso dei pesticidi, si tratta di raccogliere tutte le informazioni tossicologiche e sui residui negli alimenti e confrontare i risultati.
La sicurezza alimentare non dipende dalla totale assenza di contaminanti ma dalla loro concentrazione nei prodotti e pertanto dalla dose di assunzione. Quindi per il rischio chimico come per quello biologico risulta corretto parlare di valori di accettabilità piuttosto che di rischio zero.
Il manifestarsi di un effetto tossico e la sua intensità dipendono dalla “esposizione” alla sostanza tossica:
- per esposizione si intende: la quantità di una sostanza che viene a contatto con
l’organismo per un determinato periodo di tempo;
- vie di esposizione per l’uomo sono: l’inalazione, l’ingestione e il contatto con la pelle;
Gli effetti tossici possono variare sensibilmente in relazione alle diverse vie di esposizione:
- le sostanze tossiche assorbite attraverso i polmoni o attraverso la pelle
raggiungono rapidamente il circolo sanguigno e con esso i vari organi del corpo umano;
- le sostanze tossiche assorbite per ingestione raggiungono il circolo sanguigno soltanto dopo essere state trasformate (detossificate) dal fegato;
- una volta assorbite le sostanze possono trasformarsi all’interno dell’organismo e formare sostanze chimiche diverse da quelle di partenza (metaboliti);
- alcune sostanze ed i loro metaboliti possono anche accumularsi nei singoli tessuti (principalmente grasso, ma anche tessuto osseo);
- gli effetti tossici si manifestano quando la dose assorbita dall’organismo supera la “soglia di effetto” ;
- “l’effetto tossico” si può manifestare a seguito di una singola esposizione (generalmente a dosi elevate) o di esposizioni prolungate nel tempo (basse dosi ripetute nel tempo e non tossiche singolarmente) .
In merito alla tossicità dei neonicotinoidi per l’uomo, L’EFSA ha elaborato il suo parere scientifico, come discusso nel paragrafo 3.7, su richiesta della Commissione Europea, prendendo in considerazione le recenti ricerche di Kimura-Kuroda(Kimura-Kuroda J et al. Nicotine-like effects of the neonicotinoid insecticides acetamiprid and imidacloprid on cerebellar neurons from neonatal rats. PloS ONE 7 (2), 2012),sul potenziale di Acetamiprid e Imidacloprid di danneggiare il sistema nervoso umano nella fase di sviluppo, il cervello in particolare.
A titolo esemplificativo, di seguito vengono riportati alcuni dati sperimentali condotti sia
su colture cellulari sia su colture cellulari, che su modelli animali, nonché centri antiveleni.
- Kim J. et al. Imidacloprid, a neonicotinoidinsecticide, inducesinsulinresistance. The J of ToxicologicalSciences. 38, 655-60, (2013). Da test condotti su colture cellulari esposte a imidacloprid per
individuare le cause di incremento di incidenza del diabete di tipo 2, è emerso che sussiste una
correlazione
tra uso di neonicotinoidi e alterata omeostasi del glucosio.
- Green T. Thiametoxam induced mouse liver tumors and their relevance to humans. Toxicol Sci.86,36- 47, (2005).
(studi di tossicità cronica, esposizione a dosi 500-2500
TMX (thiametoxam) induce tumori epatici in topi
ppm per 18 mesi)
- Forrester NB. Neonicotinoid insecticide exposures reported to six poison centers in Texas. Human &
Experimental Toxicology.33, 568-73, (2014) (OK , ma non in grassetto)
Abstract
“Neonicotinoids are a relatively newer class of insecticide. Used primarily in agriculture, neonicotinoids are also used for flea control in domestic animals. Information on human exposures to neonicotinoids is limited. Neonicotinoidexposuresreported to Texaspoisoncenters during 2000-2012 were identified and the distribution by selected factors examined. Of 1,142 total exposures, most products contained imidacloprid (77%) or dinotefuran (17%). The exposures were seasonal with half reported during May-August. The most common routes of exposure were ingestion (51%), dermal (44%), and ocular (11%). The distribution by patient age was 5 years or less (28%), 6-19 years (9%), 20 years or more (61%), and unknown (2%); and 64% of the patients were female. Of all, 97% of the exposures were unintentional and 97% occurred at the patient’s own residence. The management site was on-site (92%), already at/en route to a health care facility (6%), and referred to a health care facility (2%). The medical outcomes included no effect (22%), minor effect (11%), moderate effect (1%), not followed judged nontoxic (14%), not followed minimal effects (46%), unable to follow potentially toxic (1%), and unrelated effect (4%). The most commonly reported adverse
clinical effects were
ocular irritation (6%), dermal irritation (5%), nausea (3%), vomiting (2%), oral irritation
The most frequently reported treatments were dilution/wash (85%)
(2%), erythema (2%), and red eye (2%).
and food (6%). In summary, these data suggest that the majority of neonicotinoidexposuresreported to the poisoncenters may be managed outside of health care facilities with few clinical effects expected.”…
- Han M et al. Human exposure to neonicotinoid insecticides and the evaluation of their potential
toxicity: An overview, Chemosphere. 192:59-65, (2018)
Abstract
Neonicotinoid insecticides have become the fastest growing class of insecticides over the past few decades. The insecticidal
activity of neonicotinoids is attributed to their agonist action on nicotinic acetylcholine receptors (nAChRs). Because of the
special selective action on nAChRs in central nervous system of insects, and versatility in application methods, neonicotinoids
are used to protect crops and pets from insect attacks globally. Although neonicotinoids are considered low toxicity to
mammals and humans in comparison with traditional insecticides, more and more studies show exposure to neonicotinoids
pose potential risk to mammals and even humans. In recent years, neonicotinoids and their metabolites have been successfully
detected in various human biological samples. Meanwhile, many studies have focused on the health effects of neonicotinoids
on humans. Our aims here are to review studies on human neonicotinoid exposure levels, health effect, evaluation of potential
toxicity and to suggest possible directions for future research.
- Wood T.J et al. The environmental risks of neonicotinoid pesticides: a review of the evidence post
2013. Environ Sci Pollut Res Int. 24(21):17285-17325, (2017
Abstract
Neonicotinoid pesticides were first introduced in the mid-1990s, and since then, their use has grown
rapidly. They are now the most widely used class of insecticides in the world, with the majority of
applications coming from seed dressings. Neonicotinoids are water-soluble, and so can be taken up by a
developing plant and can be found inside vascular tissues and foliage, providing protection against
herbivorous insects. However, only approximately 5% of the neonicotinoid active ingredient is taken up
by crop plants and most instead disperses into the wider environment. Since the mid-2000s, several studies
raised concerns that neonicotinoids may be having a negative effect on non-target organisms, in particular
on honeybees and bumblebees. In response to these studies, the European Food Safety Authority (EFSA)
was commissioned to produce risk assessments for the use of clothianidin, imidacloprid and thiamethoxam
and their impact on bees. These risk assessments concluded that the use of these compounds on certain
flowering crops poses a high risk to bees. On the basis of these findings, the European Union adopted a
partial ban on these substances in May 2013. The purpose of the present paper is to collate and summarise
scientific evidence published since 2013 that investigates the impact of neonicotinoids on non-target
organisms. Whilst much of the recent work has focused on the impact of neonicotinoids on bees, a growing
body of evidence demonstrates that persistent, low levels of neonicotinoids can have negative impacts on
a wide range of free-living organisms.
(sottolineato e in rosso)
Il 27 aprile
UE
si è pronunciata a favore della messa
2018 l’
bando
di 3 neonicotinoidi, Imidacloprid, Clothianidin e Tiamethoxam, limitandone
al
l’utilizzo esclusivo nelle serre. Detto bando estende quello parziale già in essere dal 2013
a cura della EFSA.
La tossicità, caratteristica di ciascuna sostanza chimica, viene stimata attraverso studi sperimentali condotti su animali, utilizzando la cosiddetta “relazione dose-risposta” che descrive l’intensità degli effetti biologici di una sostanza in funzione della dose a cui sono esposti gli animali di laboratorio. Lo scopo di questi studi è quello di determinare:
- la tossicità acuta di una sostanza o “Dose Letale 50” (DL50) : che rappresenta la
quantità di una sostanza, per unità di peso corporeo, capace di provocare la morte del 50% degli individui della popolazione sperimentale nei test di tossicità in laboratorio;
- la tossicità cronica o NOAEL (No ObservedAdverseEffectLevel) ossia la dose che
non provoca effetti avversi osservabili sugli animali sottoposti ai test di laboratorio.
DOSI SOGLIA DI ESPOSIZIONE PER L’UOMO
Le dosi soglia di esposizione per l’uomo esprimono la quantità massima di sostanza, per unità di peso corporeo, al di sotto della quale non ci si attende che una esposizione
provochi effetti tossici. Tali soglie vengono definite a partire dai valori di NOAEL ottenuti dalle sperimentazioni su specie animali. A tal fine i valori di NOAEL vengono divisi per un Fattore di Sicurezza che generalmente è pari a 100, in considerazione del fatto che esiste:
-
-
-
- una differenza tra gli animali e l’uomo relativamente ai: meccanismi di assorbimento, disponibilità, distribuzione, trasformazione e eliminazione delle sostanze tossiche (tossicocinetica); meccanismi chimici a livello cellulare con cui si verifica la tossicità (tossicodinamica);
- una variabilità nella popolazione umana in termini di differenze genetiche, di età, sesso, ambiente di vita, stili di vita (es. abitudini alimentari) e gruppi di individui con maggiore sensibilità (neonati, bambini, anziani, malati);
-
-
In tal modo i dati sperimentali ottenuti su animale, possono essere utilizzati per l’uomo con un elevato grado di “sicurezza”.
Le principali “soglie di esposizione per l’uomo” definite secondo questa procedura sono:
- ADI (AcceptableDailyIntake) o DGA (Dose Giornaliera Accettabile): quantità di sostanza, espressa in mg per kg di peso corporeo, che può essere assunta quotidianamente per l’intero arco di vita senza che si manifestino effetti tossici; Generalmente viene ricavata dividendo il NOAEL per un fattore di sicurezza pari a 100
- ARfD (Acute Reference Dose): quantità di sostanza, espressa in mg per kg di peso corporeo, che può essere assunta in un ristretto intervallo di tempo (es. un pranzo o un
giorno), senza che si manifestino effetti tossici. Generalmente l’ARfD viene ricavata dividendo il NOAEL per un fattore di sicurezza pari a 10;
- AOEL (AcceptableOperator ExposureLevel): quantità massima di sostanza, espressa in mg per kg di peso corporeo, alla quale un operatore agricolo può essere esposto giornalmente, senza che si manifestino effetti tossici. Generalmente l’AOEL viene ricavata dividendo il NOAEL per un fattore di sicurezza pari a 10 o a 100;
Le “soglie di esposizione” così definite rappresentano “soglie di tossicità” per l’uomo e vengono utilizzate nella valutazione del rischio per il consumatore (ADI e ARfD) e per l’operatore (AOEL).
VALUTAZIONE DEL RISCHIO CRONICO
Considera gli effetti a lungo termine e consiste nel caratterizzare il rischio derivato dall’ingestione di bassi livelli di residui di sostanze fitosanitarie presenti nella dieta per un periodo pari all’intero arco di vita. Tale valutazione viene effettuata a livello nazionale e comunitario.
Il calcolo del rischio cronico mette in rapporto una stima dell’esposizione, derivante dall’assunzione di residui con la dieta, e l’ADI, che rappresenta la quantità (dose) di una determinata sostanza che può essere assunta quotidianamente per l’intero arco di vita senza che si verifichino effetti tossici.
Se il valore dell’esposizione supera il valore dell’ADI allora si è in presenza di un rischio non accettabile.
La stima dell’assunzione di residui di sostanze fitosanitarie (esposizione) si basa sul calcolo della TMDI (TheoreticalMaximum DailyIntake) o Massima Assunzione
Quotidiana Teorica, che stima l’assunzione di una sostanza fitosanitaria considerando la dieta e una presenza di residuo nelle diverse componenti di origine agricola pari al valore del Limite Massimo di Residuo (LMR).
Una valutazione più realistica dell’esposizione attraverso la dieta può essere basata considerando la IEDI (International EstimatedDailyIntake) o Massima Assunzione Quotidiana che tiene conto dei residui presenti nella sola porzione edibile e degli effetti di processo e di cottura sui livelli di residuo.
LA VALUTAZIONE DEL RISCHIO ACUTO
Considera gli effetti di un’esposizione a residui di “sostanze attive con elevata tossicità acuta” durante un pasto o una giornata, in quanto si ritiene che:
- il consumo di un particolare alimento in una singola assunzione può essere molto più elevato rispetto al consumo medio;
- una particolare porzione di alimento può contenere un residuo più alto del valore medio. Il livello di residuo in una singola unità di un frutto o di un ortaggio può essere più alto di un determinato fattore (definito come fattore di variabilità) rispetto al residuo medio del campione analizzato a cui quella unità appartiene;
La variabilità della quantità di residuo sul singolo prodotto vegetale dipende dalla disomogenea distribuzione del prodotto fitosanitario durante il trattamento.
Il calcolo del rischio acuto mette in rapporto la stima dell’assunzione di residui in un singolo pasto, con l’ARfD che rappresenta la quantità (dose) di una determinata sostanza
che può essere assunta in un ristretto intervallo di tempo senza che si verifichino effetti tossici.
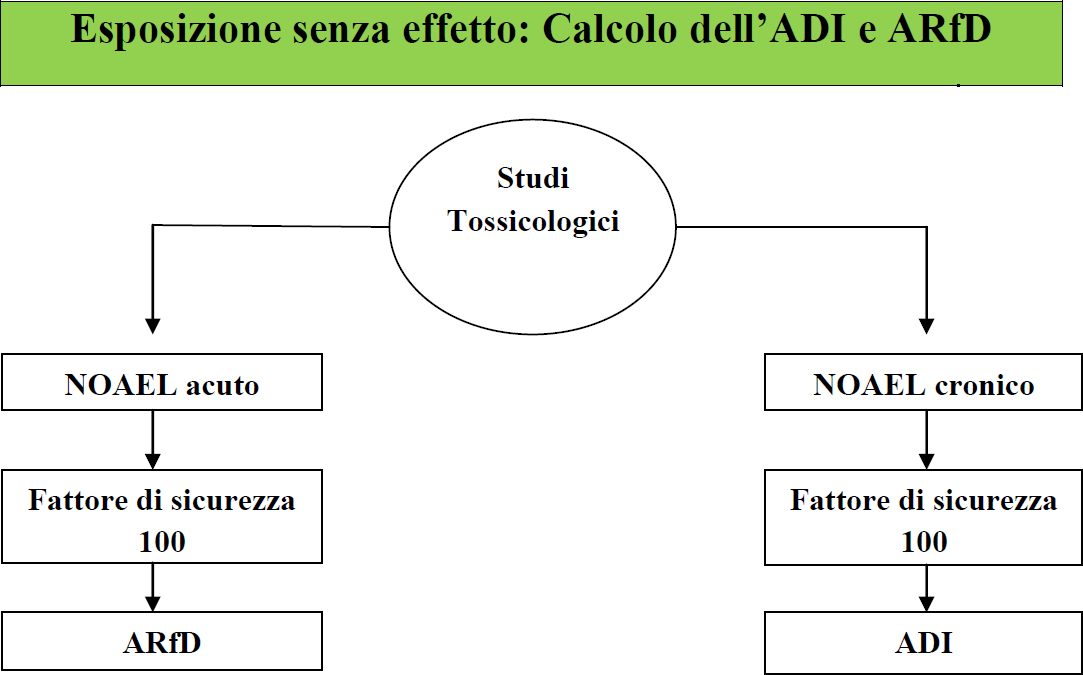 Se il valore dell’esposizione supera il valore dell’ARfD allora si è in presenza di un rischio non accettabile.
Se il valore dell’esposizione supera il valore dell’ARfD allora si è in presenza di un rischio non accettabile.
VALUTAZIONE DEL RISCHIO PER IL CONSUMATORE
La valutazione del rischio per il consumatore mette in rapporto i valori dell’ADI per il rischio cronico e dell’ARfD per il rischio acuto con la quantità di sostanza attiva presente come residuo negli alimenti e ingerita durante i pasti (esposizione). Relativamente all’entità dell’esposizione, essa è correlata alle abitudini alimentari degli individui, all’età e al peso corporeo. Per procedere ad una corretta valutazione dell’esposizione è
necessario avere a disposizione dati sulla dieta di questi gruppi di popolazione.
IL FATTORE DI SICUREZZA PER LA DEFINIZIONE DELLE SOGLIE DI ESPOSIZIONE PER L’UOMO
Il “Fattore di sicurezza” tiene conto del trasferimento da animale all’ uomo dei risultati dei test su animale (variabilità interspecifica) e della variabilità tra la popolazione umana (variabilità intraspecifica).
Normalmente esso è pari a 100. In questo caso , se si definisce sperimentalmente un valore di NOAEL pari a 1mg/kg di peso corporeo, il corrispondente valore soglia di esposizione per l’uomo sarà pari a 1/100 ossia 0,01 mg/kg di peso corporeo, ossia il valore del NOAEL ricavato sperimentalmente viene diminuito di 100 volte. Questo significa che, sulla base dello studio svolto su animale, ci si aspetta un potenziale effetto tossico per l’uomo ad una dose di esposizione superiore a 0,01 mg/kg di peso corporeo.
In alcuni casi il “Fattore di sicurezza” può essere anche superiore a 100 per tenere conto di ulteriori incertezze sul dato ricavato da particolari test o inferiore a 100 perché ci si riferisce, ad esempio, ad un ristretto gruppo di popolazione (esposizione degli operatori agricoli).
3.9PRINCIPALI STUDI TOSSICOLOGICI PER LA VALUTAZIONE DELL’IMPATTO SULLA SALUTE RICHIESTI NEL PROCESSO DI AUTORIZZAZIONE DI UN PRODOTTO FITOSANITARIO
Gli studi sono condotti su specie animali ed hanno l’obiettivo di caratterizzare la classe di tossicità del prodotto fitosanitario (o della sostanza attiva). Ne determinano quindi le caratteristiche tossicologiche intrinseche.
Si tratta di studi di:
- tossicocinetica : processi di assorbimento, distribuzione, metabolismo, escrezione della sostanza tossica (ADME).
- tossicità acuta su ratto: DL50 orale, inalatoria, cutanea;
- irritazione cutanea ed oculare su coniglio;
- sensibilizzazione su topi e cavie;
- genotossicità: presenza e tipo di interazioni con il patrimonio genetico (con test in vitro e in vivo)
- tossicità cronica e cancerogenesi su ratto (della durata di 2 anni) e su topo (della durata di 18 mesi) che consentono la determinazione del NOAEL;
- tossicità a breve termine su ratto e topo (della durata di 28 giorni o 90 giorni) e su cane (della durata di 1 anno) che consentono la determinazione del NOAEL;
Ad esempio un prodotto (o una sostanza attiva) viene classificato R27 (Molto tossico a contatto con la pelle) se lo studio di tossicità acuta per via cutanea su ratto o coniglio ha prodotto una DL50 minore o uguale a 50 mg/kg (ossia milligrammi di sostanza per kg di peso dell’animale testato).
CAPITOLO 4.SICUREZZA ALIMENTARE E CONTROLLI UFFICIALI
Il controllo ufficiale sui residui di prodotti fitosanitari negli alimenti rappresenta una delle priorità sanitarie più rilevanti nell’ambito della sicurezza alimentare, ed ha la finalità di garantire un livello elevato di protezione del consumatore.
In Italia i programmi di controllo sui prodotti alimentari e che comprendono anche i piani annuali di controllo in materia di residui di prodotti fitosanitari negli alimenti, vengono elaborati dalla Direzione Generale per l’Igiene e la Sicurezza degli Alimenti e la Nutrizione (D.G.I.S.A.N.) del Ministero della Salute.
Parte dei controlli che vengono effettuati a livello nazionale, vanno ad interessare un Programma coordinato di controllo ufficiale previsto dall’Unione Europea su alimenti di produzione interna e di importazione che mira a conoscere l’effettiva presenza dei livelli massimi consentiti di residui nelle derrate alimentari.
Al fine di definire tale programmazione, si fa riferimento al Decreto Ministeriale del 23 Dicembre 1992, (DM. 23/12/92) al Regolamento CE 882/04 relativo ai controlli ufficiali e al Reg. CE n.396/2005 che riguarda la fissazione dei livelli massimi di residui sui prodotti alimentari.
Il Decreto Ministeriale del 23/12/92 prevede un programma dettagliato di attuazione dei
controlli in ambito delle Regioni e delle Province autonome, con l ’indicazione tra l’altro
del numero minimo e del tipo di campioni da analizzare. La ripartizione dei campioni
per ogni Regione e Provincia autonoma è calcolata in base ai dati sul consumo e sulla produzione degli alimenti interessati.
Il Regolamento CE 882/2004 fissa invece criteri generali per l’effettuazione dei controlli
ufficiali per la verifica della conformità alla normativa, stabilendo le caratteristiche
che devono possedere i Laboratori per il controllo ufficiale, le procedure, le attività, i
metodi e le tecniche per effettuare i controlli. Al fine di dare attuazione inoltre al campionamento previsto dal piano coordinato comunitario di cui al Regolamento UE 2016/662, destinato a garantire il rispetto dei livelli massimi di residui di antiparassitari e a valutare l’esposizione dei consumatori ai residui di antiparassitari nei e sui prodotti alimentari di origine vegetale e animale, la DGISAN ha emanato degli indirizzi operativi che stabiliscono il numero di campioni da prelevare per le tipologie di alimenti previste da tale regolamento, le modalità di prelievo, le modalità di raccolta dei risultati dei controlli.
Le analisi per la ricerca di residui di prodotti fitosanitari vengono effettuate dai
Laboratori
del controllo ufficiale (Agenzie Regionali per la Protezione dell’Ambiente (A.R.P.A.),
Laboratori di Sanità Pubblica (L.S.P.) e Istituti Zooprofilattici Sperimentali (I.Z.S.). Ai sensi del Regolamento CE 882/2004 sono stati istituiti i Laboratori nazionali di riferimento che coordinano i Laboratori e sono a loro volta coordinati dai Laboratori comunitari di riferimento. I Laboratori devono essere accreditati, devono partecipare ai “proficiency test”, devono trasmettere i risultati delle analisi al Ministero e i metodi di analisi da loro utilizzati devono essere almeno validati.
I dati del controllo ufficiale sono utilizzati anche dall’ Istituto Superiore di Sanità per
ricavare una stima dell’assunzione giornaliera dei residui di prodotti fitosanitari con la
dieta, al fine di raggiungere i seguenti obiettivi:
- Valutare, in relazione all’esito delle analisi effettuate, il rischio per la salute
pubblica derivante dal grado di contaminazione dei prodotti alimentari;
- Conoscere puntualmente l’andamento dei controlli sui residui di prodotti fitosanitari negli alimenti di origine vegetale svolti in Italia da tutte le Amministrazioni Sanitarie Centrali e Territoriali.
La natura di questo rapporto riepilogativo fornisce un quadro sia generale che di dettaglio sui risultati conseguiti e fornisce indicazioni sulle azioni future da intraprendere ad ogni livello istituzionale per migliorare e rafforzare ulteriormente il sistema di controllo ufficiale nazionale sui residui dei prodotti fitosanitari, per assicurare adeguati livelli di sicurezza alimentare.
ORGANISMI CENTRALI E TERRITORIALI DEL SISTEMA DEI CONTROLLI PER LA SICUREZZA ALIMENTARE
Il Ministero della Salute opera a livello centrale con la D.G.I.S.A.N. e, a livello territoriale, con i propri Uffici di Sanità Marittima, Aerea e di Frontiera (U.S.M.A.F.), per i controlli all’importazione sui prodotti alimentari di origine vegetale e con i Posti d’ispezione frontaliera (P.I.F) per i controlli all’importazione degli alimenti di origine animale.
Il Comando Carabinieri per la Tutela della Salute, attraverso i Nuclei Antisofisticazione e Sanità (N.A.S.), coordinati dal Ministro della Salute, esercita azioni di controllo a fini repressivi su tutto il territorio nazionale e con strutture articolate anche a livello periferico.
A livello territoriale per l’attività di controllo ufficiale dei prodotti alimentari operano le Regioni e le Province Autonome di Trento e Bolzano, con gli Assessorati alla Sanità e le A.S.L., con i rispettivi Servizi dei Dipartimenti di Prevenzione.
Le attività di controllo analitico sugli alimenti e sulle bevande sono espletate dai
Laboratori di controllo ufficiale (A.R.P.A; L.S.P. e I.Z.S.) mentre l’Istituto Superiore di
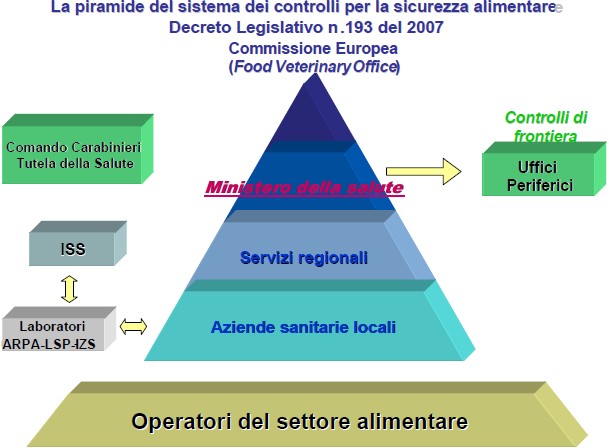 Sanità (I.S.S.), che li coordina, opera sia per l’effettuazione delle analisi di revisione sugli alimenti e le bevande che per una serie di compiti tecnico-scientifici tra i quali anche l’organizzazione di proficiency test di cui ogni anno rende noti gli esiti.
Sanità (I.S.S.), che li coordina, opera sia per l’effettuazione delle analisi di revisione sugli alimenti e le bevande che per una serie di compiti tecnico-scientifici tra i quali anche l’organizzazione di proficiency test di cui ogni anno rende noti gli esiti.
D.M. 23 DICEMBRE 1992 – PROGRAMMAZIONE NAZIONALE DEL CONTROLLO UFFICIALE DEI RESIDUI DI PRODOTTI FITOSANITARI NEGLI ALIMENTI
Il Decreto del Ministro della Sanità del 23 dicembre 1992, relativa ai limiti massimi di residui di sostanze attive nei presidi sanitari tollerate su e nei prodotti alimentari, ha fornito dei requisiti minimi alle Regioni e alle Province Autonome di Trento e Bolzano per la programmazione dei controlli sui residui di sostanze attive da parte delle A.S.L.Il
Decreto contiene delle tabelle riportanti il numero di campioni da prelevarsi in
ogniRegione o Provincia Autonoma per le seguenti matrici alimentari: ortaggi, frutta,
cereali, vino, oli, carni, latte e derivati, uova, prodotti ittici.
Sono distinti in tabelle separate i campioni da prelevare per gli alimenti prodotti nell’ambito della Regione o Provincia Autonoma e quelli per gli alimenti provenienti dal di fuori della Regione o Provincia autonoma di riferimento.
Gli Assessorati delle Regioni o delle Province Autonome si avvalgono dei Dipartimenti
di Prevenzione delle A.S.L. per il prelievo dei campioni alimentari, che vengono
analizzati daiLaboratori (A.R.P.A., LSP, I.Z.S.). Questi ultimi provvedono ad inviare i
risultati sui residui dei prodotti fitosanitari, direttamente e via web, al Ministero –
D.G.I.S.A.N.
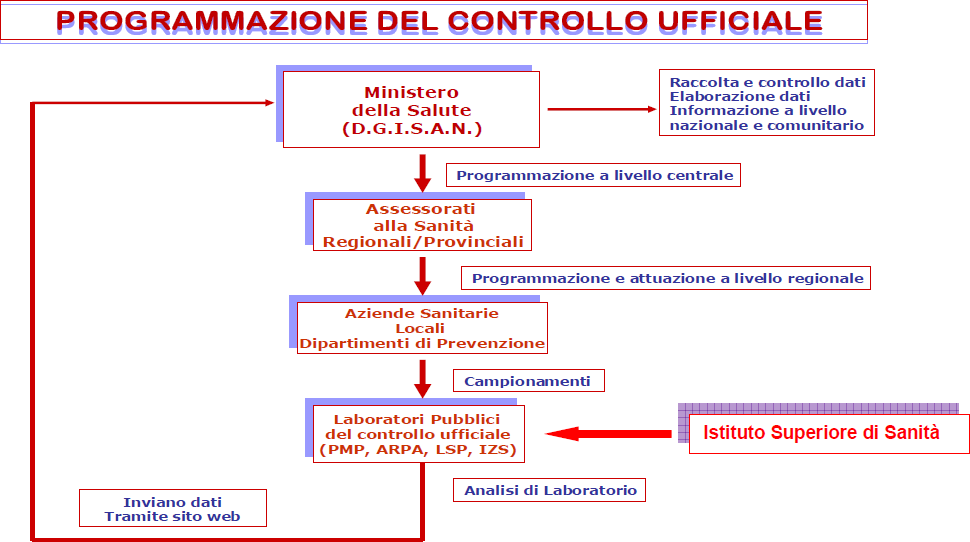
La programmazione regionale viene effettuata tenendo conto del valore minimo indicato dal Decreto e dei dati del consumo e produzione di frutta, ortaggi, cereali, olio e vino. In particolare si definiscono il dettaglio del numero di campioni attesi per Regione o Provincia autonoma, ed i Laboratori che devono inviare i dati via web sulle analisi per la ricerca di residui di prodotti fitosanitari.
Oltre alle tipologie previste dal Decreto Ministeriale le Regioni e Province autonome di Trento e Bolzano programmano anche i campionamenti per i baby food e per gli altri prodotti che sono alimenti trasformati o alimenti non contenuti nelle classi previste dal decreto.
Per i prodotti alimentari di origine vegetale i punti di prelievo consigliati sono:
i centri di raccolta aziendale e cooperativi per i prodotti provenienti dall’interno della Regione o Provincia autonoma, i mercati generali specializzati, quelli non specializzati, i
depositi all’ingrosso, gli ipermercati e i supermercati per i prodotti provenienti dal di fuori della Regione o della Provincia autonoma.
IL REGOLAMENTO (CE) 396/2005 – PROGRAMMA COORDINATO COMUNITARIO PLURIENNALE.
Il Regolamento (CE) 396/2005 e successive modificazioni ed integrazioni, fissa gli LMR
(Livelli Massimi di Residuo) dei fitosanitari in o sui prodotti alimentari e mangimi di
origine vegetale e animale. Gli LMR sono armonizzati su tutto il territorio europeo e permettono la libera circolazione delle merci, fornendo nel contempo un’elevata garanzia della salubrità, per quanto riguarda i residui di pesticidi, degli alimenti circolanti sul territorio europeo. In particolare, nel Regolamento è indicata, per ciascuna sostanza attiva e per ciascun alimento, la massima concentrazione ammissibile della molecola espressa in mg di sostanza attiva per kg di alimento ovvero parti per milione (ppm).L’art. 26 del citato Regolamento (CE) 396/2005 stabilisce che gli Stati Membri devono effettuare controlli ufficiali sui residui di fitofarmaci negli alimenti e nei mangimi. Tali controlli consistono nel prelevare campioni alimentari, individuare l’eventuale presenza di fitofarmaci e quantificare i livelli di concentrazione (residui), verificare il rispetto degli LMR in vigore.
Il successivo art. 27 specifica che ciascuno Stato Membro debba prelevare un numero e una serie sufficiente di campioni, affinché i risultati ottenuti siano rappresentativi del mercato, tenendo conto dei risultati dei precedenti programmi di controllo. Tale prelievo
di campioni deve essere effettuato il più vicino possibile al luogo di distribuzione, per consentire di adottare qualsiasi conseguente misura esecutiva.
L’art. 29 del citato Regolamento (CE) 396/2005 stabilisce un Programma coordinato comunitario pluriennale che specifica quali e quanti campioni debbano essere analizzati da ciascuno Stato Membro in attuazione di programmi nazionali di controllo, i cui dettagli sono specificati nel successivo art. 30.
In particolare nel Programma Nazionale di Controllo devono essere almeno indicati i seguenti elementi:
-
-
- i prodotti da sottoporre a campionamento;
- il numero di campioni da prelevare e di analisi da effettuare;
- gli antiparassitari da analizzare;
- i criteri applicati ai fini dell’elaborazione dei programmi, tra cui, in particolare:
-
- le combinazioni antiparassitario/prodotto da selezionare;
- il numero di campioni prelevati, rispettivamente, per i prodotti della produzione nazionali e per quelli esteri;
- il consumo dei prodotti, rispetto alla dieta alimentare nazionale;
- il programma di controllo comunitario;
- i risultati dei precedenti programmi di controllo.
Il Programma Coordinato Comunitario pluriennale è adottato e aggiornato ogni anno per tener conto di eventuali criticità, riscontrate nel corso degli anni precedenti, relative all’osservanza degli LMR.
L’attuazione del citato Programma Comunitario avviene annualmente attraverso la pubblicazione di specifici regolamenti che stabiliscono i prodotti alimentari da sottoporre alcontrollo ufficiale.
Il Programma Coordinato Comunitario pluriennale è attuato, per il triennio 2016-2019, dal Regolamento (UE) 662/2016, che prevede l’analisi di circa 200 pesticidi su matrici di origine vegetale e di circa 70 su matrici di origine animale. Il numero totale delle molecole
da analizzare, tenendo conto del fatto che per numerosi pesticidi è richiesta l’analisi di
molteplici molecole (sostanza attiva, suoi isomeri ed eventuali metaboliti), diventano di
fatto circa 350.
Si definiscono isomeri due molecole che differiscono fra di loro per la disposizione
spaziale degli atomi costituenti. Ad esempio gli isomeri del DDT (o,p’ DDT e p,p’ DDT) differiscono per la posizione degli atomi di cloro sugli anelli benzenici (Figura 1).
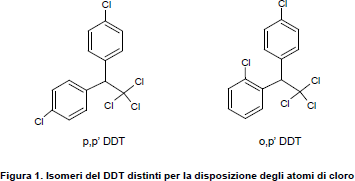
Si definisce metabolita una molecola derivante dal pesticida genitore (parent) a causa di
reazioni (spesso di ossidazione) dovute al metabolismo oppure all’azione di agenti fisici naturali (calore, luce, acqua ecc.).
Ad esempio il p,p’ DDE è un prodotto del metabolismo del p,p’ DDT (Figura 2)
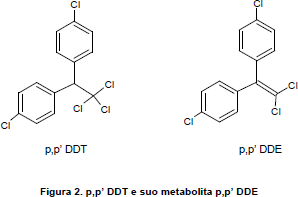
Spesso i metaboliti hanno rilevanza tossicologica simile o maggiore del parent da cui derivano. L’allegato I del Regolamento (UE) 662/2016 riporta le combinazioni di pesticida/prodotto alimentare da controllare nei/sui prodotti di origine vegetale (Parte A) e nei/sui prodotti di origine animale (Parte B) e le combinazioni di antiparassitario/prodotto da monitorare nei/sui prodotti di origine vegetale (Parte C).
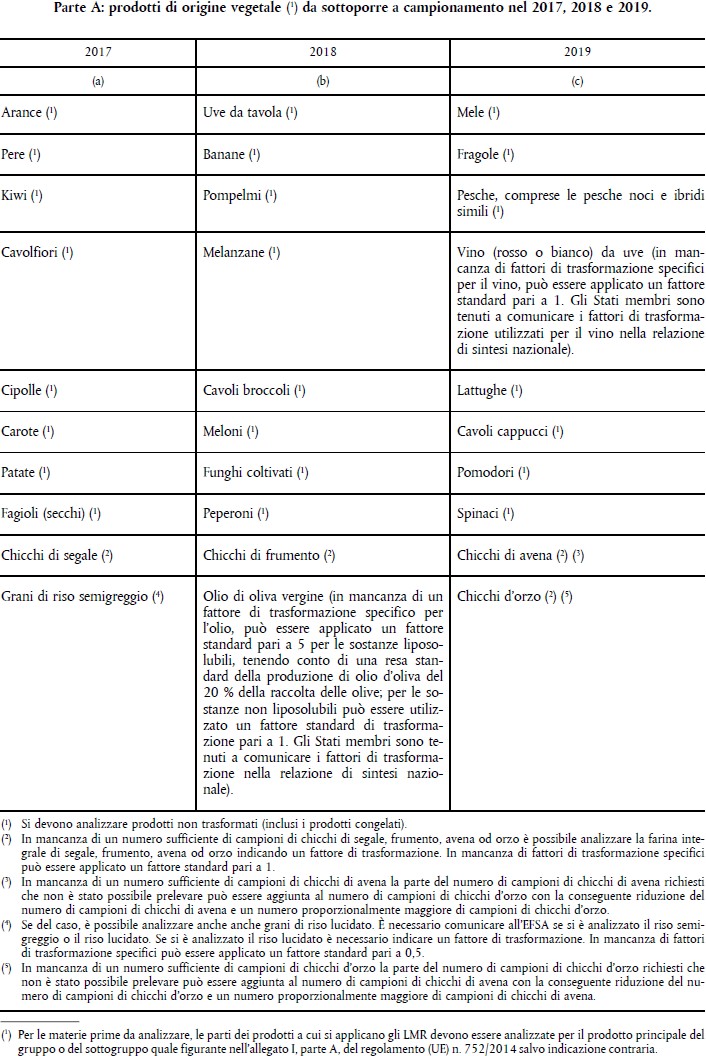
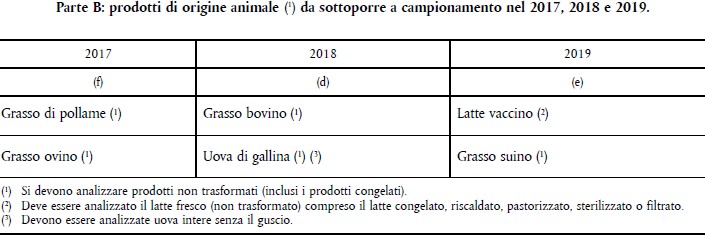
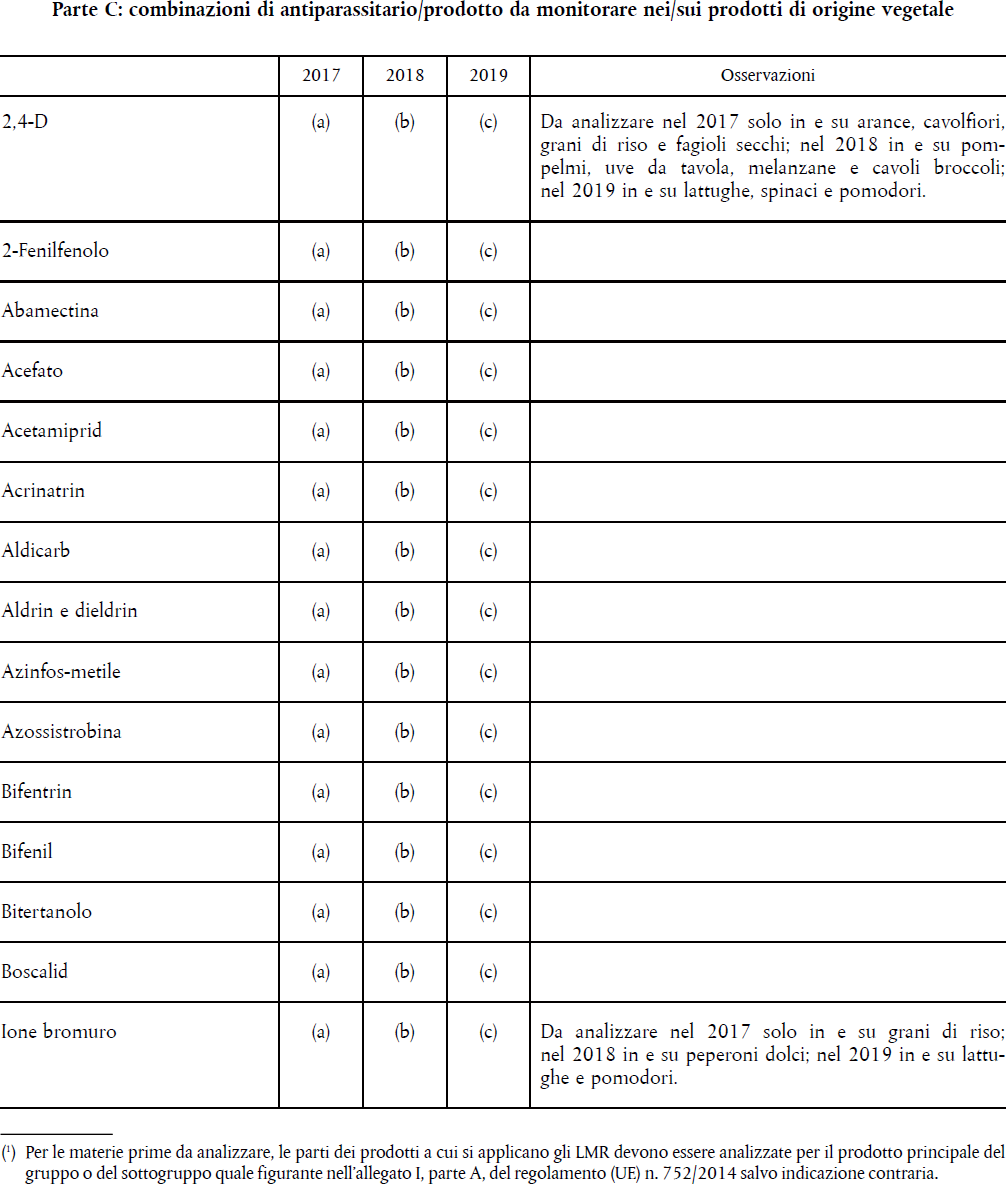
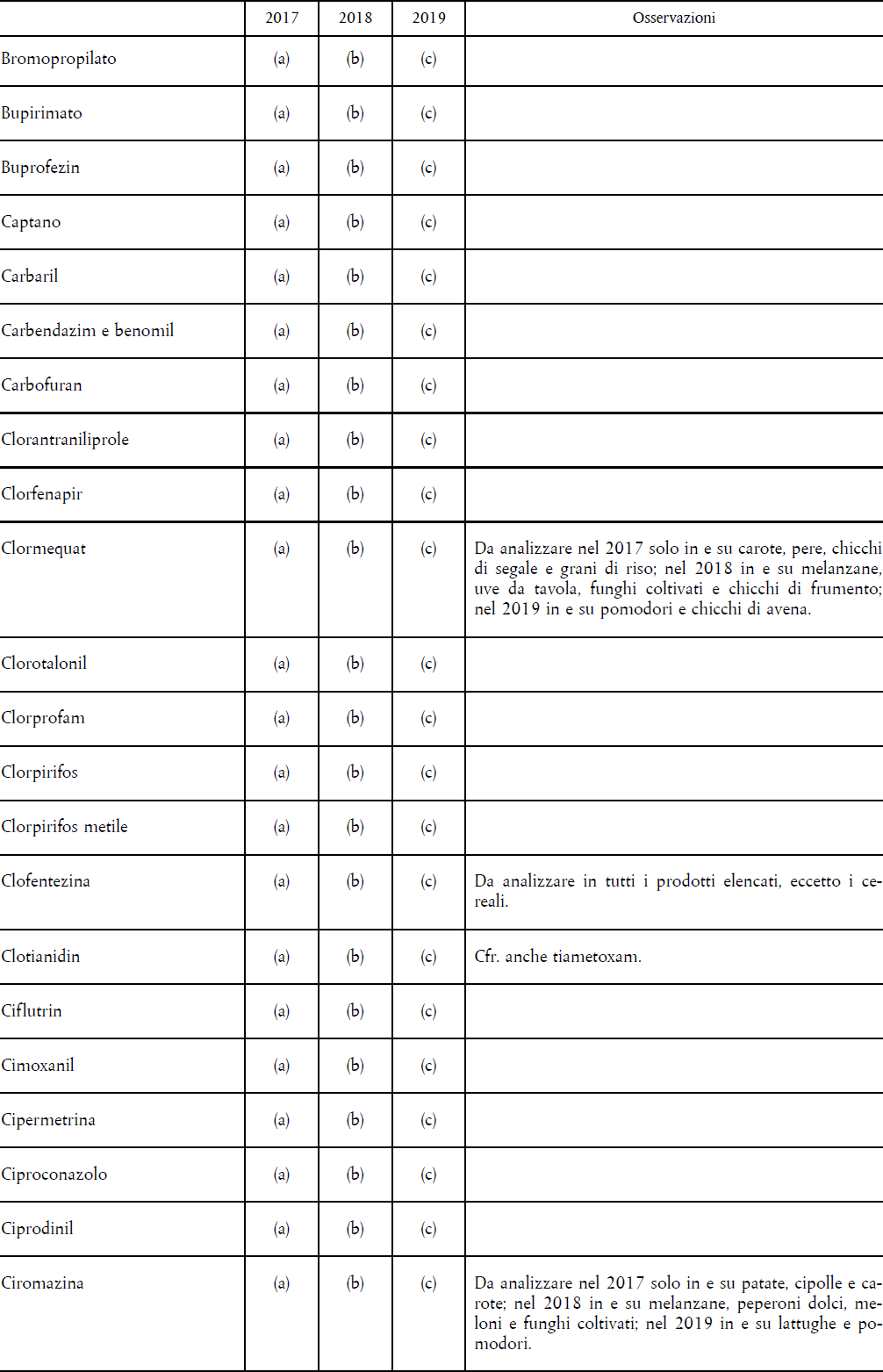
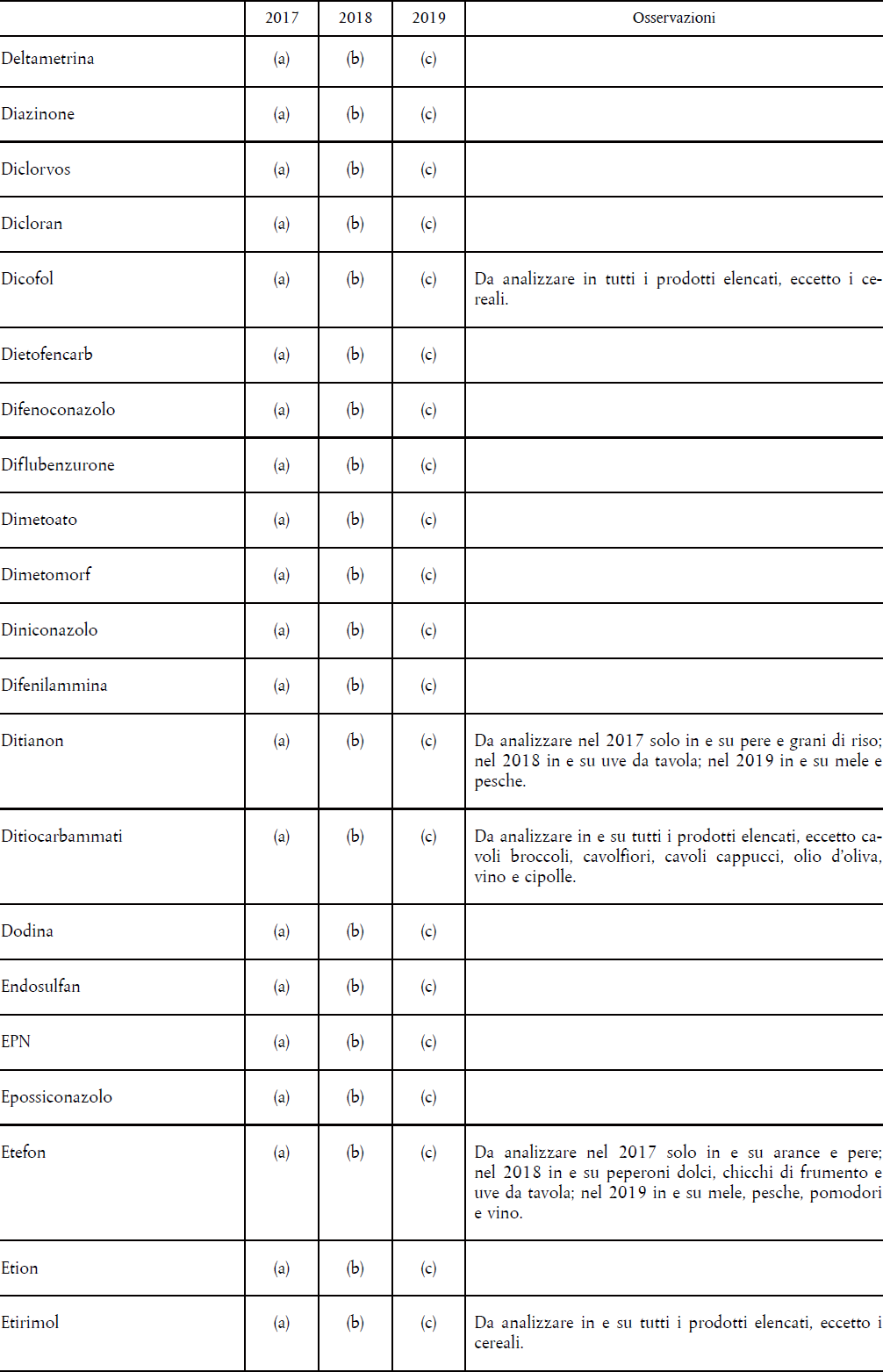
87
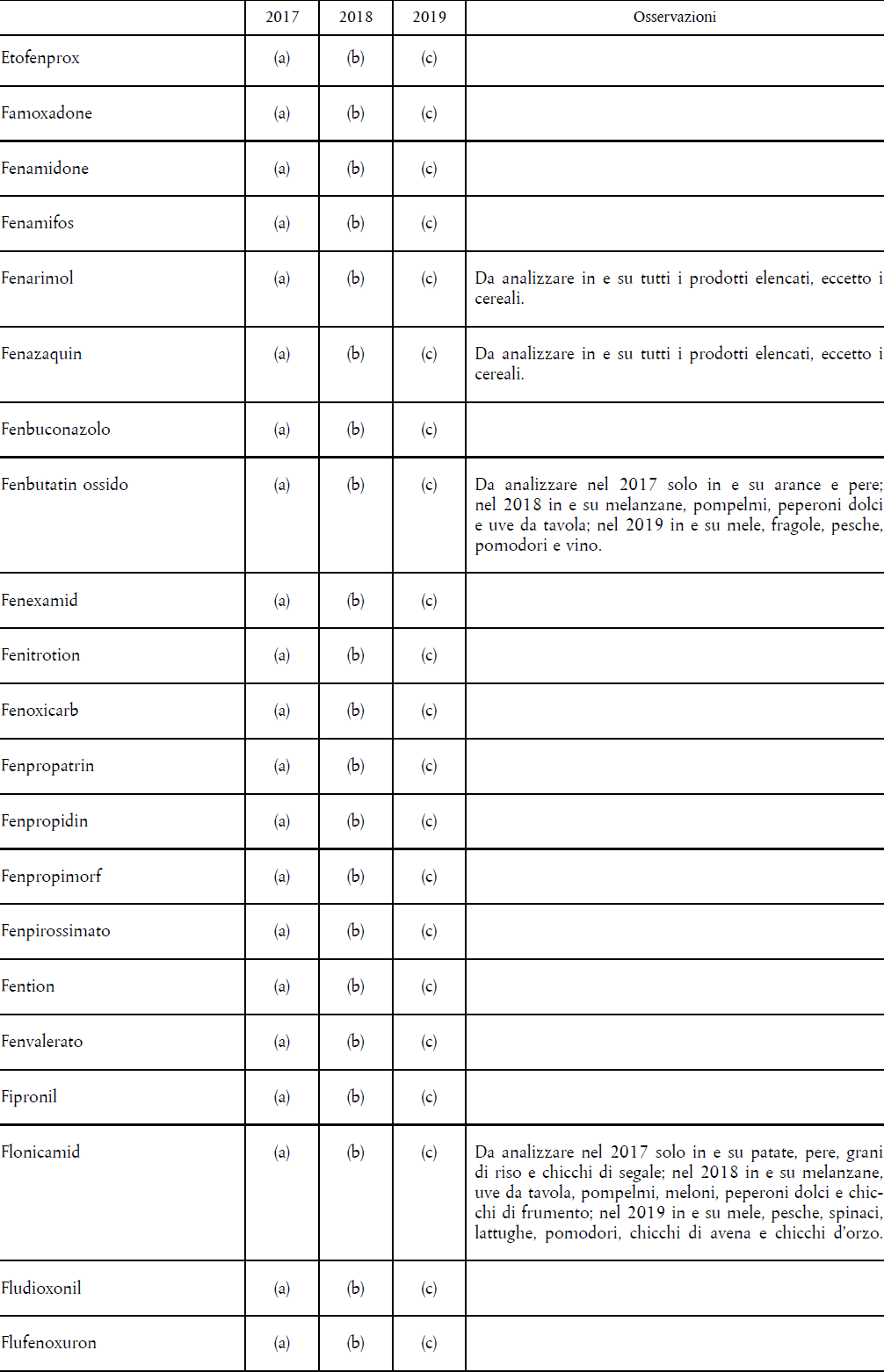
88
89
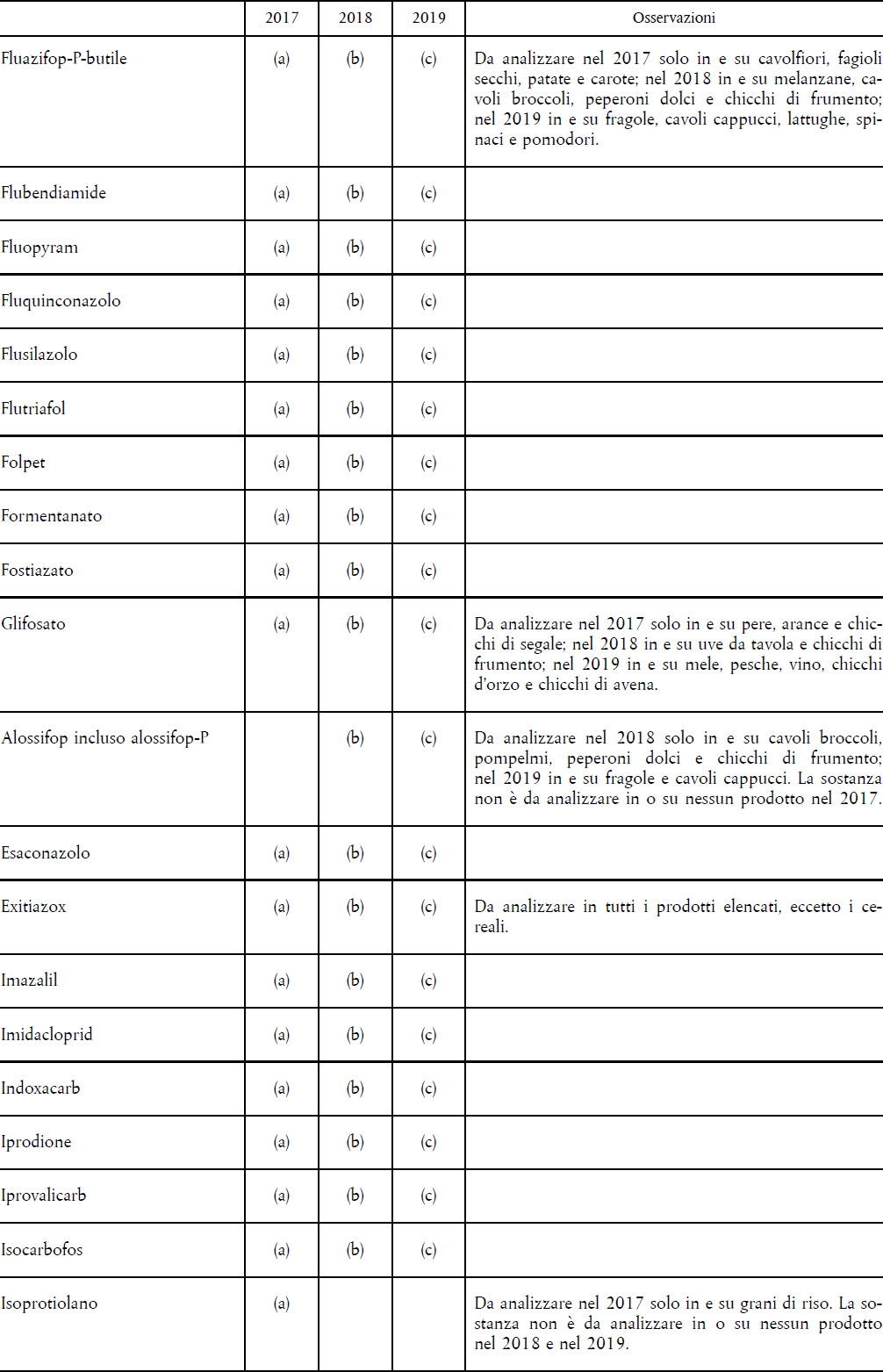
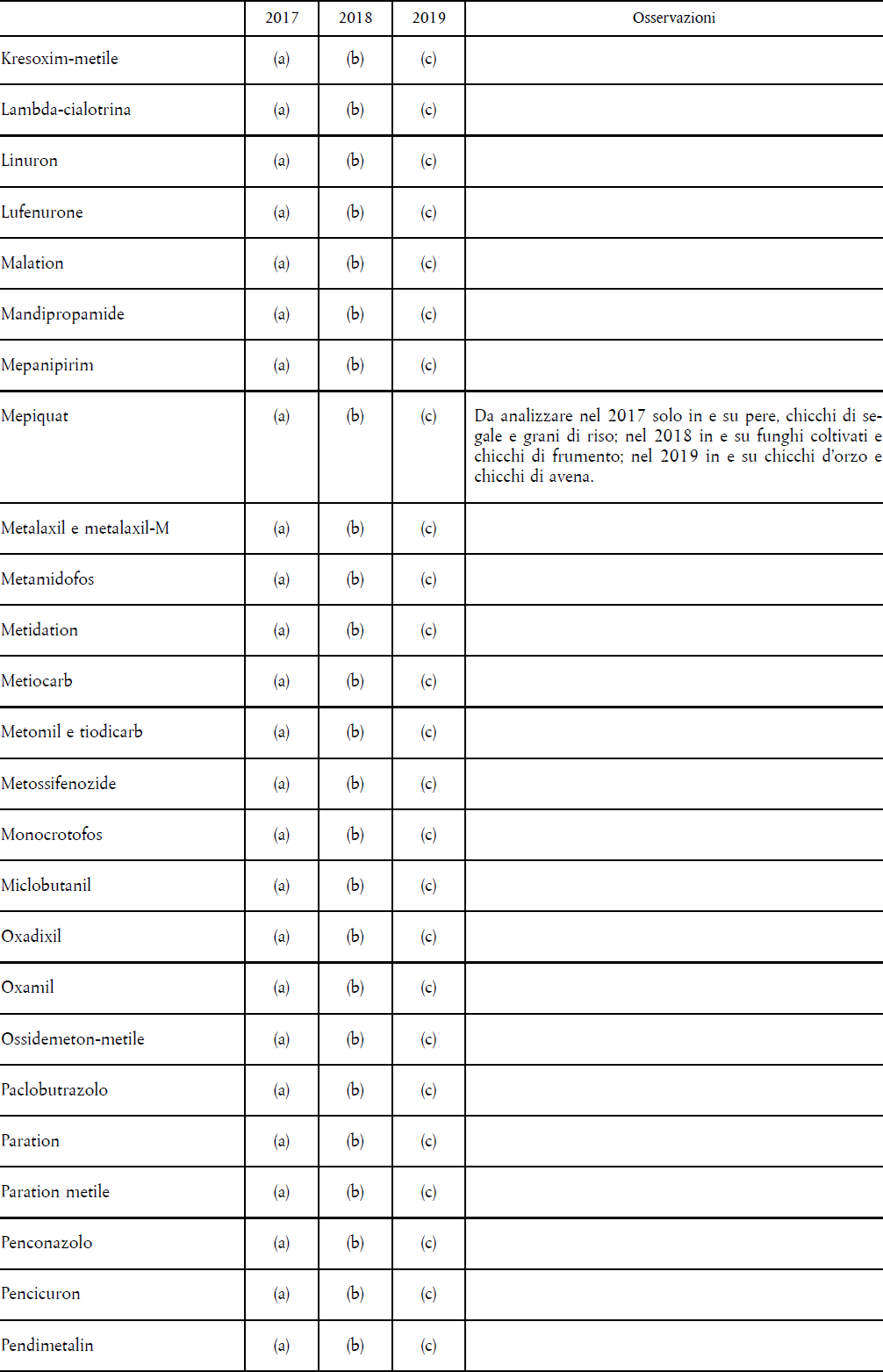
90
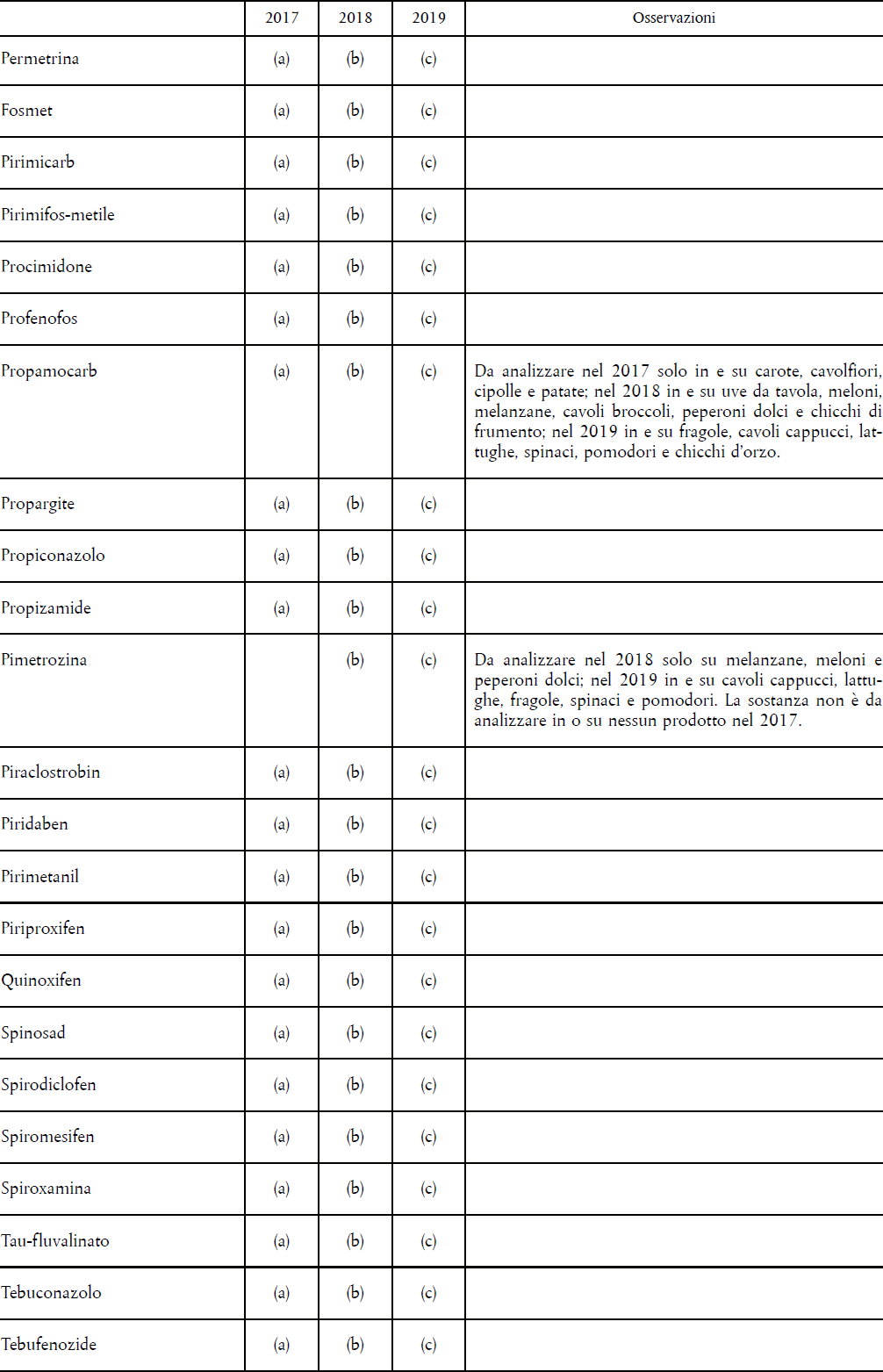
91
92
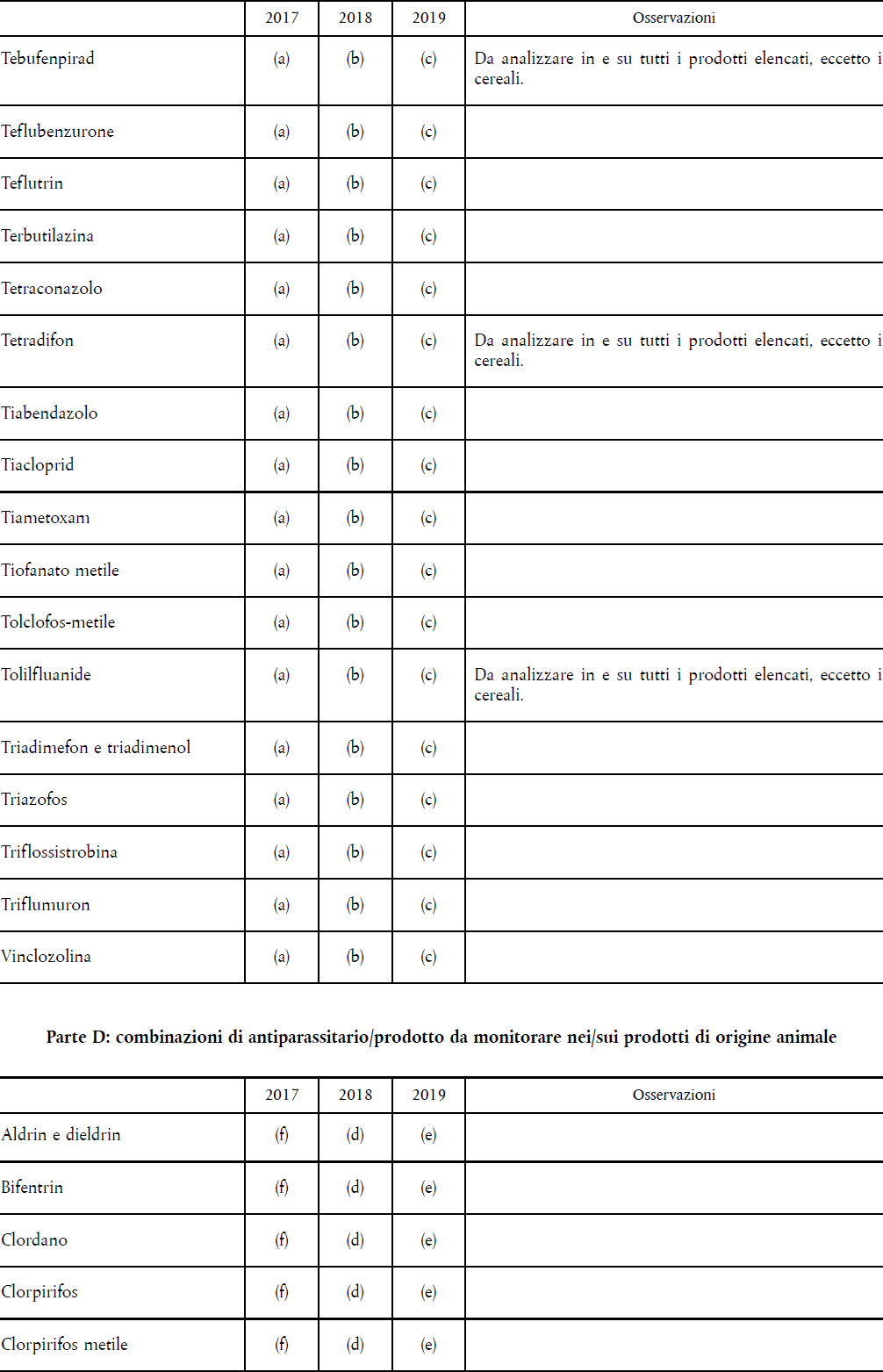
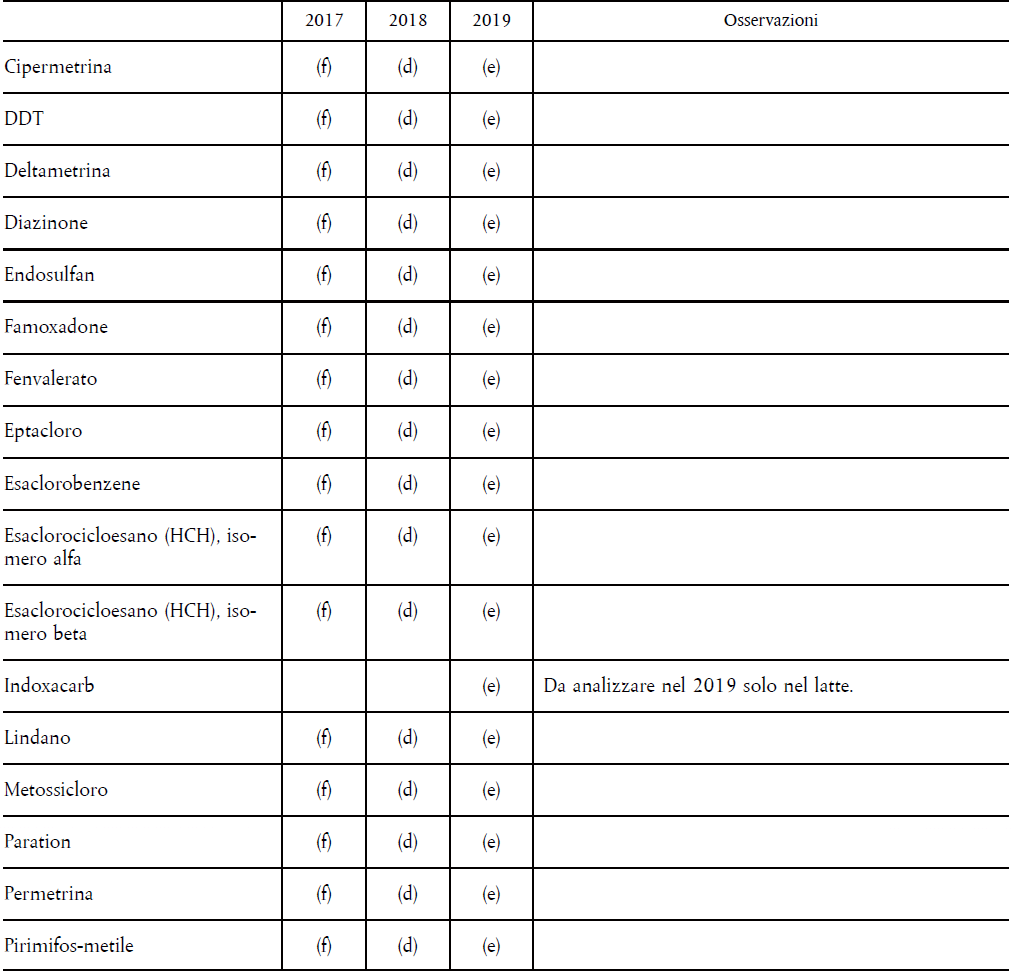
Il Regolamento (UE) 662/2016 inoltre precisa che:
il lotto da sottoporre a campionamento è scelto su base casuale;
-
-
- la procedura di campionamento è conforme a quanto disposto nella Direttiva 2002/63/CE;
- uno dei campioni per ciascun alimento, da prelevare e analizzare, deve provenire, se possibile, da prodotti dell’agricoltura biologica;
- l’Italia è tenuta a prelevare 69 campioni per ciascun prodotto alimentare specificato nella tabella X;
- oltre ai prodotti prescritti, ciascuno Stato Membro preleva ed analizza il numero e la tipologia di campioni indicati nella successiva tabella 2.
-
Tabella 2. Altri campioni da prelevare nel Programma di monitoraggio coordinato ai sensi del Reg. 662/2016/UE
| Anno | Descrizione dei prodotti da prelevare ogni anno |
| 2017 | 5 campioni di alimenti destinati ai lattanti e ai bambini |
| 2018 | 10 campioni di alimenti per lattanti e alimenti di proseguimento |
| 2019 | 10 campioni di alimenti per lattanti a base di cereali trattati. |
In Italia le indicazioni del Programma di Monitoraggio Coordinato vengono attuate dal Ministero della Salute che, con riferimento al Decreto Ministeriale del 23 dicembre 1992, recepisce le indicazioni dell’Unione Europea e fornisce indicazioni operative circa la suddivisione dei campioni da prelevare tra le Regioni e le Provincie Autonome (PA) di Trento e Bolzano. La ripartizione dei campioni è effettuata in base ai dati relativi al consumo e alla produzione di frutta e ortaggi, tenendo conto del valore minimo indicato dal Regolamento (UE) 662/2016.
I dati del Controllo Ufficiale vengono annualmente inviati all’Unione Europea e divulgati attraverso la pubblicazione di una relazione ufficiale, consultabile anche in formato elettronico sul sito del Ministero della Salute.
La Direttiva 2002/63/CE, come più volte ricordato in altri riferimenti legislativi (Regolamento (CE) 396/2005, Regolamento (UE) 662/2016, ecc.), stabilisce le modalità di campionamento dei prodotti alimentari ai fini del controllo ufficiale per la loro conformità agli LMR. Tale Direttiva è stata recepita in Italia dal Decreto del Ministero della Salute D.M. 23 luglio 2003.
D.M. 23 LUGLIO 2003 – METODI DI CAMPIONAMENTO AI FINI DEL CONTROLLO UFFICIALE DEI RESIDUI DI ANTIPARASSITARI NEI PRODOTTI ALIMENTARI DI ORIGINE VEGETALE E ANIMALE
Il prelevamento di campioni di prodotti alimentari di origine vegetale e animale per il controllo ufficiale dei residui di antiparassitari (sostanze attive dei prodotti fitosanitari) viene effettuato secondo i metodi riportati nell’allegato del D.M. DM 23 luglio 2003, in attuazione della succitata Direttiva 2002/63/CE.
I metodi di campionamento hanno lo scopo di permettere il prelievo di un campione rappresentativo in una partita da sottoporre ad analisi allo scopo di verificare la conformità di un prodotto con i limiti massimi di residui (LMR) di antiparassitari fissati nel regolamento 396/2005 e successive modifiche ed integrazioni.
Si ribadisce quindi che analizzando il campione si controlla la partita. È possibile affermare che, nel caso in cui un campione alimentare da sottoporre a controllo di conformità dei residui di pesticidi non sia stato prelevato in accordo a quanto stabilito dal DM 23 luglio 2003, tale campione potrebbe non essere rappresentativo della partita
da sottoporre a controllo.Da un punto di vista giuridico, il risultato delle successive analisi, l’eventuale giudizio di irregolarità e il conseguente procedimento penale potrebbero essere considerati nulli.
Di seguito si riportano degli esempi di campioni elementari ed entità minima delle aliquote in relazione al prodotto da prelevare estratte dalla tabella 4 del DM 23 luglio 2003:
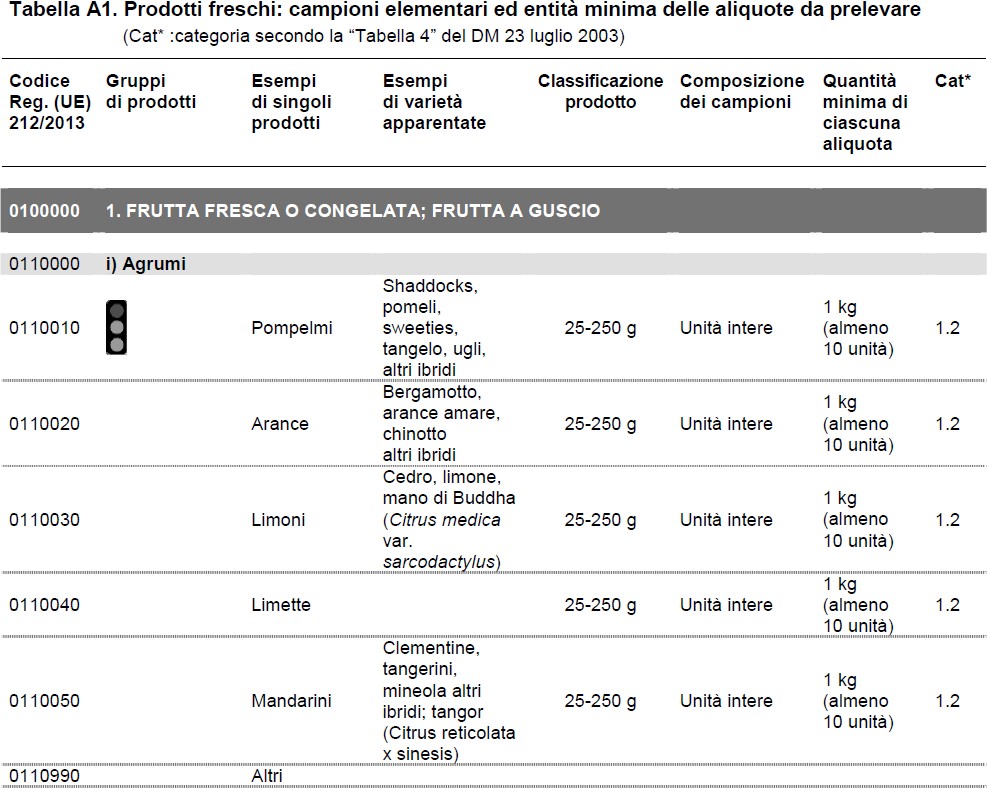
Il campione da inviare al laboratorio indica la quantità rappresentativa di materiale prelevata dal campione globale, da suddividere in aliquote da destinare alle analisi. Il campione di laboratorio può essere la totalità o una parte del campione globale. Non si devono tagliare o rompere le unità per costituire i campioni di laboratorio. Dal campione di laboratorio devono essere ricavate 4 (quattro) aliquote, secondo le modalità previste
dal DPR 26 marzo 1980 n. 327. Nel caso di prodotti confezionati non prelevati presso il produttore le aliquote devono essere 5 (cinque), una delle quali destinata al detentore della merce. Una delle parti delle aliquote prelevate viene consegnata, al momento del prelievo, al Responsabile dell’esercizio o ad un suo Rappresentante o al Detentore della merce. Le altre, insieme al verbale di prelevamento, vengono inviate per le analisi nel più breve tempo possibile al Laboratorio pubblico competente per territorio o ad altroLaboratorio autorizzato allo scopo. Una di tali parti è utilizzata per l’analisi di prima istanza, un’altra è destinata all’eventuale analisi di revisione e deve essere conservata per la durata di sessanta giorni a decorrere dalla data di comunicazione dell’esito dell’analisi all’interessato; ed un’altra parte infine rimane di riserva per eventuali perizie ordinate dall’Autorità Giudiziaria. In caso di prodotti confezionati, una parte del campione sarà messo a disposizione dell’impresa produttrice, per la durata di sessanta giorni, presso il laboratorio di cui al precedente comma.
In seguito alle analisi effettuate presso un Laboratorio di Controllo Ufficiale un campione alimentare potrebbe risultare non conforme ai requisiti del Regolamento (CE) 396/2005 relativamente agli LMR. Come conseguenza viene avviato un procedimento a carico del detentore e/o del produttore o rivenditore della merce; è quindi facoltà dell’interessato richiedere la revisione dell’analisi, come previsto dalla Legge n. 283 del 30.04.1962, da effettuarsi su un’ulteriore aliquota del campione presso l’Istituto Superiore di Sanità, Dipartimento di Ambiente e connessa prevenzione primaria, Reparto di Antiparassitari. L’immissione sul mercato di alimenti contenenti residui di pesticidi in quantità superiore ai loro rispettivi LMR comporta una denuncia penale, da parte dell’Autorità Sanitaria,
nei confronti del detentore della merce e/o del produttore o dell’importatore. In particolare, chi produce o mette in vendita prodotti alimentari è responsabile della loro sicurezza nei confronti della salute dei consumatori.
CAPITOLO 5. PIANO REGIONALE DI CAMPIONAMENTO AZIENDA SANITARIA UNICA REGIONE MARCHE ANNO 2017
In Italia le attività di controllo ufficiale degli alimenti e delle bevande hanno la finalità di verificare e garantire la sicurezza degli alimenti, prevenire i rischi per la salute pubblica
e proteggere gli interessi dei consumatori. Il controllo riguarda sia prodotti italiani o di
altra provenienza destinati ad essere commercializzati nel territorio nazionale, che quelli
destinati ad essere spediti negli Stati Membri oppure esportati nei Paesi Terzi. Esso
considera tutte le fasi della produzione, della trasformazione, della manipolazione, del
magazzinaggio, del prelievo dei campioni e analisi di laboratorio dei campioni prelevati. Quando asserisce ciò, Fa riferimento al DM del 23 luglio 2003?
Per poter portare avanti un efficace controllo sulle matrici alimentari si èindirizzata l’attività di vigilanza, per quanto riguarda le matrici da campionare, sulla base di evidenze oggettive.
Le evidenze sono date da:
- Numero, distribuzione degli stabilimenti di lavorazione degli alimenti e loro produzioni;
- Distribuzione della popolazione;
- I risultati delle attività di campionamento effettuate negli anni precedenti sulla base dei quali stabilire dati di prevalenza di contaminazione;
- Indagini su determinate matrici alimentari;
- Dati di allerte alimentari.
Allo stato attuale l’Intesa Stato-Regioni concernente le Linee Guida per il controllo ufficiale ai sensi dei Regolamenti CE 882/2004 e 854/2004, recepita con la Deliberazione
di Giunta del 5 dicembre 2016, n.1508, ha fornito al capitolo 15 – Controlli analitici sugli alimenti: interpretazione e gestione degli esiti analitici – indicazioni uniformi per la predisposizione dei piani di campionamento degli alimenti sia in termini quantitativi che in termini qualitativi (quali matrici e quali parametri). Gli allegati 6 e 7 delle suddette LL.GG. definiscono i pericoli da ricercare nelle diverse matrici alimentari, provvedendo anche alla loro ripartizione fra comparto produttivo e distributivo.
La Regione Marche ha concordato con i Laboratori del controllo ufficiale competenti per territorio, i piani di campionamento finalizzati all’applicazione delle normative e all’approfondimento delle caratteristiche dei pericoli microbiologici, chimici e fisici degli alimenti sulla base delle quali i Dipartimenti di Prevenzione delle Aree Vaste (ex ASL), organizzano la loro attività. Gli accertamenti analitici per i controlli su pericoli chimici, riguardano alimenti di origine prevalentemente vegetale e comprendono la ricerca di contaminati, residui di pesticidi e di altre sostanze indesiderate.
ASUR MARCHE –INDAGINE RESIDUI ANTIPARASSITARI SU E NEI PRODOTTI ALIMENTARI ANNO 2017
PREMESSA
Il controllo finalizzato al rispetto dei limiti del Reg. 396/2005 per l’Anno 2017,è stato svolto secondo le indicazioni della normativa comunitaria (Reg. UE del 15 aprile 2015 n.595) e secondo le prescrizioni della normativa italiana (D.M. 23 dicembre 1992).
Il Regolamento UE della Commissione del 15 aprile 2015 n.595 (sostituito dal Reg. UE n.660 del 6 aprile 2017) , stabilisce che sulla base di piani triennali deve essere adottato un programma comunitario coordinato di controllo per garantire il rispetto dei limiti massimi di residui di antiparassitari su e nei prodotti di origine vegetale e animale.
Il Decreto del Ministro della Sanità del 23 dicembre 1992, che recepisce la Direttiva 90/462/CEE, relativa alle quantità massime di residui di antiparassitari in prodotti di origine vegetale, compresi gli ortofrutticoli, incarica le Regioni e le Province Autonome di fornire ai Servizi Territoriali competenti appositi indirizzi per dare attuazione al programma dei controlli diretti a verificare il rispetto delle quantità massime di sostanze attive dei prodotti fitosanitari negli alimenti.
CAMPIONAMENTO
Le procedure di campionamento adottate nell’attuazione del piano campionamenti per l’anno 2017 dall’ASUR MARCHE, sono quelle stabilite nel Decreto del Ministero della Salute del 23 Luglio 2003 relativo ai metodi di campionamento ai fini del controllo ufficiale dei residui di antiparassitari nei prodotti alimentari di origine vegetale e
animale.
(DA RIPORTARE)
………………….
L’attività di campionamento è stata svolta presso:
-
-
- I centri di raccolta aziendale e cooperativi;
- I mercati generali specializzati e non specializzati;
- I depositi all’ingrosso;
- Gli ipermercati e supermercati; pertanto hanno riguardato:
- La produzione primaria;
- La trasformazione;
- I prodotti da esportare ed importati.
-
I lotti sottoposti a campionamento sono stati scelti su base casuale ed il campione globale è stato suddiviso in 4 aliquote (5 nel caso di prodotti non prelevati presso il produttore). Al fine di acquisire tutte le informazioni necessarie e secondo quanto previsto da normativa vigente, è stato redatto il verbale di campionamento che unitamente al campione, è stato consegnato al Laboratorio ARPAM o IZS secondo la tipologia di matrice e di ricerca da effettuare.
Il piano di campionamento ha riguardato i seguenti prodotti:
- Cereali in granella o farine;
- Ortaggi;
- Frutta;
- Olio;
- Vino;
- Miele.
DETERMINAZIONE ANALITICHE
ILaboratori hanno analizzato una gamma di residui di fitosanitari scelti, e incrementati nel tempo, in base a vari elementi:
-
-
- All’impiego dei prodotti fitosanitari nella coltura e perciò alla probabilità di essere ritrovati nell’alimento;
- Alle positività riscontrate sia in ambito regionale che nazionale nei monitoraggi degli anni precedenti;
- All’autorizzazione di nuovi principi attivi;
- Alle indicazioni del Ministero della Salute e della Commissione Europea;
- All’Allegato I del Reg. UE del 15 aprile 2015, n.595 (ora n.660/2017), in cui vengono
-
definiti i protocolli analitici(*) per valutare l’esposizione dei consumatori ai residui di antiparassitari in applicazione del programma coordinato di controllo;
E’ il caso di descrivere, anche se in breve, i protocolli analitici (v. in seguito), senza
creare un nuovo capitolo.
-
-
- Alla possibilità di essere determinati mediante il metodo del multiresiduo validato e la disponibilità di strumentazione analitica presente in laboratorio.
-
(*) Protocolli analitici
……………………….
È stata data inoltre continuità alla ricerca di pesticidi revocati o non più ammessi in determinate colture, per verificare rispettivamente gli usi illegali o gli utilizzi non autorizzati di tali prodotti, oppure perché rivestono notevole importanza sia tossicologica che ambientale. L’elenco dei principi attivi da tenere in considerazione circa “l’uptake” secondo il Programma di Controllo Nazionale (capitolo 4) è quello riportato nel documento SANCO 12745/2013.30 November 1 December 2015 rev. 6(3) (ora rev.9.3) “Working document on pesticides to be considered for inclusion in the national control programmes to ensure compliance with maximum residue levels of pesticides residues in and on food of plant and animal origin”.
In questa sede, per brevità, viene riportato detto elenco, limitatamente a taluni parametri
quali “Categorization”, “Frequent detection: Method”, “Recently Approved“, “Priority
List” e “High Toxicity”.
(da Doc. SANCO) (lasci il colore blu del carattere e si ricordi di cancellare questa nota)
…………………………………
3.1. Categorisation
The pesticides in chapter 4 are split up into the following categories:
-Frequent detections, MRL exceedances or RASFF notifications
-Recently approved
-Art. 12 priority list
-High toxicity
-
- Pesticides to be considered for analysis in products of plant origin
- Frequent detections, MRL exceedances or RASFF notifications
- Pesticides to be considered for analysis in products of plant origin
Benalaxayl including other mixtures of constituent isomers including benalaxyl-M
Method: MRM, Toxicity: ADI = 0.04 mg/kg bw/day, Clomazone
Method: MRM, Toxicity: ADI = 0.133 mg/kg bw/day, Cyazofamid
Method: MRM, Toxicity: ADI = 0.14 mg/kg bw/day, Etoxazole
Method: MRM, Toxicity: ADI = 0.04 mg/kg bw/day, Fluopicolide
Method: MRM, Toxicity: ADI = 0.08 mg/kg bw/day, Fosetyl-Al
Method: SRM, Toxicity: ADI = 3 mg/kg bw/day, Glufosinate ammonium
Method: SRM , Toxicity: ADI = 0.021 mg/kg bw/day, ( especially relevant for apples, cultivated fungi, peaches/ nectarines, potatoes, strawberries and rice. Additionally relevant for some non-MACP commodities such as: celery, currants maize and soy beans).
Heptachlor (Not approved)
Method: MRM, Toxicity: ADI = 0.0001 mg/kg bw/day, Phosphines and phosphides
Method: SRM, Toxicity: ADI = 0.011 mg/kg bw/day, Prosulfocarb
Method: MRM, Toxicity: ADI = 0.005 mg/kg bw/day, Quintozene (Not approved)
Method: MRM, Toxicity: ADI = 0.01 mg/kg bw/day,
-
-
- Recently approved
-
Ametoctradin (RD)
Approved since 08/2014, Method: MRM, Toxicity: ADI = 10 mg/kg bw/day, Benzovindiflupyr
Approval pending, Method: MRM, Toxicity: ADI 0-0.05 mg/kg bw day Emamectin benzoate
Approved since 5/2014, Method: MRM , Toxicity: ADI = 0.0005 mg/kg bw/day, Fenpyrazamine
Approved since 01/2013, Method: MRM, Toxicity: ADI = 0.13 mg/kg bw/day, Fluxapyroxad
Approved since 1/2013, Method: MRM, Toxicity: ADI = 0.02 mg/kg bw/day, Isopyrazam
Approved since 4/2013, Method: MRM , Toxicity: ADI = 0.03 mg/kg bw/day, Penflufen
Approved since 02/2014, Method: MRM, Toxicity: ADI = 0.04 mg/kg bw/day, Penthiopyrad
Approved since 5/2014, Method: MRM, Toxicity: ADI = 0.1 mg/kg bw/day, Spirotetramat
Approved since 5/2014, Method: MRM (high cost of standards of the metabolites), Toxicity: ADI = 0.05 mg/kg bw/day,
Sulfoxaflor
Approved since 8/2015, Method: MRM , Toxicity: ADI = 0.04 mg/kg bw/day, ARfD = 0.25 mg/kg bw /day
-
-
- Art. 12 priority list
-
(On Art. 12 priority list because of possible chronic consumer risk) Diquat
Method: SRM, Toxicity: ADI 0.002 mg/kg bw/day, (especially relevant for potatoes, dried beans and cereals (e.g. barley, maize, oats); additionally relevant for some non-MACP comodities such as: sweet potatoes, various dry pulses (e.g. dry lentils, dry peas, soya beans), various oilseeds (e.g. borage seeds, rape seeds, sesame seeds, chia seeds, sunflower seeds, mustard seeds and linseed).
-
-
- High toxicity
-
Ethoprophos
Toxicity: ADI = 0.0004 mg/kg bw/day,
(in pagina a parte)
Piano campionamenti 2017 ASUR MARCHE – campioni minimi programmati
| Frutta | Ortaggi | Cereali in
granella o farine |
Miele | Vino | Olio | Tot. |
| 50 | 56 | 90 | 25 | 25 | 13 | 259 |
ESITO CONTROLLO RESIDUI ANTIPARASSITARI SU E NEI PRODOTTI ALIMENTARI ANNO 2017
A fronte di un programma di campionamento che prevedeva un numero minimo di campioni pari a 259 suddiviso tra le varie tipologie di prodotti vegetali, già nominate in precedenza, l’ASUR MARCHE nell’Anno 2017 è stata molto virtuosa, riuscendo ad effettuare ben 374 campioni di prodotti alimentari di origine vegetale.
Di seguito si riportano in dettaglio gli esiti del controllo residui di antiparassitari:
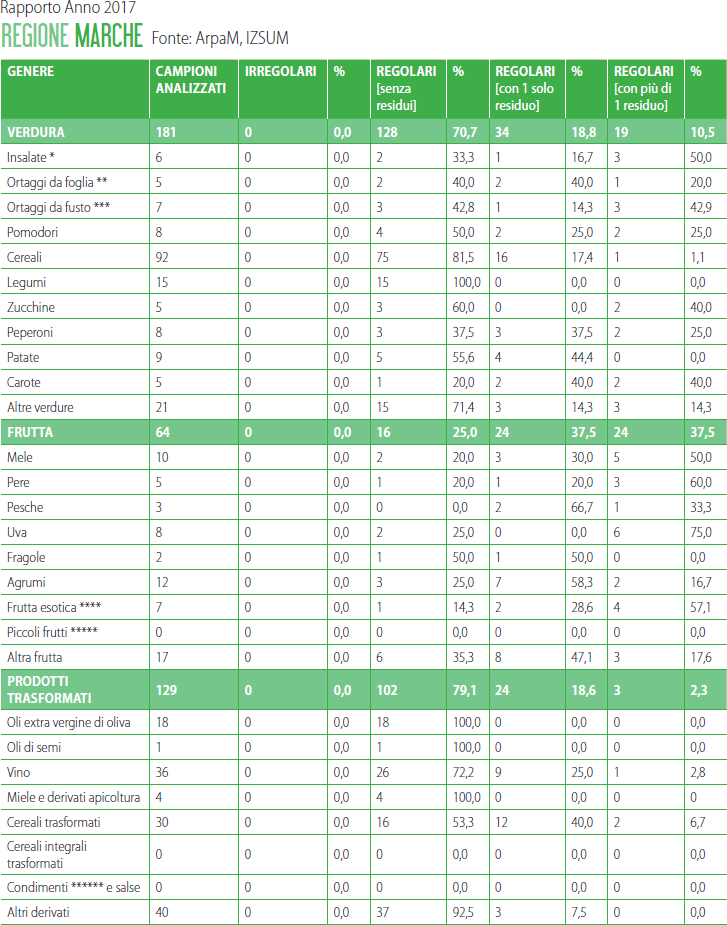
Nei 362 campioni analizzati dall’ArpaM, la percentuale dei campioni contenenti uno o più residui di pesticidi ha raggiunto il 34% e il multiresiduo si è attestato all’11,6%.
I campioni di frutta che hanno presentato il maggior numero di principi attivi (cinque per campione) sono quelli riferiti a Pere e Uva. I multiresiduo maggiormente presenti sono risultati essere il Pirimos-Metile (organafosfato) e Clorpirifos(organofosforico)con numero di positività riscontrata rispettivamente di 27 e 20.
Per quanto riguarda i 12 campioni analizzati dall’IZSUM, 7 sono risultati regolari, 1 campione di ciliegie è risultato regolare con la presenza di un residuo di Thiamethoxam (Neonicotinoide), mentre i 4 campioni rimanenti risultano regolari ma con la presenza di più residui:
- 1 con 3 residui: Boscalid (Anilide), Clorpirifos (organofosforico)e
Metossifenozide(diacilidrazine) ;
- 1 con 4 residui: Triadimenol(triazolinoni), Imidacloprid(neonicotinoidi), , Flutriafol(Triazolinoni)e Tebuconazolo (triazolinoni);
- 2 con 5 residuidi cui 1 con Carbendazim(benzimidazoli), Boscalid (Anilide), Piraclostrobin (strobilurine), Azossistrobina (strobilurine)e Thiacloprid (neonicotinoidi);
- 1 con Thiacloprid (neonicotinoidi), Tebuconazolo(triazolinoni), Miclobutanil
(triazolinoni) , Lambda-Cialotrina(Piretroidi)e Triflossistrobina (strobilurine)
5.5 REPERTI ANALITICI
Non essendo possibile, per ovvi motivi, inserire tutti i reperti analitici inerenti al piano di campionamento svolto nell’Anno 2017, si riporta a titolo illustrativo copia di un reperto analitico riferito a campione di farina di grano tenero prelevato c/o un molino nel Comune di Monteprandone (AP) in data 30/08/2017 dallo scrivente:

111
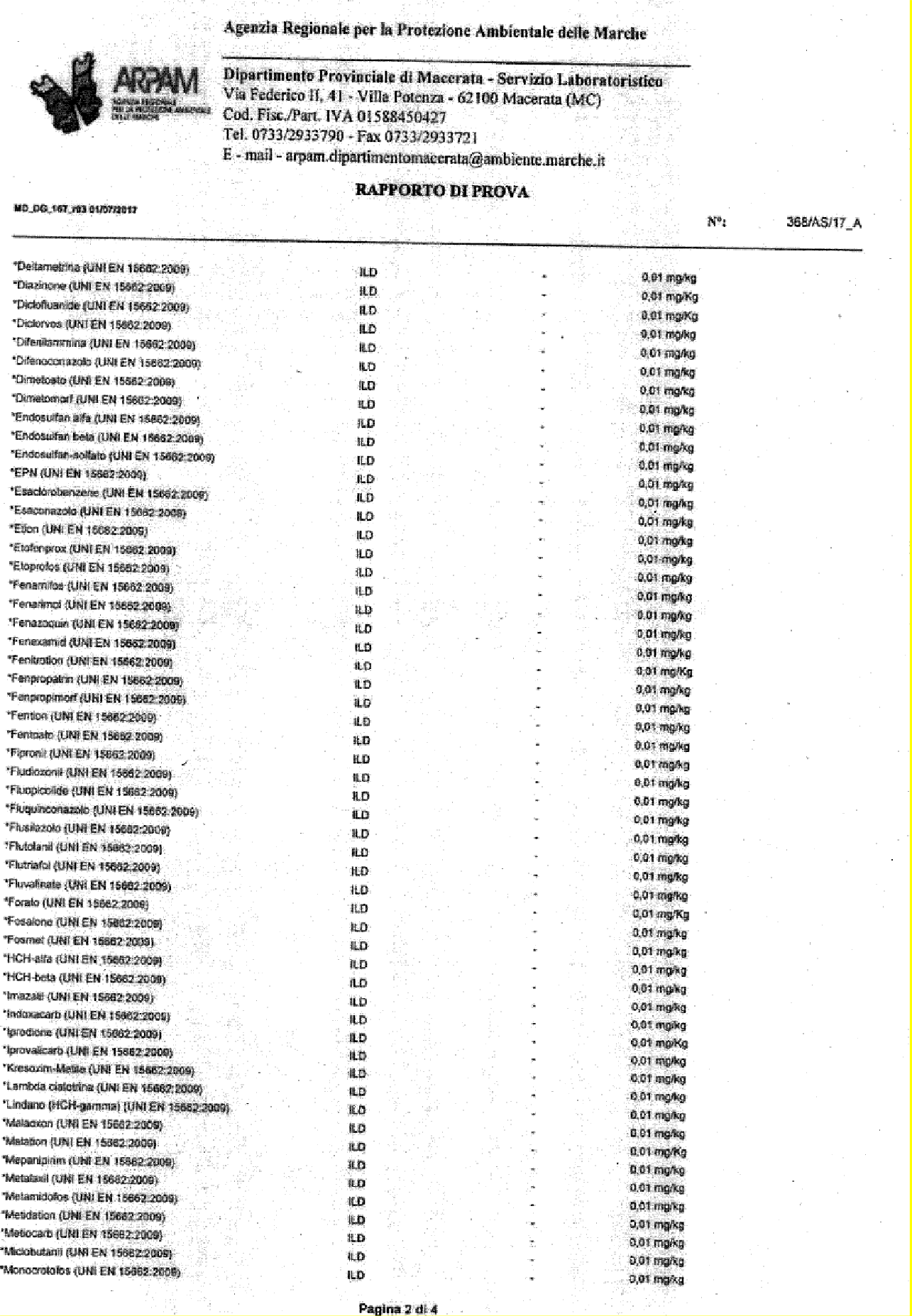
112
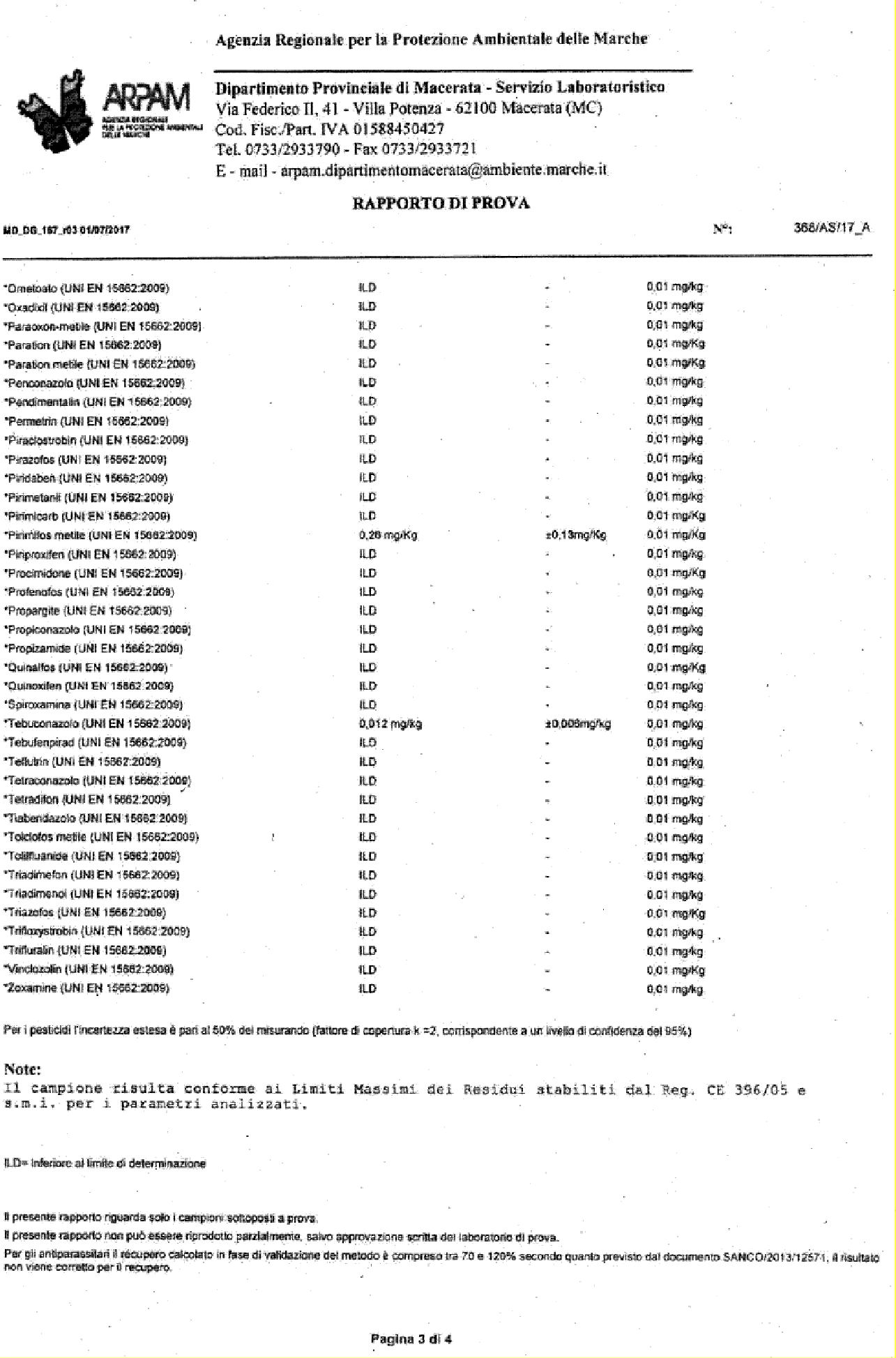
113

114
CONSIDERAZIONI CONCLUSIVE
Con il presente elaborato, frutto di una profonda ricerca e un’attenta analisi si è tentato di mettere a disposizione del lettore tutte le informazioni necessarie a comprendere come se da un lato l’utilità dei pesticidi in agricoltura, nell’ultimo mezzo secolo, ha portato enormi vantaggi in termini di produttività dei raccolti, permettendo un più ampio sfruttamento delle aree coltivabili, una difesa più efficace contro le malattie infettive e parassitarie e una migliore conservazione dei prodotti agricoli, dall’altro il raggiungimento di questi indiscussi vantaggi è avvenuto a caro prezzo per l’ambiente che ha pagato e ne paga, le conseguenze soprattutto in termini di progressiva contaminazione del suolo e delle acque. La contaminazione da pesticidi impatta, oltre che sulle singole specie di insetti dannosi, su interi ecosistemi e sulla biodiversità nel suo complesso, sollevando questioni rilevanti sul modo in cui queste sostanze chimiche vengono valutate, autorizzate e regolamentate nell’UE e nel mondo intero.
Si è voluto mettere in evidenza come nonostante la sicurezza dell’ecosistema, divenuta una prerogativa sempre più importante nella scelta da parte degli utilizzatori di insetticidi sempre meno aggressivi per l’ambiente ma sempre più efficace nel combattere i parassiti, abbia indotto i Ricercatori a sviluppare nuove molecole di insetticidi che hanno via via sostituito i pesticidi di vecchia concezione esi fa riferimento ai pesticidi neonicotinoidi che grazie alla loro eccellente efficacia e alla loro relativamente bassa tossicità nei confronti dell’ambiente e dei mammiferi hanno occupato gran parte del mercato degli antiparassitari, tuttavia non sono stati esenti da nuove ripercussioni
mettendo in pericolo la vita di ecosistemi fondamentali per lo svolgimento della vita
stessa dell’uomo, come l’impollinazione, dovuta all’ incremento della mortalità delle api che va sotto il nome di Sindrome da Spopolamento degli Alveari (SSA). Tematica di interesse mondiale che ha visto coinvolti numerosi studi al fine di correlare questa classe più recente di fitofarmaci e la moria di api, per giungere al 28 Febbraio 2018 quando l’Autorità Europea per la Sicurezza Alimentare (EFSA) ha aggiornato le proprie valutazioni del rischio relative a tre neonicotinoidi“clothianidin, imidacloprid e thiamethoxam” concludendo che la maggior parte dei modi in cui i pesticidi neonicotinoidi vengono usati “rappresenta un rischio per le api selvatiche e quelle mellifere” e che ha portato l’Unione Europea il 27Aprile 2018 (Italia compresa) a pronunciarsi a favore della messa albando dei 3 neonicotinoidi, Imidacloprid, Clothianidin e Tiamethoxam limitandone l’utilizzo esclusivo nelle serre.
In seguito si è voluto evidenziare come l’Unione Europea attraverso un programma coordinato che si interseca con i programmi nazionali dei Paesi Membri, svolga un’attenta analisi (attraverso il Controllo Ufficiale) al fine di garantire un livello elevato di protezione del consumatore e volto a conoscerel’effettiva presenza dei Livelli Massimi consentiti di Residui nelle derrate alimentari.
Confrontando i dati relativi al 2016 (pubblicati dal Ministero della Salute il 14/03/2018) con quelli degli anni precedenti, risulta evidente come lapercentuale di irregolarità negli ortofrutticoli abbia subito un assestamento al disotto della mediaeuropea ed al disotto dell’ 1% (0,9%). Tale risultato positivo è attribuibile in parte alle attività delle strutture sia centrali sia territoriali ormai permanentemente impegnate nel controllo ufficiale (orgoglioso di farne parte) in materia di prodotti fitosanitari in Italia, in parte alla
costante revisione in senso restrittivooperata dal Ministero su alcuni impieghi ammessi, nonché aduna sempre maggiore consapevolezzadegli operatori agricoli nell’impiego dei prodotti fitosanitari. C’è da sottolineare, ad ogni modo, come il superamento occasionale di un limite legale non comporti un pericolo per la salute, ma il superamento di una soglia legale tossicologicamenteaccettabile. La tendenza decrescente delle irregolarità configura, comunque, una situazione in progressivo miglioramento dal punto di vista della sicurezza dei prodotti alimentari. Relativamente al livello di esposizione della popolazione italiana con la dieta, le stime diassunzione elaborate con i dati relativi ad anni precedenti, ma simili nei risultati, indicano che i residui dei singoli pesticidi ingeriti ogni giorno dal consumatore rappresentano una percentuale molto modesta dei valori delle dosi giornaliere accettabili delle singole sostanze attive e molto al di sotto del livellodi guardia preso come riferimento per assicurare la qualità igienico-sanitaria e tossicologica deglialimenti.
Complessivamente, come per gli scorsi anni, i risultati dei controlli ufficiali italianicontinuano ad essere in linea con quelli rilevati negli altri Paesi dell’Unione Europea e indicano un elevato livello di protezione del consumatore.
Osservando i risultati dell’indagineper la ricerca dei residui di antiparassitari nei prodotti alimentari per l’Anno 2017 (il 2018 è ancora in corso d’opera) portato a termine dalla Regione Marche attraverso i Dipartimenti della Prevenzione dell’Azienda Sanitaria Unica Regionale (di cui lo scrivente è parte attiva) e i Laboratori Competenti per territorio (ARPAM e IZSUM), possiamo confermare che i dati ricalcano quelli ottenuti a livello nazionale.
Tuttavia risulta evidente che se da un lato la normativa vigente abbia portato sicuramente ad un maggior esame delle sostanze attive impiegate nelle formulazioni e a controlli più stringenti sull’uso corretto dei pesticidi in agricoltura, dall’altro i piani di controllo dei residui di fitosanitari negli alimenti, predisposti a livello europeo e nazionale, non dedicano la giusta attenzione al fenomeno del multiresiduo, in quanto la definizione del limite massimo di residuo consentito per legge negli alimenti, ossia l’LMR elaborato dall’Autorità per la sicurezza alimentare (EFSA), si basa solo sul singolo principio attivo. In tal modo, si esclude la valutazione degli effetti sinergici che potrebbero derivare dalla presenza concomitante di più residui chimici in uno stesso alimento, seppur a basse concentrazioni ed entro i limiti di legge.
Su questo punto si è espressa anche l’Unione Europa, affinché siano approfonditi i rischi
dell’esposizione contemporanea a più sostanze chimiche pertanto attendiamo che sul fenomeno del multiresiduo sia definito un campo di indagine a tutto tondo e che l’EFSA, autorità preposta a vigilare sulla salute dei consumatori, proceda con passi più spediti verso una risoluzione del problema, contemplando la valutazione di come sostanze chimiche diverse, presenti negli alimenti, possano interagire tra di loro e nell’organismo. Per concludere possiamo affermare che se l’obiettivo fondamentale è quello di ridurre i rischi e l’impatto sulla salute umana, sull’ambiente e sulla biodiversità, sarebbe auspicabile il ricorso a diversi approcci quali la difesa integrata piuttosto che l’agricoltura biologica o “approcci alternativi” di indubbia validità come la Green Chemistry (Chimica Verde), incentivandone lo Sviluppo e la Ricerca, perché come dicevano i latini “praestat cautela quammedela”.
RIFERIMENTI NORMATIVI e BIBLIOGRAFICI
Legge 30 aprile 1962, n. 283, Modifica degli articoli 242, 243, 247, 250 e 262 del testo unico
delle leggi sanitarie, approvato con regio decreto 27 luglio 1934, n. 1265: Disciplina igienica della produzione e della vendita delle sostanze alimentari e delle bevande Art.6.
Decreto del Presidente della Repubblica 26 marzo 1980, n. 327, Regolamento di esecuzione della L. 30 aprile 1962, n. 283, e successive modificazioni, in materia di disciplina igienica della produzione e della vendita delle sostanze alimentari e delle bevande.
Ministero della Sanità. Decreto Ministeriale del 23/12/1992. Recepimento della direttiva
n. 90/642/CEE relativa ai limiti massimi di residui di sostanze attive dei presidi sanitari tollerate su ed in prodotti.
Direttiva 14 giugno 1993, n. 93/43/CEE del Consiglio, in materia di “igiene dei prodotti alimentari”.
Libro Bianco sulla Sicurezza Alimentare gennaio 2000 della Commissione delle Comunità Europea.
Direttiva 2002/63/CE della Commissione, dell’11 luglio 2002, che stabilisce metodi comunitari di campionamento ai fini del controllo ufficiale dei residui di antiparassitari sui e nei prodotti di origine vegetale e animale e che abroga la direttiva 79/700/CEE.
Regolamento (CE) 28 gennaio 2002, n. 178/2002 del Parlamento Europeo e del Consiglio, che “stabilisce i principi e i requisiti generali della legislazione alimentare, istituisce l’Autorità europea per la sicurezza alimentare e fissa procedure nel campo della sicurezza alimentare”.
Decreto Ministeriale del 23/07/2003 Attuazione della direttiva 2002/63/CE 11 luglio 2002 relativa ai metodi di campionamento ai fini del controllo ufficiale dei residui di antiparassitari nei prodotti alimentari di origine vegetale e animale.
Regolamento (CE) 29 aprile 2004, n. 852/2004 del Parlamento Europeo e del Consiglio, in materia di “igiene dei prodotti alimentari” .
Regolamento (CE) 29 aprile 2004, n. 853/2004 del Parlamento Europeo e del Consiglio, che “stabilisce norme specifiche in materia di igiene per gli alimenti di origine animale”.
Regolamento(CE) 29 aprile 2004, n. 854/2004 del Parlamento Europeo e del Consiglio, che “stabilisce norme specifiche in materia di organizzazione di controlli ufficiali sui prodotti di origine animale destinati al consumo umano”.
Regolamento (CE) 29 aprile 2004, n. 882/2004 del Parlamento Europeo e del 87 Consiglio, relativo ai “controlli ufficiali intesi verificare la conformità alla normativa in materia di mangimi ed alimenti e alle norme sulla salute e sul benessere animale”.
Regolamento (CE) n. 396/2005 del Parlamento Europeo e del Consiglio del 23 febbraio 2005 concernente i livelli massimi di residui di antiparassitari nei o sui prodotti alimentari e mangimi di origine vegetale e animale e che modifica la direttiva 91/414/CEE del Consiglio.
Decreto Legislativo n. 193 del 6 novembre 2007, relativo alla Attuazione della direttiva 2004/41/CE relativa ai controlli in materia di sicurezza alimentare e applicazione dei regolamenti comunitari nel medesimo settore.
Ministero del Lavoro, della Salute e delle Politiche Sociali
Decreto 17 settembre 2008, Sospensione cautelativa dell’autorizzazione di impiego per la concia di sementi, dei prodotti fitosanitari contenenti le sostanze attive clothianidin, thiamethoxam, imidacloprid e fipronil, ai sensi dell’articolo 13, comma 1, del decreto del Presidente della Repubblica 23 aprile 2001, n. 290.
Ministero del Lavoro, della Salute e delle Politiche Sociali
Decreto 26 Gennaio 2009, fissazione del limite temporale relativo alla sospensione cautelativa dell’autorizzazione di impiego per la concia di sementi dei prodotti fitosanitari contenenti le sostanze attive clothianidin, thiamethoxam, imidacloprid e fipronil ai sensi dell’articolo 13, comma 1, del decreto del Presidente della Repubblica 23 aprile 2001, n. 290 di cui al Decreto Dirigenziale del 17 settembre 2008.
Ministero del Lavoro, della Salute e delle Politiche Sociali
Decreto 14 settembre 2009, proroga della sospensione cautelativa dell’autorizzazione di impiego per la concia di sementi dei prodotti fitosanitari contenenti le sostanze attive clothianidin, thiamethoxam, imidacloprid e fipronil.
Ministero della Salute, Decreto 16 settembre 2010 Proroga della sospensione cautelativa dell’autorizzazione di impiego, per la concia di sementi, dei prodotti fitosanitari contenenti le sostanze attive clothianidin, thiamethoxam, imidacloprid e fipronil, di cui al decreto dirigenziale 14 settembre 2009.
Decreto 28 giugno 2011, Proroga della sospensione cautelativa dell’autorizzazione di impiego per la concia di sementi dei prodotti fitosanitari contenenti le sostanze attive clothianidin, thiamethoxam, imidacloprid e fipronil, di cui al decreto dirigenziale del 16 settembre 2010.
Decreto Ministero della Salute del 25 ottobre 2011: Proroga al 30 giugno 2012 della sospensione cautelativa dell’autorizzazione di impiego per la concia di sementi dei prodotti fitosanitari contenenti le sostanze attive clothianidin, thiamethoxam, imidacloprid e fipronil, di cui al decreto dirigenziale 28 giugno 2011.
Regolamento (UE) N. 212/2013 della Commissione dell’11 marzo 2013 che sostituisce l’allegato I del regolamento (CE) n. 396/2005 del Parlamento europeo e del Consiglio per quanto riguarda le aggiunte e le modifiche concernenti i prodotti di cui a tale allegato.
Regolamento di esecuzione (UE) n. 485/2013 della commissione del 24 maggio 2013 che modifica il regolamento di esecuzione (UE) n. 540/2011 per quanto riguarda le condizioni di approvazione delle sostanze attive clothianidin, tiametoxam e imidacloprid, e che vieta l’uso e la vendita di sementi conciate con prodotti fitosanitari contenenti tali sostanze attive.
Decreto Ministero della Salute del 25 giugno 2013: Revoca delle autorizzazioni all’immissione in commercio e all’impiego di prodotti fitosanitari, contenenti le sostanze attive clothianidin, thiamethoxam e imidacloprid, per il trattamento delle sementi e del terreno, ai sensi del regolamento di esecuzione (UE) n. 485/2013 della Commissione del 24 maggio 2013 e che vieta l’uso e la vendita di sementi conciate con prodotti fitosanitari contenenti tali sostanze attive.
Regolamento di esecuzione (UE) n. 662/2016 della Commissione relativo a un programma coordinato di controllo pluriennale dell’Unione per il 2017, il 2018 e il 2019, destinato a garantire il rispetto dei livelli massimi di residui di antiparassitari e a valutare l’esposizione dei consumatori ai residui di antiparassitari nei e sui prodotti alimentari di origine vegetale e animale.
Tomizawa M, Casida J.E. Selective toxicity of neonicotinoids attributable tospecificity of insect and mammalian nicotinic receptors. AnnualReview of Entomology2003; 48: 339- 364.
Greatti, M., Barbattini, R., Stravisi, A., Sabatini, A. G., & Rossi, S. (2006). Presence of the imidacloprid on vegetation near corn fields sown with Gaucho® dressed seeds. Bulletin of Insectology, 59(2), 99.
Jeschke, P., &Nauen, R. (2008). Neonicotinoids—from zero to hero in insecticide chemistry. Pest management science, 64(11), 1084-1098.
Alkahtane AA et al. Cytotoxicity and Genotoxicity of Cypermethrin in Hepatocarcinoma Cells: A Dose- and Time-Dependent Study. Dose Response. 16, (2018)
Sharma P. et al. Cypermethrin induced reproductive toxicity in male Wistar rats: protective role of Tribulus terrestris. J. Environ. Biol. 34,857-62, (2013).
Madsen C. et al. Immunotoxicity of the pyrethroid insecticides deltametrin and alpha- cypermetrin. Toxicology. 107, 219-27, (1996).
Dai. P. Chronic Toxicity of clothianidin, imidacloprid, chlorpyrifos, and dimethoate to Apis mellifera L. larvae reared in vitro. Pest Manag Sci. 2018, (ahead of print).
Li G. et al. The Wisdom of Honeybee Defenses Against Environmental Stresses, Front Microbiol, 1,9, 722, (2018)
Pistorius J, Bischoff G, Heimbach U, Stähler M (2009) Bee poisoning incidents in Germany in spring 2008 caused by abrasion of active substance from treated seeds during sowing of maize. In: Proceedings “Hazards of pesticides to bees—10th international symposium of the ICP-bee protection group”. Julius-KühnArchiv 423:118–126
Johnson, R. M., Ellis, M. D., Mullin, C. A., & Frazier, M. (2010). Pesticides and honey bee toxicity USA. Apidologie, 41(3), 312-331.
Nazzi, F., Brown, S. P., Annoscia, D., Del Piccolo, F., Di Prisco, G., Varricchio, P., … &Pennacchio, F. (2012). Synergistic parasite-pathogen interactions mediated by host immunity can drive the collapse of honeybee colonies. PLoSPathog, 8(6), e1002735.
Girolami, V., Marzaro, M., Vivan, L., Mazzon, L., Greatti, M., Giorio, C., … &Tapparo, A. (2012). Fatal powdering of bees in flight with particulates of neonicotinoids seed coating and humidity implication. Journal of applied entomology, 136(1‐2), 17-26
Henry M, Beguin M, Requier F, et al. A common pesticide decreases foraging success and survival in honey bees. Science. 2012;336:348–350. doi: 10.1126/science.1215039.
Whitehorn PR, O’Connor S, Wackers FL, Goulson D. Neonicotinoid pesticide reduces bumble bee colony growth and queen production. Science. 2012;336:351–352. doi: 10.1126/science.1215025.
European Commission (EC) (2004b) Review report for the active substance thiacloprid European Commission (EC) (2005) Review report for the active substance clothianidin European Commission (EC) (2006) Review report for the active substance thiamethoxam
European Food Safety Authority (EFSA) (2008) Conclusion regarding the peer review of
the pesticide risk assessment of the active substance imidacloprid. European Food Safety Authority Scientific Report, European Food Safety Authority, Parma
Wetterauer B et al. Toxicity, dioxin-like activities, and endocrine effects of DDT metabolites……Environ SciPollut Res Int. 19(2), 403-15, 2012.
Kimura-Kuroda J et al., Nicotine-like effects of the neonicotinoid insecticides acetamiprid and imidacloprid on cerebellar neurons from neonatal rats. PloS ONE 7 (2), 2012 .
Kim J1, Park Y, Yoon KS, Clark JM, Park Y.Imidacloprid, a neonicotinoid insecticide, induces insulin resistance. The J of Toxicological Sciences (2013); 38(5): 655-60.
Green T1, Toghill A, Lee R, Waechter F, Weber E, Peffer R, Noakes J, Robinson M. Thiamethoxam induced mouse liver tumors and their relevance to humans. Toxicol Sci. 2005 Jul; 86(1):48-55. Epub 2005 Feb 16.
Forrester MB1. Neonicotinoid insecticide exposures reported to six poison centers in Texas Human & Experimental Toxicology (2014) Jun;33(6):568-73. doi: 10.1177/0960327114522500. Epub 2014 Feb 10.
European Food Safety Authority (EFSA) Conclusion on the peer review of the pesticide risk assessment for bees for the active substance clothianidin. Eur Food Saf Authority J. 2013;11:3066.
European Food Safety Authority (EFSA) Conclusion on the peer review of the pesticide risk assessment for bees for the active substance thiamethoxam. Eur Food Saf Authority J. 2013;11:3067.
European Food Safety Authority (EFSA) Conclusion on the peer review of the pesticide risk assessment for bees for the active substance imidacloprid. Eur Food Saf Authority J. 2013;11:3068.
Nuyttens D, Devarrewaere W, Verboven P, Foqué P. Pesticide-laden dust emission and drift from treated seeds during seed drilling: a review. Pest Manag Sci. 2013;69:564–575. doi: 10.1002/ps.3485.
Godfray HCJ, Blacquière T, Field LM, et al. A restatement of the natural science evidence base concerning neonicotinoid insecticides and insect pollinators. Proc R Soc B. 2014;281:20140558. doi: 10.1098/rspb.2014.0558
Stewart SD, Lorenz GM, Catchot AL, et al. Potential exposure of pollinators to neonicotinoid insecticides from the use of insecticide seed treatments in the mid-southern United States. Environ Sci Technol. 2014;48(9762):9769.
Godfray HCJ, Blacquière T, Field LM, et al. A restatement of the natural science evidence base concerning neonicotinoid insecticides and insect pollinators. Proc R Soc B. 2015;282:20151821. doi: 10.1098/rspb.2015.1821.
Bonmatin J-M, Giorio C, Girolami V, et al. Environmental fate and exposure; neonicotinoids and fipronil. Environ SciPollut Res. 2015;22:35–67. doi: 10.1007/s11356- 014-3332-7.
Pisa LW, Amaral-Rogers V, Belzunces LP, et al. Effects of neonicotinoids and fipronil on non-target invertebrates. Environ SciPollut Res. 2015;22:68–102. doi: 10.1007/s11356-014- 3471-x.
Gibbons D, Morrissey C, Mineau P. A review of the direct and indirect effects of neonicotinoids and fipronil on vertebrate wildlife. Environ SciPollut Res. 2015;22:103– 118. doi: 10.1007/s11356-014-3180-5.
Morrissey CA, Mineau P, Devries JH, Sánchex-Bayo F, Liess M, Cavallaro MC, Liber K. Neonicotinoid contamination of global surfacewaters and associated risk to aquatic invertebrates: a review. Environ Int. 2015;74:291–303. doi: 10.1016/j.envint.2014.10.024.
Douglas MR, Tooker JF. Large-scale deployment of seed treatments has driven rapid increase in use of neonicotinoid insecticides and preemptive pest management in U.S. field crops. Environ Sci Technol. 2015;49:5088–5097. doi: 10.1021/es506141g.
Rolke D, Persigehl M, Peters B, Sterk G, Blenau W. Large-scale monitoring of effects of clothianidin-dressed oilseed rape seeds on pollinating insects in northern Germany: residues of clothianidin in pollen, nectar and honey. Ecotoxicology. 2016;25:1691.
Todisco A. Introduzione. In Atti del Workshop “Sindrome dello spopolamento degli alveari”. Ed. V. Bellucci, 7. Roma 2008.
Kim U. Neonicotinoid Insecticides. MMG 445 Basic Biotechnology eJournal 2006.
Capelli Fausto (2002), Qualità e sicurezza dei prodotti agroalimentari nell’Unione europea, in «Alimenta», n. 9, Edizioni Scienza e Diritto, Milano.
Casnaghi Arnaldo, MAFFI Veronica, PIRANI Alberto (2006), Uno strumento in più per qualità e sicurezza, in «Largo Consumo», n. 2, Editoriale Largo Consumo, Milano.
Cassese Sabino (2002), Proposte per un’Autorità nazionale per la sicurezza alimentare, in
«Giornale di diritto amministrativo», n. 7, Ipsoa, Milano.
M. Dominicini, R. Guadagnini, D. Sciarpa, E. Ucci, Dossier 2008, Pesticidi nel piatto.
Contato Rossella (2004), Approfondiamo la conoscenza con l’EFSA di Parma, in
«Industrie alimentari», n. 12, Chiriotti Editori, Pinerolo.
Losavio C., Il consumatore di alimenti nell’Unione Europea e il suo diritto ad essere informato, Milano, Giuffrè Editore, 2007.
Losavio C., La riforma della normativa comunitaria in materia di igiene dei prodotti alimentari: il c.d. “pacchetto igiene” in «Diritto e giurisprudenza agraria e dell’ambiente», 2004.
SITOGRAFIA
- https://www.efsa.europa.eu/it/topics/topic/pesticides
- EU Pesticides Data Base – EuropeanCommission
- http://www.salute.gov.it/portale/temi/p2_4.jsp?area=fitosanitari
- http://www.salute.gov.it/portale/temi/p2_4.jsp?lingua=italiano&area=sicurezzaAlimentare
- http://www.salute.gov.it/imgs/C_17_pubblicazioni_2718_allegato.pdf
- https://anankenews.it/risvolti-neurotossici-circa-limpiego-fitofarmaci-nel-campo- agronomico-gabriella-fontecchio/
- http://www.apat.gov.it/, Greatti M. Gli insetticidi impiegati nella concia del seme di mais: effetti sulle api e dispersione nell’ambiente.
- https://ec.europa.eu/food/plant/pesticides/approval_active_substances/approval_ renewal/neonicotinoids_en
- https://www.efsa.europa.eu/en/press/news/171114
- https://www.efsa.europa.eu/en/efsajournal/pub/4610
- https://efsa.onlinelibrary.wiley.com/doi/abs/10.2903/j.efsa.2018.5177
- https://efsa.onlinelibrary.wiley.com/doi/abs/10.2903/j.efsa.2018.5178
- https://efsa.onlinelibrary.wiley.com/doi/abs/10.2903/j.efsa.2018.5179
- https://agronotizie.imagelinenetwork.com/difesa-e-diserbo/2018/05/02/ue- clothianidin-imidacloprid-e-thiametoxam-solo-in-serra-per-proteggere-le- api/58528
- https://www.efsa.europa.eu/it/press/news/180228
- https://www.efsa.europa.eu/sites/default/files/news/180228-QA-Neonics-it.pdf
- http://www.repubblica.it/ambiente/2018/04/27/news/l_ue_vieta_tre_pesticidi_ne onicotinoidi_pericolosi_per_le_api-194952866/
RINGRAZIAMENTI
Giunti alla fine di questo bel percorso formativo mi sembra doveroso ringraziare tutte le persone che nehanno preso parte.
Un sincero ringraziamento lo devoalla Prof.ssaGabriella Fontecchio per avermi dato il supporto, le competenzeoltrealla disponibilità nella realizzazione di questa tesi, nonostante i suoi mille impegni.
Ringrazio tutto il corpo docente del CLM Scienze delle Professioni Sanitarie della
Prevenzione dell’Università dell’Aquila per la loro pazienza e disponibilità.
Ringrazio i miei compagni di viaggio di questi due anni Franco, Fabio e Roberta, per tutti i momenti passati insieme, per i consigli, gli incoraggiamenti e per le nostre conversazioni.Ringrazio Francesca e Luciana per la piacevole compagnia dei nostri viaggi in auto.
Un sincero e profondo ringraziamento a mia moglieCristina e aimiei due gioielli Samuel e Nicolas, per il sostegno morale e l’amore, senza i quali non avrei materialmente potuto arrivare sin qui.
Un ringraziamento non può non andare anche a miaMadre e ai miei Suoceri che hannocondiviso con me “dall’esterno” questo cammino, esortandomi.
Per ultimo ringrazio mio Padre che da lassù sicuramente mi ha aiutato nei momenti di stanchezza.



