LA TUBERCOLOSI: UNA LUNGA STORIA-PRIMA E SECONDA PARTE-PROF.RE REMO BARNABEI
Redazione-Riproponiamo,qui di seguito, la prima e la seconda parte dell’interessantissimo intervento dell’Ill.mo Prof.re Remo Barnabei,Dirigente Biologo presso la Unità Operativa Complessa Medicina di Laboratorio-Ospedale “S. Salvatore” – L’ Aquila, sulla storia della Tubercolosi:<<
La Tubercolosi è una malattia infettiva contagiosa dovuta al batterio Mycobacterium tuberculosis; la infezione dura tutta la vita dell’ospite e determina la formazione di lesioni dette tubercoli nei polmoni ed in altre parti del corpo (rene, ossa, meningi etc.).
La Tubercolosi ha una lunga storia, almeno quanto quella del genere umano …
Per comprendere le origini della Tubercolosi è importante sapere che la Tubercolosi (nell’uomo ed in altri animali) può essere causata da diverse specie di micobatteri appartenenti al genere Mycobacterium. Mycobacterium tubercolosis provoca la maggior parte dei casi di Tubercolosi nell’uomo. Mycobacterium bovis causa la Tubercolosi bovina ed è responsabile di alcuni casi di Tubercolosi umana; anche il Mycobacterium africanum e Mycobacterium canetti possono causare Tubercolosi nell’uomo. Mycobacterium. microti, Mycobacterium caprae e Mycobacterium pinnipedii provocano la malattia in altre specie animali. Questi batteri costituiscono un raggruppamento detto Mycobacterium tubercolosis complex. Si ritiene che i batteri del genere Mycobacterium siano comparsi più di 150 milioni di anni fa, il Mycobacterium tubercolosis è una specie più giovane probabilmente comparsa 150.000 anni fa. Le prime tracce della Tubercolosi sono state trovate da Bruce Rothscild e dai suoi colleghi in un osso della zampa di un bisonte del Nord America (Wyoming) risalente (con la datazione effettuata con il Carbonio) a circa 18.000 anni fa; l’analisi del DNA indicava la presenza di batteri del genere Mycobacterium tubercolosis complex. Tracce di Tubercolosi sono state trovate nel Nord America ed in Asia nei Mastodonti, ancestori degli elefanti moderni, estintisi circa 11.000 anni fa; la Tubercolosi potrebbe aver contribuito alla loro estinzione. Le prime tracce sicure di Tubercolosi nell’uomo sono state trovate nei resti dello scheletro di una madre e del suo bambino rinvenuti in un sito preistorico sommerso chiamato Atlit-Yam, posto lungo la costa mediterranea dello Stato di Israele, a circa 200-400 m dalla linea di spiaggia e ad una profondità variabile tra gli 8 e i 12 m sotto il livello del mare. La coppia viveva in un villaggio del periodo Neolitico risalente a 8.000-9.000 anni fa, uno dei primi insediamenti in cui si allevavano animali e veniva praticata l’agricoltura. Sia la madre che il bambino presentano lesioni suggestive di tubercolosi nello scheletro e usando tecniche estremamente sofisticate e specifiche i ricercatori hanno riscontrato nelle costole, nelle braccia e nelle ossa lunghe di entrambi DNA batterico di Mycobacterium tubercolosis.
La scoperta di ossa con deformazioni riferibili alla infezione da Mycobacterium in vari siti del Neolitico in Italia, Danimarca e in regioni del Medio Oriente fa supporre che lo “spread” (la diffusione) della Tubercolosi nel mondo si sia avuto circa 4.000 anni fa. Si ritiene che batteri del genere Mycobacterium, inizialmente viventi, come altri batteri del genere Actinomycetes, nel suolo, si siano evolute per vivere nei Mammiferi. L’addomesticamento dei bovini sembra risalga a 10.000-25.000 anni fa potrebbe aver favorito il passaggio di Mycobacterium patogeni dai bovini all’uomo. Si ritiene che Mycobacterium bovis, che provoca una malattia simil-tubercolosi nei bovini, sia il precursore di Mycobacterium tubercolosis.
La Tubercolosi era una malattia comune nell’antico Egitto; DNA di Micobatteri è stato ritrovato in uno scheletro risalente a 5.400 anni fa. In uno studio su 85 mummie trovate nei siti archeologici di Tebe e datate tra il 2050 ed il 500 a.C., si è riusciti a tipizzare i diversi Mycobatteri presenti. Oltre alle tracce di DNA, in alcune mummie egiziane del 2.400 a.C. sono state osservate lesioni dello scheletro caratteristiche della Tubercolosi ossea (morbo di Pott). Lesioni caratteristiche della spondilite tubercolare sono state riscontrate in una mummia di bambino peruviano risalente allo stesso periodo: la Tubercolosi era quindi presente nel Sud America ancor prima della colonizzazione europea. Fig. 1 e 2. L’ articolo pubblicato sull’ International Journal of Tuberculosis and Lung Disease dal titolo: “The origins and precolonial epidemiology of tuberculosis in the Americas: can we figure them out?” spiega che le Americhe furono popolate da migranti asiatici in due più importanti migrazioni: la prima intorno a 20.000 anni fa e l’altra intorno ai 12.000-11.000 anni fa. La Tubercolosi quindi colonizzò le Americhe attraverso queste ondate migratorie persistendo a bassi livelli di endemicità in piccoli, dispersi gruppi di popolazioni. A partire da 1.500 anni fa iniziò una epidemia di Tubercolosi a partire probabilmente dalla regione delle Ande; questa epidemia durò poco tempo ed era finita prima dell’arrivo dei colonizzatori europei, lasciando una popolazione autoctona suscettibile alla reinfezione da Micobatteri “europei”.

Fig. 1: A. Mummia di un neonato maschio risalente al 1250-500 a.C. circa; dopo l’apertura della parete toracica sottili aderenze della pleura del polmone indicavano una infezione tubercolare.
B. Omero destro da una mummia risalente al 2050-500 a.C. circa; l’osso mostra alterazioni morfologiche probabilmente dovute ad infiammazioni aspecifiche; alla estremità distale sono visibili una neoformazione di osso e una lesione fistolare (freccia).

 Da campioni ottenuti da tessuti molli o da ossa la tecnica Polimerase Chain Reaction ha dimostrato presenza del DNA di Micobatteri (M. tuberculosis, M. bovis, M. africanum
Da campioni ottenuti da tessuti molli o da ossa la tecnica Polimerase Chain Reaction ha dimostrato presenza del DNA di Micobatteri (M. tuberculosis, M. bovis, M. africanum
Fig. 2: spondilite tubercolare (morbo di Pott) in mummia egiziana (a sinistra) e in mummia peruviana (a destra)
L’Africa è stata la culla e la madre della specie umana e del suo inseparabile compagno di viaggio: il Mycobacterium tubercolosis. Tracce di leptomeningite tubercolare sono state riscontrate su ossa craniche di Homo erectus risalenti a circa 500.000 anni a. C. (Fig. 3).



Fig. 3: Migrazione dell’Homo erectus dal centro-Africa verso aree più calde.
La suscettibilità alla infezione tubercolare sarebbe dovuta ai modesti valori di Vitamina D presenti negli esseri umani adattati ai climi tropicali e poi successivamente migrati in regioni più fredde, come dall’ Africa centrale alla odierna Turchia nel caso dell’Homo erectus. La vitamina D permetterebbe infatti la attivazione dei Linfociti T (gli organizzatori delle difese immunitarie) potenziando le difese contro Mycobacterium tubercolosis. (Von Essen MR et Al., Vitamini D controls T cell antigen receptor signaling and activation of Human T cells. Nat. Immunol. 2010; 11: 344-9).
La tubercolosi agisce e si propaga per secoli; ci sono tracce abbastanza sicure del suo passaggio.
La malattia è stata conosciuta nelle varie epoche storiche con varie denominazioni: “consunzione”,consumptione (latino), “tisi” da “phthisis” (parola greca per consunzione), yoksma (India), chaky oncay (inca), “mal sottile”, “scrofula”(negli adulti), che colpiva il sistema linfatico e provocava il gonfiore delle ghiandole del collo, “malattia del deperimento”, “peste bianca” poiché le vittime avevano un aspetto pallido, “male del re”, perché era credenza popolare che il tocco di un re potesse curare la scrofula e “malattia di Pott” o “gobba” per la tubercolosi ossea. Ovviamente la causa della tubercolosi era sconosciuta, ma i suoi sintomi devastanti erano sufficientemente noti. Come già detto la tubercolosi era una malattia abbastanza diffusa nell’ antico Egitto, sembra probabile che Akhenaten e sua moglie Nefertiti morirono entrambi di tubercolosi, e alcune prove indicano che esistevano in Egitto, già nel 1500 a.C. ospedali per la tubercolosi. I Papiri di Ebers, un importante trattato di medicina egizia del 1550 a.C., descrivono una tubercolosi polmonare associata a linfonodi cervicali. Si raccomandava di curarla con l’incisione chirurgica della cisti e l’applicazione di un miscuglio di acacia seyal, piselli, frutti, sangue di animali e di insetti, miele e sale. La prima descrizione scientifica di sintomi riferibili alla Tubercolosi si trova in un testo cinese di 4.000 anni fa, descrive una sorta di “febbre polmonare” e una “tosse polmonare”. Altri documenti scritti che descrivono la malattia risalgono a 3.300 anni fa e a 2.300 anni fa, trovati rispettivamente in India e in Cina. Altri documenti scritti relativi alla Tubercolosi sono connessi all’ Ebraismo; il termine dell’ebraico antico “schachepheth” (consunzione) si trova nei testi biblici del Deuteronomio e del Levitico.
“ecco che cosa farò a voi a mia volta: manderò contro di voi il terrore, la consunzione e la febbre, che vi faranno languire gli occhi e vi consumeranno la vita.”
Levitico 26: 16.
“Il Signore ti colpirà con la consunzione, con la febbre, con l’infiammazione, con l’arsura, con la siccità, il carbonchio e la ruggine, che ti perseguiteranno finché tu non sia perito”
Deuteronomio 28: 22.
 Gli antichi Greci conoscevano bene la malattia, che chiamavano “phtisis”. Ippocrate di Coo (Coo, 460 a.C. circa – Larissa, 377 a.C) ha descritto la phtisis come una malattia mortale specialmente nei giovani adulti, ha definito i suoi sintomi e le lesioni tubercolari caratteristiche a livello dei polmoni. Sorprendenti le scoperte dei primi scienziati greci: Isocrate (IV secolo a.C.) per primo ipotizza che la Tubercolosi sia una malattia infettiva e Aristotele suggerisce la natura contagiosa della scrofola nei maiali e nei bovini. In epoca romana la malattia viene descritta da Cornelio Celso, Areteo di Cappadocia e Celio Aureliano, ma gli autori dell’età classica non arrivarono a comprendere che anche la scrofola, il morbo di Pott, il lupus tubercolare, tutte manifestazioni extrapolmonari della malattia, fossero da ascrivere ad un unico agente morboso. In quello che viene considerato il primo trattato completo di medicina in latino: il “De Re Medica” di Aulo Cornelio Celso (in latino: Aulus Cornelius Celsus; 14 a.C. circa – 37 d.C. circa), rimasto pressoché ignoto durante il Medioevo e riscoperto tra il 1425 e il 1427 e pubblicato a stampa per la prima volta nel 1478 (Fig. 4), viene citata la frase “…ex hoc febricula levis fit, quae etiam quievit tamen repetit; frequens tussis est….” cioè “da questa (malattia) deriva una febbricola, che anche se si spegne facilmente, tuttavia subito dopo riprende vigore; la tosse poi è frequente in questi malati…”. Quindi la tubercolosi viene inquadrata come malattia già intorno primo secolo d.C. Tra i medici bizantini Alessandro di Tralles, Ezio di Amida e Paolo di Egina, descrivono nei loro trattati le forme polmonari e a quelle ghiandolari (scrofola) della tubercolosi. Secondo il famoso Galeno, che divenne medico personale dell’imperatore Marco Aurelio nel 174 d.C. i sintomi della Tubercolosi sono: febbre, sudore, tosse ed espettorato venato di sangue e la terapia raccomandata è aria fresca, latte e viaggi in mare. Fig. 4: il “De Re Medica” di Aulo Cornelio Celso
Gli antichi Greci conoscevano bene la malattia, che chiamavano “phtisis”. Ippocrate di Coo (Coo, 460 a.C. circa – Larissa, 377 a.C) ha descritto la phtisis come una malattia mortale specialmente nei giovani adulti, ha definito i suoi sintomi e le lesioni tubercolari caratteristiche a livello dei polmoni. Sorprendenti le scoperte dei primi scienziati greci: Isocrate (IV secolo a.C.) per primo ipotizza che la Tubercolosi sia una malattia infettiva e Aristotele suggerisce la natura contagiosa della scrofola nei maiali e nei bovini. In epoca romana la malattia viene descritta da Cornelio Celso, Areteo di Cappadocia e Celio Aureliano, ma gli autori dell’età classica non arrivarono a comprendere che anche la scrofola, il morbo di Pott, il lupus tubercolare, tutte manifestazioni extrapolmonari della malattia, fossero da ascrivere ad un unico agente morboso. In quello che viene considerato il primo trattato completo di medicina in latino: il “De Re Medica” di Aulo Cornelio Celso (in latino: Aulus Cornelius Celsus; 14 a.C. circa – 37 d.C. circa), rimasto pressoché ignoto durante il Medioevo e riscoperto tra il 1425 e il 1427 e pubblicato a stampa per la prima volta nel 1478 (Fig. 4), viene citata la frase “…ex hoc febricula levis fit, quae etiam quievit tamen repetit; frequens tussis est….” cioè “da questa (malattia) deriva una febbricola, che anche se si spegne facilmente, tuttavia subito dopo riprende vigore; la tosse poi è frequente in questi malati…”. Quindi la tubercolosi viene inquadrata come malattia già intorno primo secolo d.C. Tra i medici bizantini Alessandro di Tralles, Ezio di Amida e Paolo di Egina, descrivono nei loro trattati le forme polmonari e a quelle ghiandolari (scrofola) della tubercolosi. Secondo il famoso Galeno, che divenne medico personale dell’imperatore Marco Aurelio nel 174 d.C. i sintomi della Tubercolosi sono: febbre, sudore, tosse ed espettorato venato di sangue e la terapia raccomandata è aria fresca, latte e viaggi in mare. Fig. 4: il “De Re Medica” di Aulo Cornelio Celso
 La Tubercolosi comunque, secondo il medico greco, era una malattia incurabile e contagiosa.
La Tubercolosi comunque, secondo il medico greco, era una malattia incurabile e contagiosa.
Tra gli Arabi, Avicenna parla della tubercolosi come di una malattia ”ulcerosa, escavante e consuntiva”, ed esprime il sospetto che la tisi sia una malattia contagiosa.
Non si hanno dati certi sulla epidemiologia della Tubercolosi fino al XIX secolo, sappiamo invece che la sua forma linfo-adenitica, la Scrofola, doveva avere una frequenza di comparsa molto elevata. La scrofola, malattia di natura tubercolare caratterizzata da ingrossamenti ghiandolari tendenti alla suppurazione, colpiva e colpì fino a tempi abbastanza recenti soprattutto la popolazione infantile. Conosciuta fin dall’antichità come malattia affine alla tisi polmonare, essa venne curata per secoli con il rito della “toccatura” effettuata dalla mano del re. Questo era il motivo del nome “morbo regio“ assegnatole da Gilbertus Anglicus che aveva studiato a Salerno tra il 1180 e il 1190, abbandonando successivamente gli studi Salernitani per seguire Riccardo Cuor di Leone nella Crociata. Nel capitolo “De scrofolis et glandulis” del suo Compendium Medicinae egli scrive “morbus regius quia reges hunc morbum curant”. La scrofola era anche chiamata “the King’s Evil” (“il male del re” in lingua inglese). Si pensava che i sovrani inglesi avessero ereditato la capacità di guarire la malattia grazie alla loro discendenza da Edoardo il Confessore, re inglese dal 1042 al 1066, che, in base a talune leggende, lo aveva ereditato da San Remigio. L’ultimo esempio di pubblico “tocco” della scrofola fu il 31 maggio 1825 ad opera di Carlo X, tra la generale incredulità e derisione. Tillemont (Parigi, 1849), così descrive la cerimonia nella vita di S. Luigi Re di Francia:”Il Re dopo essersi preparato con digiuni e preghiere, dopo essersi accostato al S. Sacramento e avere venerato per tre giorni l’arca di S. Marcolfo a Corvigny, riceveva i malati che sfilavano innanzi a lui. Indi poneva le dita sulla glandola scrofolosa e la benediceva col segno della Santa Croce, pronunziando le parole di Nostro Signore:” Le Roi te touche et Dieu te guerit” (Fig. 5). Nel Regno di Sicilia invece, secondo i dettami della Scuola medica salernitana, la si curava semplicemente con impiastri di fico. Si narra che nel 1775 Luigi XVI, in occasione della sua incoronazione avesse toccato 2400 malati e che nel 1824 l’ultimo dei sovrani di Francia, Carlo X, per celebrare la sua incoronazione, avesse toccato 121 malati, propostigli addirittura da due illustri chirurghi come Alibert e Dupuytren.
Fig. 5: la imposizione delle mani da parte di Del Re di Francia (Enrico IV) sui malati di scrofola.
Ma se volessimo fare una statistica dei casi di tubercolosi ghiandolare sulla base del numero delle persone “toccate” dai diversi re di Francia da Francesco I (che nel 1528-30 toccò 1806 malati) in poi, non avremmo un quadro reale della epidemiologia di questa manifestazione morbosa, perché l’accorrere dei malati dal re per farsi toccare era viziato in eccesso dal fatto che al “tocco” faceva seguito un’elemosina.
Anche in mancanza di dati epidemiologici precisi è nota l’epidemia di tubercolosi in Europa, che probabilmente iniziò nel diciassettesimo secolo e che durò duecento anni; era nota come la Grande Piaga Bianca forse per distinguerla dalla Peste bubbonica (la Morte Nera). Nel 1650 la tubercolosi era la principale causa di morte e morire di tubercolosi era considerato inevitabile. L’alta densità della popolazione e le condizioni sanitarie indigenti che caratterizzavano molte città dell’Europa e del Nord America crearono un ambiente idoneo alla diffusione del morbo. Dal 1600 al 1800 la Tubercolosi causò il 25% di tutte le morti. Data la grande diffusione della malattia venivano tentate pratiche mediche più corrispondenti alle necessità del caso, almeno nella misura che le conoscenze scientifiche dell’epoca consentivano. Infatti già Paolo d’Egina, medico bizantino (625-690 dC.) del quale gli Arabi riconoscevano la sua abilità in ginecologia e ostetricia (e ciò gli valse l’appellativo di “al-Tawalīd”, l’Ostetrico) consigliava l’asportazione chirurgica delle ghiandole malate avendo cura di non ledere vasi o nervi di cui la regione del collo è ricca. Invece la Scuola Salernitana, forse perché non all’altezza di proporre delicati interventi chirurgici, preferiva consigliare cure locali a base di bile porcina oppure cataplasmi di fichi.
Il famoso chirurgo della Scuola bolognese Teodorico da Lucca era favorevole alla asportazione chirurgica delle ghiandole scrofolose, ma solo se suppurate, per medicarle poi con albume d’uovo, mentre sconsigliava l’asportazione di quelle non suppurate per la sua pericolosità, a meno che questa non fosse eseguita da mani esperte.
Il famoso chirurgo francese Guy de Chauliac, pur non disdegnando, in ossequio al re, di cui era medico personale, la pratica della “toccatura“ reale, era decisamente favorevole all’asportazione della ghiandola con una incisione “a foglia di mirto”. Bisogna attendere il XVI secolo per avere una chiara definizione della tubercolosi come malattia contagiosa.
Fu Girolamo Fracastoro, padre della “dottrina del contagio”, ad impegnarsi in tal senso. La diffusione di questa notizia creò panico fra la gente che prese a trattare gli scrofolosi e i tisici alla stessa stregua dei lebbrosi. Nel 1699 il consiglio di sanità della repubblica di Lucca dispose la denuncia obbligatoria “delle persone di qualsivoglia sesso e condizione affette da etisia” e nel 1735 dispose l’isolamento e la cura dei tisici, ma ne vietò il ricovero negli ospedali comuni, istituendo luoghi di cura per il loro isolamento. Nel 1753 a Firenze, fu addirittura promulgata una legge che privava quei poveretti di tutti i loro diritti.
Franciscus de La Boe (1614-1672), comunemente noto come Sylvius, nel 1671 descrisse i tubercoli polmonari riconoscendovi la stessa natura delle scrofole e attribuì la tisi alla suppurazione dei tubercoli nel parenchima polmonare, con la formazione delle caverne. Nel 18° secolo in Europa occidentale la Tubercolosi divenne epidemica con un tasso di mortalità elevato (900 morti ogni 100.000 abitanti) soprattutto fra i giovani per cui la malattia veniva definita “il ladro di giovani”. Pott sul finire del XVIII secolo (1779-1782) descrisse la malattia che da lui prese il nome senza però riconoscerne l’esatta eziologia. Nel 1793 il patologo scozzese Matthew Baille denominò “tubercoli” gli ascessi della tisi, caratterizzati dalla necrosi caseosa (“cheese-like”).
Nel 1761 Leopold Auenbrugger col suo trattato sulla percussione “Inventum novum” schiuse nuovi orizzonti alla semeiologia fisica del torace.
Infine nel 1783 Baumes pubblicò il “Traité de la phtisie pulmonaire” che è la summa di tutte le conoscenze sulla tubercolosi fino a lui.
Un particolare fervore di studi sulla tubercolosi si ebbe nel XVII e nel XVIII secolo in Inghilterra a causa dei numerosi casi della malattia presenti su quel territorio e vi contribuirono autori come Willis, Morton, Marten, per citarne solo alcuni. Non vanno dimenticati i notevoli contributi dati da G. B. Morgagni, il quale descrisse le lesioni tubercolari in via di caseificazione.
Nel 1810 Bayle per primo distinse diverse entità anatomo-patologiche, descrivendo la presenza di tubercoli in altri organi diversi dal polmone, parlando della forma diffusa a tutto l’organismo o “tubercolosi miliare” riconoscendo la tubercolosi come malattia generalizzata. La “tubercolosi miliare” probabilmente era più diffusa rispetto ai nostri giorni, come evidenziato già nel “seicento” dal famoso anatomico Thomas Willis (1621-1675). Nel XIX secolo la tubercolosi fu soprannominata oltre che “Piaga Bianca”, anche “male di vivere”, e “male del secolo”. Era vista come una “malattia romantica”. Si pensava che soffrire di Tubercolosi concedesse al malato una sensibilità nascosta. La lenta progressione della malattia permetteva una “buona morte” consentendo alle vittime di mettere ordine nei loro affari. La malattia cominciò a rappresentare la purezza spirituale e la salute terrena, portando molte giovani donne del ceto alto ad impallidire volutamente il loro viso per avere un aspetto malato. Il poeta britannico Lord Byron scrisse nel 1828,”mi piacerebbe morire di tubercolosi”, aiutando a far divenire popolare questa malattia come la malattia degli artisti. George Sand amava ciecamente la sua “tisica” amante, Fryderyk Chopin, lo chiamò il suo “povero melanconico angelo”. In Francia, furono pubblicate più di cinque novelle in cui si narravano gli ideali della Tubercolosi: “La signora delle camelie” di Dumas figlio, “Scene de la vie de bohème” di Murger,” Les miserables” di Victor Hugo, “Madame Gervaisais” e “Germinie Lacerteux” dei fratelli Goncourt e “L’aiglon” di Edmond Rostand. In letteratura la prospettiva della malattia spirituale e che redime continuò anche dopo che furono accumulate conoscenze mediche della malattia. Accanto alla visione “romantica” ottocentesca delle classi sociali elevate, le fasce più povere della popolazione in Europa subirono gli effetti devastanti della malattia. Si stima che la tubercolosi abbia raggiunto il picco della prevalenza tra la fine del diciottesimo secolo e il diciannovesimo. Una giornata lavorativa di almeno 12 ore con un solo giorno di riposo alla settimana, il consumo di alimenti scadenti con abbondanti dosi di alcool, la condizione di semi povertà di gran parte del proletariato urbano, unite alla visione di un capitalismo senza freni inibitori, queste sono le condizioni che provocarono il passaggio della Tubercolosi da endemica ad epidemica e pandemica nel Regno unito tra la fine del XVIII e l’inizio del XIX secolo. Cristóbal Rojas (1886) affetto da tubercolosi, dipinge gli aspetti sociali della malattia e la sua  relazione con le condizioni di vita alla fine del diciannovesimo secolo (Fig. 9).
relazione con le condizioni di vita alla fine del diciannovesimo secolo (Fig. 9).
Fig. 9: Cristóbal Rojas – La Miseria
Sempre nel XIX secolo nasce il mito del Sanatorio come luogo di purificazione, legato a tematiche culturali complesse e filosofiche ed antropologiche profonde: “… il risiedere su di un versante della montagna, pervaso da aria purissima è la condizione necessaria perché si realizzi un vero e proprio ritorno all’infanzia …” Carl Gustav Jung (Repertorio della realtà simbolica). I Sanatori fioriscono in tutto il Mondo Occidentale, assumendo la consistenza di vere e proprie Città della Malattia, in cui vigono regole e norme specifiche sociali e di convivenza. Il primo in assoluto fu opera di un medico tedesco dalla vita avventurosa, di nome Hermann Brehmer (1826 –1889), nato nella cittadina oggi polacca di Strzelin (Strehlen), in Slesia (Fig. 10).

Fig. 10: Il primo sanatorio aperto da Hermann Brehmer a Görbersdorf, oggi Sokołowsko in Polonia, nel 1859 e ad un’altitudine di circa 550 m. s. l. m.
Il XIX secolo fu ricco di dibattiti attorno alla natura del tubercolo e all’inquadramento nosografico della tubercolosi. Mentre il francese Laennec nel 1819 dava un inquadramento nosografico unitario della malattia, per contro il suo avversario Broussais considerava i tubercoli come il risultato di una reazione infiammatoria, perciò non un prodotto specifico.
Louis, supportato da 167 autopsie, dimostrò che i tubercoli erano veramente una produzione specifica, dove l’infiammazione aveva solo un ruolo accessorio. Tuttavia Virchow negò la natura specifica del tubercolo e per l’autorità scientifica che rivestiva e la credibilità che ne derivava, con questa sua presa di posizione ritardò l’accettazione di una concezione unitaria della tubercolosi secondo quanto aveva affermato Laennec. Non mancarono coloro che credettero nel carattere ereditario della malattia, come Linneo (1740), il quale sostenne però anche che la tisi polmonare è causata “da un vero invisibile germe di contagio”.
Giacinto Laennec (1781-1826), sotto l’aspetto diagnostico, perfezionava quel metodo della percussione toracica che era già stato proposto da G. L. Auenbrugger nel 1761 e da G. N. Corvisart nei primi anni dell’800, dividendo il torace in quindici regioni, questo consentiva una più precisa definizione degli organi toracici e delle loro patologie. Un ulteriore passo in avanti nella semeiotica toracica fu fatto da Laennec quando inventò il metodo dell’auscultazione mediata con lo stetoscopio, affinando ancora di più la semeiologia degli organi toracici.
La convinzione che la tubercolosi fosse una malattia contagiosa trovava sempre maggiori consensi e a Napoli, nel 1782, Domenico Cotugno sollecitò per questo motivo la promulgazione di una legge sanitaria per la profilassi sociale della malattia, ma due anni dopo re Ferdinando di Napoli, che rifiutava l’idea della contagiosità della tisi, revocò alcune delle disposizioni cautelative già fatte approvare da Cotugno. I termini consunzione e tisi continuarone ad essere usati entrambi nei XVII e il XVIII secolo fino alla metà del XIX secolo, quando Johann Lukas Schönlein introdusse il termine “tuberculosis”.
Fu necessario attendere la seconda metà del XIX secolo per entrare nella fase sperimentale della malattia in modo di poterne capire tutti gli aspetti etiopatogenetici e epidemiologici e Jean Antoine Villemin ne fu il pioniere. Il 5 dicembre 1865 Villemin comunicò all’Accademia di Francia che la tubercolosi è effetto di un agente causale specifico, da lui chiamato ”virus”, con dati sperimentali alla mano. Egli aveva infatti inoculato nel coniglio materiale tubercolare (caseum, escreato, pus linfonodale) di origine umana o animale, ottenendo nell’animale, dopo alcune settimane, lesioni tubercolari. Da ciò dedusse la specificità della malattia e che essa fosse dovuta ad un agente inoculabile.
Villemin pubblicherà nel 1868 a Parigi il risultato delle sue ricerche in “Etudes sur la tubercolose. Preuves rationelles et expérimetales de sa spécifité e de son inoculabilité”.
In questa sua pubblicazione Villemin aggiunse anche considerazioni di carattere epidemiologico facendo notare che la tubercolosi era più frequente negli agglomerati urbani più affollati e che nelle regioni indenni come la Nuova Zelanda, l’Australia, l’Oceania essa fosse comparsa con la colonizzazione europea provocando vere e proprie stragi, aprendo così un capitolo nuovo, quello dell’aspetto sociale della malattia. Le conclusioni sperimentali di Villemin furono confermate anche da altri studiosi come Chaveaux, Klebs e Grancher, ma restava il problema, fino ad allora insoluto, dell’isolamento dell’agente causale non ancora identificato, anche se intuito.
La consapevolezza che la tubercolosi fosse una malattia dipendente anche dalle cattive condizioni ambientali della popolazione e la convinzione che l’aria salso-iodica del mare avesse benefici effetti sull’andamento delle forme ghiandolari tubercolari di tipo scrofoloso, indusse Giuseppe Barellai a fondare a Viareggio il primo ospizio italiano per bambini scrofolosi, nel 1862.
Un notevole passo in vanti nella patogenesi della malattia venne fatto da Jules Parrot, che nel 1878 enunciò la Legge delle adenopatie ilari nella prima infezione, secondo la quale tutte le volte che un ganglio bronchiale è la sede di una lesione tubercolare ad essa corrisponde una lesione analoga nel polmone. Soltanto nel 1912 l’austriaco Ghon verrà a parlare del “complesso primario”. Robert Koch fu colui che riuscì ad isolare il bacillo tubercolare. Egli usò la colorazione con blu di metilene consigliata da Ehrlich, lo identificò, lo isolò e lo coltivò in siero animale; infine lo inoculò in animali da laboratorio riproducendo la malattia, ottenendo un risultato inoppugnabile.
Il 24 marzo 1882 Robert Koch (1843-1910) comunicò alla Società di fisiologia di Berlino di aver scoperto il microrganismo responsabile della letale Tubercolosi polmonare, che denominò due settimane più tardi, nella rivista scientifica “Berliner Klinische Wochenscrift”, “Tuberkelvirus” (cioè virus della Tubercolosi) e descrisse questo microrganismo come ”Sottile, la cui lunghezza è metà-un quarto del diametro di un globulo rosso, molto simile al bacillo della lebbra, ma più affilato” (Fig. 6). Questi primi microrganismi isolati da R. Koch in lesioni polmonari sono esposti all’ “Hunterian Museum” nel Royal College of Surgeons di Londra.
Robert Koch fu insignito del Premio Nobel nel 1905.

 Fig. 6: la pubblicazione del 1882 di R. Koch sulla eziologia della Tubercolosi e il Dr. Koch al microscopio nel suo Laboratorio di Microbiologia.
Fig. 6: la pubblicazione del 1882 di R. Koch sulla eziologia della Tubercolosi e il Dr. Koch al microscopio nel suo Laboratorio di Microbiologia.
Robert Koch, nato a Claustal, nel nord-est della Germania, si era laureato in medicina “cum extrema lauda” nella Università di Göttingen ma aveva una grande passione per le scienze naturali, passione che mantenne nella sua vita professionale di medico. Nella Università di Göttingen era stato allievo di famosi medici e scienziati quali Jacob Henle, George Meissner, Friedrich Wöhler, Wilelm Krause. Mentre era ancora studente aveva conseguito un premio di ricerca per i suoi studi sulla innervazione dell’utero; questo gli aveva consentito di incontrare il famoso medico tedesco Rudolf Virchow. La passione per le scienze naturali fu alimentata dal dono di sua moglie: un microscopio. Nel 1875 visitò molti grandi centri scientifici in Germania e fu conquistato dal nascente mondo della microbiologia; Louis Pasteur aveva infatti dimostrato che i batteri causavano la putrefazione della sostanza organica, Joseph Lister aveva sviluppato tecniche antisettiche per la chirurgia e il suo professore di anatomia a Göttingen, Jacob Henle, era un estremo difensore della idea del “contagium animatum” cioè che le malattie potevano essere causate da agenti viventi trasmissibili. La “teoria dei germi” era ancora aspramente discussa ed il ruolo dei batteri nelle malattie infettive era ancora incerto. Dopo la guerra franco-prussiana, alla quale aveva partecipato come ufficiale medico, si trasferì a Wöllstein, nella odierna Polonia, dove esercitò la pratica clinica ma si occupò del più grave problema di salute pubblica del tempo: il carbonchio o antrace. Infatti, nella regione di Wöllstein, in 4 anni la malattia aveva ucciso 528 persone e 56.000 capi di bestiame. Alcuni studi avevano dimostrato che batteri a forma di bastoncello erano presenti nel sangue degli animali malati e che la malattia poteva essere trasmessa inoculando il sangue degli animali malati in animali sani. Inoltre si sapeva che alcuni pascoli erano “pericolosi” per il bestiame che vi pascolava. Koch, attraverso complessi studi di inoculazione usando topi, cavie, conigli, cani, rane ed uccelli. Koch, inoltre sviluppò tecniche di coltivazione dei batteri “in vitro” e raffinate tecniche di osservazione al microscopio che gli permisero di individuare le “spore” del carbonchio, cioè le forme di resistenza del batterio che venivano disseminate dagli animali infetti nell’ambiente e che potevano infettare gli animali a l’uomo provocando la malattia. Sebbene la “teoria dei germi” quali causa di malattie fosse stata già accettata Koch, fu il primo a collegare uno specifico batterio ad una specifica malattia. Nel suo improvvisato laboratorio di casa aveva chiarito il ciclo vitale del batterio del carbonchio  disegnando ciò che osservava al microscopio (Fig. 7).
disegnando ciò che osservava al microscopio (Fig. 7).
Fig. 7: Disegno eseguito da R. Koch. Sono illustrate vari stadi del ciclo vitale del Clostridium anthracis (Bacillus anthracis).
 Koch presentò i suoi esperimenti al famoso botanico tedesco Ferdinand Cohn che ne fu molto impressionato e che pubblicò nel 1876 il lavoro di Koch sulla sua rivista di botanica. Era iniziata l’età dell’oro della batteriologia ed era iniziato il forte impatto di essa nella medicina. Koch migliorò la tecnica della microscopia attraverso la introduzione di tecniche di “fissaggio” dei preparati, l’uso dei derivati dell’anilina – eosina, safranina, violetto di metile – per la colorazione dei batteri, la tecnica della immersione degli obiettivi in olio, l’uso del “condensatore” della fonte di luce. Fu il primo a fotografare i batteri; le prime fotografie di batteri furono pubblicate nel 1877 (Fig. 8).
Koch presentò i suoi esperimenti al famoso botanico tedesco Ferdinand Cohn che ne fu molto impressionato e che pubblicò nel 1876 il lavoro di Koch sulla sua rivista di botanica. Era iniziata l’età dell’oro della batteriologia ed era iniziato il forte impatto di essa nella medicina. Koch migliorò la tecnica della microscopia attraverso la introduzione di tecniche di “fissaggio” dei preparati, l’uso dei derivati dell’anilina – eosina, safranina, violetto di metile – per la colorazione dei batteri, la tecnica della immersione degli obiettivi in olio, l’uso del “condensatore” della fonte di luce. Fu il primo a fotografare i batteri; le prime fotografie di batteri furono pubblicate nel 1877 (Fig. 8).
Fig. 8: apparecchio fotografico montato su microscopio utilizzato da Koch per fotografare i preparati.
Oltre alle tecniche microscopiche Koch si interessò della “coltivazione” dei batteri “in vitro” sviluppando la tecnica della coltivazione dei batteri su terreni di coltura solidificabili che consentivano di ottenere colture “pure”, cioè di far crescere una sola specie batterica; questo fu uno dei più grandi contributi alla nascente scienza della batteriologia. Sospettando che la tubercolosi fosse causata da batteri resistenti alle tecniche di colorazione convenzionali, Koch sperimentò nuove colorazioni. Usando la colorazione messa a punto da Paul Ehrlich al Blu di metilene evidenziò pochi piccoli bastoncelli nel tessuto dei tubercoli, ma quando aggiunse un colorante di contrasto marrone per avere un maggior contrasto fotografico osservò un maggior numero di batteri nello stesso preparato. Migliorò la colorazione alcalinizzando le soluzioni di blu di metilene e riuscì così ad osservare con relativa facilità i batteri tubercolari nell’ espettorato e nelle cavità polmonari dei soggetti con tubercolosi. Con prove di inoculazione di espettorato contenente batteri riuscì a indurre malattia nelle cavie sane e concluse che l’espettorato era la principale fonte di trasmissione della malattia e che i soggetti affetti da tubercolosi laringea o polmonare che emettevano grandi quantità di batteri erano particolarmente infettivi. Dimostrò che l’espettorato contenente batteri anche dopo l’essiccamento poteva mantenere la sua patogenicità. Koch lavorò per proteggere le comunità attraverso efficaci misure igieniche come la eliminazione appropriata degli espettorati infetti e la decontaminazione degli ambienti dove soggiornavano i malati, la sterilizzazione dei vestiti e delle lenzuola; fu vietato espettorare nei luoghi pubblici. Grazie agli studi e alle raccomandazioni di Koch la Tubercolosi fu considerato un problema di salute pubblica che richiedeva misure di prevenzione della sua trasmissione. Dopo la sua famosa lettura di Berlino Koch, ormai famoso, ebbe l’incarico dal governo tedesco, preoccupato di una possibile pandemia di colera, di guidare una spedizione scientifica in Egitto. Anche per il colera riuscì a dimostrare la natura infettiva della malattia, isolando il batterio che la causava: il Vibrio colerae, un batterio a “forma di virgola” presente nelle acque contaminate da feci di soggetti infetti. Dopo la esperienza in Egitto si recò a Calcutta; anche in India si avevano epidemie di colera. Anche qui i meticolosi studi epidemiologici di Koch confermarono che i batteri a “forma di virgola” erano responsabili della malattia. Al suo ritorno dall’India Koch ricevette gli onori da parte del Kaiser Guglielmo primo e dal Cancelliere tedesco Otto von Bismarck; fu nominato Professore di Igiene nell’ Università di Berlino e Direttore dell’Istituto di Igiene.
La Tubercolina
Nel 1980 Koch iniziò a cercare una cura per la Tubercolosi. Lavorando nel suo Laboratorio Robert Koch descrisse un fenomeno che da lui prende il nome. Koch osservò che l’iniezione di bacilli tubercolari in una cavia sana, ossia una cavia che non era mai venuta in contatto con l’agente della Tubercolosi prima di allora determinava, dopo un periodo di incubazione di 10-14 giorni, un nodulo che successivamente si ulcerava e dal quale i bacilli si diffondevano per tutto l’organismo. Al contrario, una seconda iniezione di bacilli tubercolari in una cavia che fosse già stata infettata 4-6 settimane prima, determinava anch’essa la formazione di un nodulo. Rispetto alla prima iniezione, tuttavia, il nodulo compariva più velocemente, dopo soli 1-2 giorni (che era indizio di una reazione di ipersensibilità), e non si ulcerava, ma rimaneva localizzato e tendeva a guarire (il che era indizio di immunità acquisita). La reazione osservata in seguito alla seconda iniezione di bacilli è nota come “fenomeno di Koch”. Koch scoprì che le reazioni osservate dopo l’iniezione di bacilli nella cavia tubercolotica (nodulo precoce e localizzato) si osservavano anche se venivano inoculati bacilli morti o estratti di bacilli. In particolare, si osservavano con estratti glicerinati di colture di vari ceppi di Mycobacterium tuberculosis, preparati a caldo e sterilizzati, da cui si otteneva un liquido vischioso e di colore bruno a cui Koch diede il nome di “tubercolina“. In seguito vennero ideati altri metodi per produrre sostanze con le caratteristiche della tubercolina di Koch. La tubercolina estratta con la procedura di Koch viene definita “tubercolina vecchia”. Sebbene non abbia il risvolto terapeutico valido sperato, è ancora oggi utilizzata (chiaramente prodotta con tecniche più all’avanguardia) a scopo diagnostico. Infatti la “tubercolina vecchia” fu utilizzata fin dal 1906 nella diagnosi di Tubercolosi per mezzo di una tecnica messa a punto dal pediatra austriaco Clemens von Pirquet; la prova («cutireazione di von Pirquet») consisteva nell’applicare una goccia di “tubercolina vecchia” su di una scarificazione praticata sulla cute. Attorno agli anni sessanta la tubercolina vecchia venne sostituita dalla tubercolina «PPD» (“Purified Protein Derivative”, in italiano: “Derivato Proteico Purificato”) ottenuta per frazionamento chimico della tubercolina vecchia. La PPD si ottiene da frazioni solubili in acqua, preparate scaldando al vapore libero e successivamente filtrando le colture del bacillo di Koch che si sono sviluppate in un substrato liquido sintetico. La frazione attiva del filtrato, proteica, viene isolata per precipitazione, lavata e nuovamente diluita ed addizionata con sostanze antimicrobiche, come per es. il fenolo, che non danno luogo a reazioni falsamente positive. Lo studio della tubercolosi e del batterio che la provoca porterà Koch anche a sostenere, a ragione, anche se nessuno gli crederà, al Congresso Medico sulla Tubercolosi svoltosi a Londra nel 1901, che il batterio che causa la tubercolosi umana e quello che causa la tubercolosi bovina sono differenti. Con la scoperta del Mycobacterium tuberculosis e della Tubercolina da parte di Koch, con la cutireazione di von Pirquet e con la tecnica di colorazione dei preparati messa a punto da Ziehl-Neelsen (Fig. 11) si riuscì ad avere una visione più precisa del problema della Tubercolosi e fu stimato che nel 1900 il 12% dei casi di morte era dovuto alla infezione da Mycobacterium tuberculosis e una gran parte della popolazione adulta nelle grandi città europee era  infetto dal batterio.
infetto dal batterio.
Fig. 11: la colorazione di Ziehl-Neelsen con la quale si evidenziano i Micobatteri nei vari preparati biologici.
La croce di Lorena.
All’inizio del ventesimo secolo, la tubercolosi era una dei problemi di salute più urgenti soprattutto nel Regno Unito. Nel 1901 fu costituita una commissione denominata “The Royal Commission appointed to inquire into relations of human and animal tubercolosis”. Il suo scopo era scoprire se la tubercolosi negli animali e nell’uomo fosse la stessa malattia, e se gli animali e l’uomo potessero infettarsi a vicenda. Dal 1919 la commissione divenne il “Medical Research Council” del Regno Unito.
Da quando fu provato nel 1880 che la malattia era contagiosa, la tubercolosi divenne una malattia conosciuta e le persone infette furono costrette ad entrare nei sanatori che sembravano prigioni, anche se i sanatori per le classi media e alta offrivano cure eccellenti e costante attenzione medica. La Germania fu all’avanguardia in quel periodo perché, grazie alla legge di assicurazione sociale contro le malattie (1883), furono costruiti numerosi sanatori ad Hannover (70 letti), a Grabowsee
(189 letti), a Oberderg (114 letti), a Stiege (80 letti). Ma oltre a questi luoghi di cura anche altri, più piccoli, entrarono in attività. Nel 1889 a Boston, la Società Americana di Climatologia, riconosceva che la miglior opportunità di cura per i tisici era il sanatorio. Da un punto di vista scientifico e organizzativo fu importantissimo il Congresso di Berlino del 1889 nel quale veniva affermato, nella risoluzione conclusiva, che “La TBC (Tubercolosi) è una malattia popolare e la lotta contro di essa deve venire condotta con i mezzi di tutto il popolo”. In Italia, a partire dal 1898, erano sorti diversi comitati locali (Siena, Pisa, Padova) e l’anno seguente queste associazioni davano vita alla Lega Italiana, sotto il patronato del Re d’Italia e con Presidente Guido Baccelli. Nel 1900 si tenne a Napoli, su iniziativa della Lega Italiana, un congresso sulla tubercolosi che, nella mozione conclusiva, riportava due importanti obbiettivi programmatici. Il primo era l’istituzione di una Cattedra per lo studio sperimentale e clinico della tubercolosi, il secondo auspicava l’intervento dello Stato e degli Enti pubblici per la costruzione dei sanatori. Riprendendo infine le indicazioni emerse dai
Congressi di Berlino (1889) e di Parigi del 1898 si rilanciava la proposta di formare un Comitato
Internazionale con i rappresentati di Francia, Germania ed Italia. La prima Lega Nazionale contro la Tubercolosi fu fondata in Francia nel 1891, seguita nel 1893 dall’Associazione Svizzera per lottare contro la Tubercolosi e costruire i sanatori. Due anni dopo fu costituito il Comitato Centrale Tedesco per la lotta alla tubercolosi.
Nel 1902 si tenne a Berlino la prima Conferenza internazionale contro la tubercolosi, che introdusse l’idea di una lotta internazionale contro la tubercolosi e propose l’adozione della croce di Lorena (proposta dal medico parigino G. Sersiron) come simbolo della “crociata” contro il male, a ricordo di Goffredo di Buglione che la adottò come simbolo nel suo stendardo nel corso della 1° Crociata. La proposta fu accolta durante la costituzione effettiva dell’Unione internazionale contro la tubercolosi e le malattie respiratorie, nel 1920. Il concetto di aiuto collettivo, sviluppatosi come estensione laica della “cristiana solidarietà”, nel corso della fine del XIX e della prima metà del XX secolo si rafforza, compiendo un salto di qualità sul piano organizzativo; si affermò il valore del concorso collettivo negli studi, corroborato dall’azione propulsiva delle associazioni scientifiche. Queste, riunendosi in congressi nazionali ed internazionali, svolsero una profonda funzione di stimolo e di indirizzo sui governi degli stati più moderni. Le eccezionali scoperte scientifiche in ambito microbiologico di quel periodo, grazie all’opera divulgativa, intrinseca al dibattito dei ricercatori e mediante l’ispirazione di leggi collegate a campagne d’opinione, guidarono importanti indirizzi di politica sanitaria. Questo sinergismo d’azione alimentò la crescita sociale e sanitaria, ma gli scarsi presidii terapeutici a disposizione non potevano consentire un altrettanto efficace contrasto dell’epidemia tubercolare.
 Nonostante i benefici dell’aria fresca e del lavoro nei sanatori, anche sotto le migliori condizioni, il 50% di coloro che entravano morivano in cinque anni (1916). In Italia si ebbero comunque delle deflessioni nel tasso di mortalità per Tubercolosi nel periodo 1900-1914 (Fig. 11), in coincidenza della diffusione della “collassoterapia secondo Forlanini”, consistente nel provocato collasso o afflosciamento del polmone (tramite pneumotorace o altro intervento chirurgico), introdotta
Nonostante i benefici dell’aria fresca e del lavoro nei sanatori, anche sotto le migliori condizioni, il 50% di coloro che entravano morivano in cinque anni (1916). In Italia si ebbero comunque delle deflessioni nel tasso di mortalità per Tubercolosi nel periodo 1900-1914 (Fig. 11), in coincidenza della diffusione della “collassoterapia secondo Forlanini”, consistente nel provocato collasso o afflosciamento del polmone (tramite pneumotorace o altro intervento chirurgico), introdotta  da Carlo Forlanini (1882) con il pneumotorace artificiale intrapleurico (Fig. 12) e della diagnostica radiologica.
da Carlo Forlanini (1882) con il pneumotorace artificiale intrapleurico (Fig. 12) e della diagnostica radiologica.
Fig. 11: Tasso di mortalità per tubercolosi in Italia dal 1900 al 1951
Fig. 12: apparecchio per pneumotorace ideato da Carlo Forlanini.
Purtroppo con lo scoppio della prima guerra mondiale furono stroncate tutte le iniziative di collegamento e coordinamento fra le diverse nazioni. Con il riemergere delle antiche rivalità, vennero meno gli organismi sanitari internazionali che negli anni precedenti avevano consentito scambi di idee, omogeneizzando le linee d’indirizzo organizzative dei diversi governi ed apparati sanitari.
In Italia i dati raccolti a posteriori dimostrano che già a partire dal 1914 si registrò una ripresa significativa dei decessi per tubercolosi, in particolar modo fra i bambini. Tra il 1914 ed il 1918 questa tendenza, caratterizzata dalla riaccensione del fenomeno, si registrò non soltanto negli stati belligeranti, ma anche fra le popolazioni degli stati neutrali. Con la chiamata alle armi anche di soggetti a rischio si delineò, rapidamente, una crescita della tubercolosi fra i diversi eserciti e poi tra i prigionieri di guerra che si andavano ammassando, nei campi di prigionia, nel prosieguo del conflitto. Il contagio in trincea e nelle caserme, il deficit di alimentazione dei soldati e della popolazione civile erano i fattori epidemici più significativi; si osservavano però peculiarità e caratteristiche varianti in ogni paese. In Francia, per esempio, con l’utilizzo di truppe africane nelle retrovie, dal Reno alle Alpi, si osservò la diffusione massiva dell’epidemia tra questi soldati. Queste truppe, provenienti da regioni che in quell’epoca non avevano ancora subìto un’importante pressione epidemica tubercolare, si trovavano, per la prima volta nella loro vita, a contatto con l’infezione. In Italia, tra il 1917 ed il 1918, furono rimpatriati11.000 prigionieri dai campi di detenzione austriaci perché affetti dalla malattia tubercolare. A partire dal 1916 la Federazione delle Opere antitubercolari aveva proposto un piano per far fronte ad un’emergenza di questo tipo. L’anno seguente la Direzione Generale di Sanità Militare era in grado di accogliere in centri di accertamento diagnostico circa 20.000 soldati. Nel 1918 la mortalità in Italia per TBC toccò la cifra di 73.000 decessi; negli anni precedenti allo scoppio del conflitto i deceduti erano annualmente circa 50.000 (Fig. 11)
Visto il diffondersi della tubercolosi, si cercarono nuove strade per il suo contenimento. Su iniziativa del medico Gaetano Ronzoni fu istituito il Consorzio Provinciale Antitubercolare. Facevano parte obbligatoriamente del consorzio la Provincia, i Comuni e gli enti pubblici che in tutto e in parte svolgevano azione antitubercolare. Essi sorsero allo scopo di promuovere e agevolare l’impianto di opere necessarie alla lotta contro la tubercolosi; di coordinare e disciplinare il funzionamento delle opere esistenti nella provincia a tale scopo, di vigilare sulla protezione e l’assistenza sanitaria e sociale dei malati, di integrare con i propri mezzi l’azione delle istituzioni antitubercolari. Organi esecutivi dei Consorzi erano i Dispensari, finalizzati a individuare i casi di tubercolosi (anche in forme latenti attraverso il test della tubercolina), all’educazione sanitaria e alla profilassi, all’assistenza morale e materiale ai malati (con particolare riguardo ai bambini avviati alle colonie marine e montane), all’attività di propaganda, alla raccolta di dati per le statistiche e alla promozione di studi e ricerche. In Italia fu istituita inoltre, nel 1922, la FNILT Federazione Nazionale Italiana per la lotta contro la Tubercolosi, come organo di collegamento dei 28 Consorzi Provinciali Antitubercolari esistenti e di unificazione delle associazioni operanti nel campo degli studi e dell’azione socio sanitaria antitubercolare. La Federazione ha svolto la sua attività per la prevenzione della tubercolosi, a carattere scientifico, culturale e divulgativo in stretto collegamento con le omologhe istituzioni straniere. In Italia già nel 1907 alla Conferenza Internazionale di Roma si era stabilito di affidare alla Lega delle Croci Rosse di condurre a termine una ricerca per accertare la diffusione della malattia negli ambienti operai industriali. Per vari motivi, tra cui anche il primo conflitto mondiale, questa indicazione non fu subito sviluppata. Fu ripresa in considerazione solo nel 1928-29, quando l’Ufficio d’Igiene di Milano l’adottò sviluppando un’inchiesta fra le operaie di una fabbrica ove si lavorava la gomma, ottenendo interessanti risultati. E’ del 1915 la nascita dell’Opera di Prevenzione Antitubercolare Infantile (Mangiagalli), che andò a svolgere la sua missione a Milano, assistendo i figli dei tisici. In questo caso si registrarono elargizioni significative di banche e di privati in varie città italiane (Torino, Milano, Verona, Palermo, Alessandria, Milano, Trapani, Roma, Reggio Calabria). A Torino la famiglia Agnelli si distinse per generosità.
Nel 1920 e nel 1921, per ricordare il loro problema gli ex-militari italiani, dichiarati invalidi perché tisici e costituitisi in associazione, tennero due congressi, rispettivamente, a Milano ed a Roma. Questa spinta rivendicativa venne recepita dal Governo Italiano che, costituendo l’Opera Nazionale per gli Invalidi di Guerra, andò ad inglobare anche le richieste dei militari tubercolotici, disciplinando le cure per questi malati. Anche l’Opera Nazionale per la Maternità e l’Infanzia, voluta nel 1925 dal Governo, si occupò della prevenzione: accudiva i figli dei tubercolotici mediante provvedimenti di prevenzione primaria e secondaria. Nel periodo 1919-1930 crebbe la disciplina legale assicurativa e mediante il concorso attivo di nuovi strati di popolazione, prima non coinvolti, si ottenne così un’organizzazione di tipo nazionale più efficace. Nel 1919 una legge specifica decuplicava gli stanziamenti di bilancio, concedendo crediti e sussidi per la costruzione di dispensari e sanatori. Si trasformarono così i Comitati Provinciali Antitubercolari in Consorzi fra i Comuni, Provincie ed Opere antitubercolari, con l’intento di meglio coordinare ed unificare l’azione da svolgere. Nel 1923venne data facoltà ai Prefetti di dichiarare l’obbligatorietà dei Consorzi. Il regime fascista fece propria una questione di così grande importanza sociale e nazionale come la lotta contro la Tubercolosi promulgando nel 1927 una Legge che rese obbligatoria, in ogni provincia, la costituzione del Consorzio antitubercolare come ente di diritto pubblico destinato alla disciplina della lotta, alla tutela ed assistenza del malato, nonché alla profilassi dei sani nella rispettiva provincia. In particolare con il Decreto Legge del 17 ottobre 1927 si imponeva a tutti gli assicurati per invalidità e vecchiaia, un contributo per organizzare ed eseguire l’assistenza, nel caso che essi o persone di famiglia si fossero ammalati di TBC. La emanazione del Decreto fu preannunciata, alla vigilia del quinto anniversario della marcia su Roma, al II Congresso nazionale per la lotta antitubercolare (Milano, ottobre 1927) nel quale figura all’ordine del giorno anche il tema del finanziamento della lotta contro la tubercolosi. Si calcolò che, grazie a questi provvedimenti, quasi la metà della popolazione italiana sia stata coinvolta nei benefici assicurativi. Si ottenne un sensibile calo del tasso di mortalità: 160 decessi per 100.000 abitanti nel 1920, 112 decessi per 100.000 nel 1930 (Fig. 11). Il cartogramma riportato in Fig. 12 consente di valutare, nel 1927, la mortalità per tubercolosi (tutte le forme), per ciascuna provincia. Nel 1928 la Federazione organizzò a Roma, per formare imedici impegnati contro la Tubercolosi, un corso di aggiornamento sulle ultime acquisizioni sanitarie e
Scientifiche. L’organizzazione sanitaria a favore dei tubercolotici, in mancanza dei presidi farmacologici indispensabili ancora non disponibili14, rispondeva come poteva al dilagare dell’epidemia tubercolare. Si implementavano così i posti letto nei sanatori: erano 12.000 nel 1923, nel 1930 divennero32.00015. In termini di mortalità e morbilità pur presentando miglioramenti la situazione rimaneva drammatica. Nel 1910 la mortalità per tubercolosi era pari a 161 decessi per100.000 abitanti, nel 1920 era di 160, per scendere a 112 nel 1930. (Dati Ministero dell’Interno– Direzione Generale Sanità Pubblica). L’Italia in quegli anni contava i morti. Uno studio del 1931 rilevava che “al quinto anno dall’inizio della lotta alla TBC si registravano 10.000 decessi in meno all’anno, grazie alla pianificazione degli interventi di prevenzione e dell’assistenza curativa”. Inoltre si riportavano mille decessi in meno su 6.000 morti per meningite tubercolare. All’epoca la meningite tubercolare 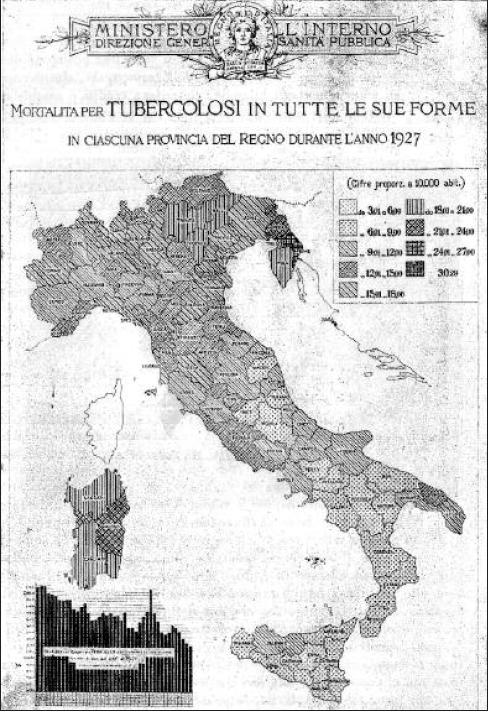 presentava un tasso di letalità del 100%.
presentava un tasso di letalità del 100%.
Fig. 12: cartogramma della mortalità per Tubercolosi nelle province italiani del 1927.
Durante la VI conferenza internazionale della tubercolosi tenutasi a Roma nel 1928, la Croce di Lorena ricevette la codifica e la consacrazione ufficiale come emblema della lotta contro la Tubecolosi. Nonostante le iniziative del Governo Fascista come il grande sanatorio, inizialmente chiamato “Istituto Benito Mussolini” (successivamente trasformato nell’ Ospedale “Carlo Forlanini” grande e prestigioso istituto scientifico di riferimento e importante centro di ricerca sociale sulla tu
bercolosi a livello mondiale), inaugurato grandiosamente il primo dicembre 1934 proprio dal capo





 Fig. 13 : Francobolli Antitubercolari.
Fig. 13 : Francobolli Antitubercolari.
del Governo Benito Mussolini, i ceti sociali più deboli ed emarginati, a causa di povertà, denutrizione e forzata coabitazione, continuarono però a restare pressoché indifesi. Furono intraprese campagne di beneficenza promosse soprattutto dalla Croce Rossa Italiana, impegnata con successo nella costruzione di nuovi sanatori civili, che contribuirono, significativamente, alla lotta alla Tubercolosi negli anni venti e trenta E costituendo i “preventori” per i figli dei tubercolotici. Famoso fu quello di Fara Sabina Aperto il 16 novembre 1918 e chiuso il 16 luglio 1919. Ospitava 100 letti e fu trasformato in collegio permanente per i figli di tubercolotici. Furono organizzate, in collaborazione con la Croce Rossa Italiana, campagne governative per la raccolta di fondi da destinare alla lotta antitubercolare che prevedevano la vendita di francobolli con la Croce di Lorena (fig.13).
I Vaccini.
Nella lotta alla Tubercolosi furono inventati due vaccini.
Il primo fu quello all’italiana (come lo si definiva all’epoca), costituito da micobatteri uccisi al calore messo a punto dalla scuola di Edoardo Maragliano. Fu utilizzato sull’uomo nei primi due decenni del Novecento. Il vaccino italiano ebbe due evoluzioni. Negli anni Venti-Trenta ci fu l’Anatubercolina Integrale Petragnani (AIP) messo a punto dal tisiologo e rettore Università di Siena,
Giovanni Petragnani sull’esperienza precedente. Infine, dal 1938 al 1976 il VDS Vaccino Diffondente Salvioli del professor Gaetano Salvioli dell’Università di Bologna.
Il secondo vaccino anti tbc, definito alla francese, è stato, ed è il BCG (Bacillo di Calmette-Guérin), sviluppato sul principio opposto a quello italiano. Il BCG è costituito da micobatteri vivi, ma attenuati. Il BCG fu sviluppato da Albert Calmette e Camille Guérin all’Istituto Pasteur in Francia tra il 1908 e il 1921. I primi esperimenti del BCG sull’uomo avvennero nel 1921 in Francia. Weill-Hallé e Turpin negli anni 1921-1922 condussero esperimenti su neonati a rischio somministrando loro dosi orali di 2 mg. di BCG a 3,5,7 giorni di vita senza suscitare effetti collaterali di rilievo dimostrando la resistenza nel tempo di questi bambini all’infezione tubercolare. Questa pratica vaccinale fu presto adottata, anche se ancora in via sperimentale, in Europa e nelle colonie francesi. Successivamente il BCG orale fu sostituito da quello sottocutaneo che si era rivelato più attivo, ma ci si avvide presto che l’introduzione del vaccino sottocute determinava facilmente una lesione di notevoli dimensioni, che si poteva ulcerare e andare incontro a fluidificazione, perciò si scelse la via intradermica come metodo di elezione.
Anche in Italia ci fu chi promosse l’uso del BCG; si tratta di Alberto Ascoli fondatore dell’IstitutoVaccinogeno Antitubercolare.
Con la legge 25 novembre 1926 la vaccinazione con BCG fu intrapresa in Italia dapprima in campo veterinario, poi in campo umano.
L’introduzione della vaccinazione contro la Tubercolosi, disponibile dal 1927, venne ritardata a causa di un grave incidente noto più tardi come “disastro di Lubecca” del 1930; a 251 neonati vennero somministrate, per via orale, tre dosi di vaccino antitubercolare a base di BCG , risultate ad una successiva indagine sanitaria condotta dal Dr. A. Moegling contaminate da batteri Mycobacterium tuberculosis virulenti. Morirono 72 bambini mentre 173 sopravvissero alla infezione sviluppando però segni clinici e radiologici di Tubercolosi. Comunque fu escluso che i batteri del vaccino BCG si fossero trasformati in virulenti e nonostante l’alto tasso di mortalità (circa il 29%) la maggior parte dei neonati incidentalmente inoculati con batteri virulenti superò la malattia tubercolare dimostrando così la resistenza naturale della specie umana al batterio della Tubercolosi; per questo motivo le vaccinazioni furono riprese.
La vaccinazione antitubercolare trovò ampia diffusione solo dagli anni 1950-60; insieme ai tubercolostatici contribuì significativamente alla riduzione della tubercolosi nei Paesi industrializzati
Nel 1931 l’Istituto Vaccinogeno Antitubercolare fu eretto ad ente morale.
Tuttavia, avversato da Petragnani, Ascoli si dimise dalla direzione scientifica dell’Istituto il 27 luglio 1939, anche per le leggi razziali promulgate dal regime fascista, essendo lui ebreo, e l’attività dell’Istituto stesso venne interrotta il 30 settembre 1940 per essere affidata alla Stazione zooprofilattica di Brescia.
L’Istituto riaprì nel 1948 a Milano per iniziativa del sindaco e tisiologo Virgilio Ferrari e dell’assessore all’Igiene, l’igienista Augusto Giovanardi i quali propugnarono l’uso del BCG come strumento di controllo della tubercolosi.
Giovanardi, dopo un periodo d’incertezza, dovuto al conflitto fra il vaccino Maragliano-Petragnani-Salvioli a germi uccisi e il vaccino vivo attenuato di origine bovina BCG, al Congresso di Montecatini del 1949 segnalò quest’ultimo come il solo vaccino capace di soddisfare tutti i requisiti di efficacia. Nel 1948 fu una lanciata una straordinaria campagna sanitaria per il controllo della Tubercolosi promossa dall’ UNICEF e dalla Croce Rossa Danese sotto la direzione di Johannes Holm, Chief Tuberculosi Division, State Serum Institut Copenhaghn – Denmark, che aveva già condotto una estesa campagna vaccinale in Danimarca. La campagna prevedeva l’esecuzione del test cutaneo alla tubercolina e la vaccinazione dei soggetti non rettivi con BCG. Iniziò in Polonia ma fu subito estesa ad altre regioni europee ed estesa all’ Ecuador. Nei successivi 3 anni vennero testate con la tubercolina circa 30 milioni di persone e vennero vaccinate circa 14 milioni di persone. Questo programma fu il primo programma di controllo di una malattia intrapreso da una agenzia della Organizzazione Mondiale di Sanità (WHO).
Nel 1951 ebbe inizio anche in Italia l’attività vaccinale selettiva, come raccomandava l’OMS e nel 1970 risultarono vaccinate 400.000 persone; poco per poter influire sull’epidemiologia della malattia. Solo con la legge 1088 del 14/12/1970 si ebbe l’obbligatorietà selettiva della vaccinazione antitubercolare, senza che fosse fatto cenno al particolare tipo di vaccino da usarsi, anche se nel 1965 il Consiglio Superiore di Sanità aveva raccomandato il BCG, pur non escludendo altri vaccini.
Il BCG fu scelto in via definitiva dal Ministero della Salute italiano nel 1976.
L’efficacia della vaccinazione con BCG nei confronti della TB polmonare negli adulti è fortemente variabile e mediamente bassa, mentre i risultati nella popolazione pediatrica nella prevenzione delle forme di TB meningea e miliare (forme cliniche severe di TB) sono più consistenti e l’efficacia è maggiore.
La terapia.
Il contributo più importante alla lotta alla Tubercolosi fu la scoperta della Streptomicina. La streptomicina fu isolata inizialmente nel 1943, da Albert Schatz, nel laboratorio di Selman Abraham Waksman alla Rutgers University. Waksman, Schatz e Wlizabeth Bugie avevano scoperto che il batterio presente nel suolo batterio scoperto da A. Krainsky nel 1914, l’ Actinomyces griseus, ribattezzato successivamente Streptomyces griseus, era in grado di produrre sostanze bioattive, fra cui diversi antibiotici come l’actinomicina, la clavacina, la streptotricina, la griseina, la neomicina, la fradicina, la candicina e la candidina. Di questi, la streptomicina e la neomicina furono quelli che andarono incontro a più estesi usi nel trattamento di numerose infezioni; la streptomicina fu uno dei primi a essere usati contro la tubercolosi. La scoperta della streptomicina è generalmente considerata l’inizio dell’era moderna della tubercolosi, anche se la vera rivoluzione comincia qualche anno dopo, nel 1952, con lo sviluppo dell’isoniazide, il primo farmaco micobattericida orale. L’avvento della rifampicina nel 1970 accelerò i tempi di ricovero e ridusse in modo significativo il numero di casi di tubercolosi fino al 1980.
 Selman Waksman fu insignito del premio Nobel per la Medicina nel 1952 (Fig. 13 e 14)
Selman Waksman fu insignito del premio Nobel per la Medicina nel 1952 (Fig. 13 e 14)
 Fig. 13: Lettura di Selman Waksman nel 1952 in occasione del premio Nobel per la Medicina confertogli per la scoperte della Streptomicina.
Fig. 13: Lettura di Selman Waksman nel 1952 in occasione del premio Nobel per la Medicina confertogli per la scoperte della Streptomicina.
Fig. 14: Le tappe salienti della Tubercolosi
La tubercolosi nella seconda metà del XX secolo.
 La attività dei Sanatori e Dispensari, le campagne antitubercolari e la scoperta dei farmaci attivi contro il batterio della Tubercolosi come la Isoniazide nel 1952 (che blocca la sintesi degi acidi micolici, importanti costituenti della parete batterica), la Pyrazinamide nel 1954 (inibitore FAS1-Fatty Acid Sintase di tipo 1) e l’ Etambutolo nel 1962 (che blocca la arabinnositrasferasi del batterio e quindi la sintesi della parete cellulare) le Rifamicine: la Rifampicina e Rifabutina (che inibiscono la RNA-polimrasi DNA-dipendente e quindi provocano il blocco della sintesi proteica batterica) aveva fatto sperare che la Tubercolosi, almeno nei paesi sviluppati, potesse essere debellata (Fig. 15 e 16).
La attività dei Sanatori e Dispensari, le campagne antitubercolari e la scoperta dei farmaci attivi contro il batterio della Tubercolosi come la Isoniazide nel 1952 (che blocca la sintesi degi acidi micolici, importanti costituenti della parete batterica), la Pyrazinamide nel 1954 (inibitore FAS1-Fatty Acid Sintase di tipo 1) e l’ Etambutolo nel 1962 (che blocca la arabinnositrasferasi del batterio e quindi la sintesi della parete cellulare) le Rifamicine: la Rifampicina e Rifabutina (che inibiscono la RNA-polimrasi DNA-dipendente e quindi provocano il blocco della sintesi proteica batterica) aveva fatto sperare che la Tubercolosi, almeno nei paesi sviluppati, potesse essere debellata (Fig. 15 e 16).
 Fig.15: diminuzione della mortalità per tubercolosi In Italia dal 1965.
Fig.15: diminuzione della mortalità per tubercolosi In Italia dal 1965.
Fig. 16: diminuzione della mortalità per tubercolosi in UK dopo la scoperta della Streptomicina e con la adozione di campagne vaccinali.
Alla fine degli anni Settanta, pensando illusoriamente che la tubercolosi nei ricchi paesi occidentali fosse oramai debellata, si era provveduto a smantellare quelle strutture come i dispensari e i sanatori trascurando che già nel 1950 il giovane medico inglese John Crofton aveva osservato in alcuni pazienti ceppi resistenti alla Streptomicina per cui aveva adottato una bi-terapia aggiungendo alla Streptomicina l’Acido Paramino-Salicilico (PAS). Ben presto venne osservata dallo stesso Crofton e colleghi la resistenza alla doppia terapia. Venne adottata una tri-terapia aggiungendo la Isoniazide (The Edimburgh Method). Questa tri-terapia era ovviamente più costosa.
 Fig. 18: discrepanza fra il numero di casi di Tubercolosi attesi e quelli osservati negli U.S.A.
Fig. 18: discrepanza fra il numero di casi di Tubercolosi attesi e quelli osservati negli U.S.A.
 Le speranze che la malattia potesse essere completamente eliminata si frantumò negli anni ’80; infatti intorno al 1985 per vari motivi spesso interconnessi come l’aumento della popolazione carceraria, l’aumento degli “homeless”, la diffusione delle droghe d’abuso, l’affollamento degli alloggi, la vita nelle baraccopoli, la povertà e l’emarginazione (mancato accesso alle cure), l’aumento delle persone ricoverate negli ospizi per anziani, la pandemia di AIDS, l’ aumento della immigrazione di popolazioni provenienti da aree ad alta endemia di Tubercolosi (Fig. 19), il rallentamento delle attività di sorveglianza. A far aumentare la diffusione della infezione contribuirono la epidemia di HIV/AIDS e la comparsa di ceppi multi-resistenti ai farmaci (MultiDrugResistant TuBercolosis – MDR-TB).
Le speranze che la malattia potesse essere completamente eliminata si frantumò negli anni ’80; infatti intorno al 1985 per vari motivi spesso interconnessi come l’aumento della popolazione carceraria, l’aumento degli “homeless”, la diffusione delle droghe d’abuso, l’affollamento degli alloggi, la vita nelle baraccopoli, la povertà e l’emarginazione (mancato accesso alle cure), l’aumento delle persone ricoverate negli ospizi per anziani, la pandemia di AIDS, l’ aumento della immigrazione di popolazioni provenienti da aree ad alta endemia di Tubercolosi (Fig. 19), il rallentamento delle attività di sorveglianza. A far aumentare la diffusione della infezione contribuirono la epidemia di HIV/AIDS e la comparsa di ceppi multi-resistenti ai farmaci (MultiDrugResistant TuBercolosis – MDR-TB).  A New York l’eliminazione di istituzioni per la salute pubblica e l’emergenza dell’HIV, determinò una recrudescenza della TB verso la fine del 1980; il numero di pazienti che non riuscivano a completare la cura con i farmaci era alto. Per questo New York dovette affrontare una nuova emergenza: più di 20.000 pazienti con TB con ceppi MDR-TB (resistenti a entrambi i farmaci:
A New York l’eliminazione di istituzioni per la salute pubblica e l’emergenza dell’HIV, determinò una recrudescenza della TB verso la fine del 1980; il numero di pazienti che non riuscivano a completare la cura con i farmaci era alto. Per questo New York dovette affrontare una nuova emergenza: più di 20.000 pazienti con TB con ceppi MDR-TB (resistenti a entrambi i farmaci: 

 rifampicina e isoniazide) (Fig.20)
rifampicina e isoniazide) (Fig.20)
Fig.19: Casi di TB in Inghilterra secondo l’origine etnica
Fig. 20: coincidenza fra la epidemia di Tubercolosi e la epidemia di AIDS nella città di New York alla fine del 1980 e inizi degli ann1 ’90.
Fig. 21: Report del WHO (World Healt Organization) 1993.
 Gli anni ’70 erano stati contrassegnati dalla speranza della eradicazione della Tubercolosi (almeno nelle regioni economicamente sviluppate). Purtroppo i dati epidemiologici forniti dal Dr. Mario Raviglione (Professore all’ Università di Milano) e Arata Kochi del Tuberculosi Programme della l’Organizzazione Mondiale della Sanità – WHO (World Healt Organization) erano particolarmente allarmanti: nel 1990 la incidenza della tubercolosi era stimata in 7,5 milioni di casi, di cui 3,1 milioni nel Sud-Est asiatico, 1,8 milioni nella regione del Pacifico occidentale, 1,0 milioni nell’ Africa sub-Sahariana e 1,6 milioni nelle altre regioni del mondo. Era evidente, quindi, che la sola disponibilità di farmaci anti-tubercolari non riusciva a controllare la tubercolosi a causa della impossibilità di controllare la auto-somministrazione dei farmaci per ragioni organizzative (le strutture sanitarie deputate al controllo della tubercolosi erano state smantellate nei paesi sviluppati e non erano mai state attivate nei paesi poveri); in molti paesi poveri non c’era accesso alla cura delle Tubercolosi attive (i malati disseminano batteri con la tosse e contagiano persone sane) né era possibile stabilire un trattamento profilattico per prevenire la Tubercolosi attiva nei soggetti contagiati. In studi condotti in India nei primi anni ’90 emergeva che il trattamento farmacologico della malattia, in chi poteva sopportarne i costi, portava a indebitamento personale e familiare. Nella regione di Pune (India) i pazienti spendevano metà del loro stipendio mensile per il trattamento anti-tubercolare; questo portava un terzo di essi ad indebitarsi. L’impatto negativo della malattia sulla economia familiare era evidente: un soggetto affetto da tubercolosi non può lavorare quindi non può contribuire economicamente al bilancio familiare inoltre la malattia sottrae risorse per le cure. Questo circolo vizioso impoverisce ulteriormente le famiglie già povere. La Tubercolosi non solo è il riflesso della povertà ma contribuisce a generare povertà (Fig. 22).
Gli anni ’70 erano stati contrassegnati dalla speranza della eradicazione della Tubercolosi (almeno nelle regioni economicamente sviluppate). Purtroppo i dati epidemiologici forniti dal Dr. Mario Raviglione (Professore all’ Università di Milano) e Arata Kochi del Tuberculosi Programme della l’Organizzazione Mondiale della Sanità – WHO (World Healt Organization) erano particolarmente allarmanti: nel 1990 la incidenza della tubercolosi era stimata in 7,5 milioni di casi, di cui 3,1 milioni nel Sud-Est asiatico, 1,8 milioni nella regione del Pacifico occidentale, 1,0 milioni nell’ Africa sub-Sahariana e 1,6 milioni nelle altre regioni del mondo. Era evidente, quindi, che la sola disponibilità di farmaci anti-tubercolari non riusciva a controllare la tubercolosi a causa della impossibilità di controllare la auto-somministrazione dei farmaci per ragioni organizzative (le strutture sanitarie deputate al controllo della tubercolosi erano state smantellate nei paesi sviluppati e non erano mai state attivate nei paesi poveri); in molti paesi poveri non c’era accesso alla cura delle Tubercolosi attive (i malati disseminano batteri con la tosse e contagiano persone sane) né era possibile stabilire un trattamento profilattico per prevenire la Tubercolosi attiva nei soggetti contagiati. In studi condotti in India nei primi anni ’90 emergeva che il trattamento farmacologico della malattia, in chi poteva sopportarne i costi, portava a indebitamento personale e familiare. Nella regione di Pune (India) i pazienti spendevano metà del loro stipendio mensile per il trattamento anti-tubercolare; questo portava un terzo di essi ad indebitarsi. L’impatto negativo della malattia sulla economia familiare era evidente: un soggetto affetto da tubercolosi non può lavorare quindi non può contribuire economicamente al bilancio familiare inoltre la malattia sottrae risorse per le cure. Questo circolo vizioso impoverisce ulteriormente le famiglie già povere. La Tubercolosi non solo è il riflesso della povertà ma contribuisce a generare povertà (Fig. 22).
Fig. 22: la maggiore prevalenza della Tubercolosi si riscontra nelle aree più povere del mondo (linee verdi). Le linee rosse indicano i tassi di prevalenza della co-infezione Tubercolosi-HIV.
 Anche il crollo del regime comunista aveva contribuito al riemergere della Tubercolosi. Infatti sia durante il periodo pre-Rivoluzione dal 1902 al 1917 che in quello dei Soviet erano stati varati programmi di contrasto alla Tubercolosi (Sanatori, raccolta di fondi per il trattamento, la individuazione dei malati con il test di Mantoux e la radioscopia, l’isolamento e la riabilitazione in Sanatorio nonché la profilassi con la vaccinazione) con i quali si era ottenuto una drastica riduzione della mortalità (Fig. 23) ma lo smantellamento del sistema sanitario avutosi nel Post-comunismo
Anche il crollo del regime comunista aveva contribuito al riemergere della Tubercolosi. Infatti sia durante il periodo pre-Rivoluzione dal 1902 al 1917 che in quello dei Soviet erano stati varati programmi di contrasto alla Tubercolosi (Sanatori, raccolta di fondi per il trattamento, la individuazione dei malati con il test di Mantoux e la radioscopia, l’isolamento e la riabilitazione in Sanatorio nonché la profilassi con la vaccinazione) con i quali si era ottenuto una drastica riduzione della mortalità (Fig. 23) ma lo smantellamento del sistema sanitario avutosi nel Post-comunismo
Fig. 23: programmi di lotta alla Tubercolosi nella Russia zarista, nel periodo dei Soviet e della Federazione Russa.
aveva determinato la recrudescenza della tubercolosi. Molti malati avevano dovuto interrompere le terapie per motivi economici accanto alla assenza di strutture di sorveglianza e di monitoraggio della infezione. Dal punto di vista della salute pubblica un trattamento irregolare, incompleto è più pericoloso di una assenza di trattamento. Quando un paziente non riesce a completare un adeguato protocollo terapeutico o riceve un trattamento incompleto non solo rimane infettivo ma può ospitare un ceppo batterico resistente agli antibiotici che può essere trasmesso. Dopo la caduta del Muro di Berlino nel novembre 1989 il con il grave declino economico, la carenza di fondi per far fronte all’arretratezza del Paese, il costo del mantenimento del cosiddetto “impero sovietico”, delle milizie, del KGB avevano rapidamente prosciugato l’economia sovietica questo aveva riportato la mortalità per Tubercolosi a tassi di prevalenza elevati nelle Repubbliche sovietiche; l’Ucraina superava nel 1999 i 20 morti/100.000 abitanti/anno (Fig. 24).


Fig. 24: alti tassi di mortalità per Tubercolosi nelle Repubbliche della ex U.R.S.S.
Nel 1991 Arata Kochi, uno dei “leader” dell’ International Union Against Tuberculosis and Lung Diseases– IUATLD, prima organizzazione non governativa contro la Tubercolosi fondata da 31 nazioni nella prima conferenza post-bellica tenutasi a Parigi nel 1920, scrisse un articolo che dipingeva in modo chiaro l’impatto devastante della Tubercolosi in tutto il mondo; questo articolo cambiò l’ottica dell’Organizzazione Mondiale della Sanità – WHO, dei vari governi nazionali e delle più importanti associazioni di volontariato: la impressionante realtà era che un terzo della popolazione mondiale era infettato dal batterio della Tubercolosi provocando ogni anno 8 milioni di nuovi casi di infezione e 3 milioni di morti per anno, esigeva un cambiamento di rotta. La lotta alla Tubercolosi doveva esigeva delle strategie nuove e globali; nel suo articolo Kochi segnalava che la vaccinazione con BCG non aveva avuto un impatto significativo sulla riduzione della trasmissione della infezione e che la vera emergenza era il trattamento dei soggetti infettivi, in special modo di quelli con espettorato positivo al controllo microscopico. Il principale obiettivo dei programmi di controllo della Tubercolosi doveva essere il tasso di cura (cioè il numero di persone malate che vengono curate con un determinato trattamento) dei pazienti in terapia; adottando “target” specifici e opportuni sistemi di monitoraggio si sarebbe dovuto raggiungere un tasso di cura non inferiore all’85%. Secondo Kochi il raggiungimento del tasso di cura dell’85% in tutto il mondo avrebbe ridotto la prevalenza della Tubercolosi del 50%, con un abbattimento del tasso di mortalità del 40%. Nel suo articolo “Tuberculosis in the present tense: a global overview of tuberculosis stuation” – WHO Working Document Arata Kochi riportava la esperienza fatta dal suo collega del WHO e dello IUATLD: il Dott. Karel Styblo. Il Dott. Styblo conosceva bene la Tubercolosi. Nato in Cecoslovacchia nel 1921sul finire della Seconda Guerra Mondiale fu fatto prigioniero nel campo di concentramento di Mauthausen-Gusen in Austria dove contrasse la Tubercolosi. Dopo il recupero dalla malattia e dopo la liberazione, entrò nella “Charles University” di Praga. Durante gli studi di medicina la infezione tubercolare contratta a Mauthausen si riattivò e fu ricoverato e curato nell’ospedale “Bulovka” di Praga dall’ottobre 1948 sin all’aprile del 1950. Dopo aver conseguito la Laurea in Medicina nel 1950, ritornò nell’ospedale “Bulovka” in qualità di Pneumologo; dopo 5 anni si specializzò al Tuberculosis Research Institute della Università di Edimburgo sotto la guida di Sir John Crofton. Famoso a livello internazionale per la sua attività contro la Tubercolosi fu nominato consulente della Royal Netherlands Tuberculosis Association e direttore dell’International Union Against Tuberculosis and Lung Disease (IUATLD) a Parigi nel1979. Viene considerato “il padre della epidemiologia moderna della Tubercolosi” e “padre della lotta moderna alla Tubercolosi”. Nel 1980 Styblo definì per lo IUATLD una nuova strategia di lotta alla Tubercolosi: il Programma denominato DOTS (Directly Observed Therapy – Short Course) applicato con successo in Tanzania, Benin, Malawi, Mozambique, Nicaragua. Nel 1990 la Banca Mondiale chiese al Dott. Styblo di creare un progetto pilota DOTS in Cina. Nel 1991 la nuova strategia fu adottata dal Governo Peruviano. Il programma DOTS è stato definito “il modo più efficace di controllo della Tubercolosi negli anni novanta” ed applicato finno al 2001 in più di 90 nazioni. I capisaldi della strategia DOTS sono:
- Un efficace impegno dei governi (con un impegno politico a tutti i livelli istituzionali, con lo stanziamento di adeguate risorse economiche, con la istituzione sistemi di monitoraggio della infezione/malattia, con la istituzione del Registro dei malati e con la promulgazione di programmi di addestramento per il personale);
![]()
![]() La individuazione dei casi di malattia con l’esame microscopico dell’espettorato dei pazienti che si presentano alle strutture sanitarie provviste di laboratori diagnostici efficienti (Fig. 25);
La individuazione dei casi di malattia con l’esame microscopico dell’espettorato dei pazienti che si presentano alle strutture sanitarie provviste di laboratori diagnostici efficienti (Fig. 25);
Fig. 25: osservazione al microscopio ottico dei Micobatteri nell’ espettorato
![]()
![]() Short-course chemotherapy – Utilizzo di schemi terapeutici standardizzati di breve durata (6 – 8 mesi) con trattamento effettuato con la supervisione di un sanitario o di un soggetto designato (Fig. 26);
Short-course chemotherapy – Utilizzo di schemi terapeutici standardizzati di breve durata (6 – 8 mesi) con trattamento effettuato con la supervisione di un sanitario o di un soggetto designato (Fig. 26);
Fig. 26: somministrazione di farmaci controllata.
- Una somministrazione senza interruzione e continuata di farmaci qualitativamente idonei e gratuiti;
- Monitoraggio e valutazione dei risultati attraverso la registrazione standardizzata dei dati di ogni paziente per poter evidenziare eventuali problemi e valutare i risultati globali di ogni distretto DOTS.
In risposta alla recrudescenza della tubercolosi, l’Organizzazione Mondiale della Sanità ha emesso una dichiarazione di emergenza sanitaria globale nel 1993 (Fig. 21).
Nel 1994 è stato organizzato un nuovo Gruppo per il controllo della Tubercolosi con la supervisione del Dott. Arata Kochi.
Nel 1995 la Organizzazione Mondiale della Sanità – WHO ha lanciato il primo programma globale per arginare la Tubercolosi attraverso la strategia DOTS che si è protratto fino al 2006.
 La strategia DOTS ha permesso di raggiungere risultati notevoli in termini di tassi di individuazione di casi di malattia e di tassi di cura in molti paesi. In Perù, che negli anni ’90 aveva uno dei più alti tassi di incidenza di Tubercolosi al Mondo (190 casi per 100.000 abitanti), si sono raggiunti il 70% di tasso di individuazione di soggetti malati e l’85% di tasso di cura (Fig.26).
La strategia DOTS ha permesso di raggiungere risultati notevoli in termini di tassi di individuazione di casi di malattia e di tassi di cura in molti paesi. In Perù, che negli anni ’90 aveva uno dei più alti tassi di incidenza di Tubercolosi al Mondo (190 casi per 100.000 abitanti), si sono raggiunti il 70% di tasso di individuazione di soggetti malati e l’85% di tasso di cura (Fig.26).
DOTS
Fig. 26: diminuzione del tasso di incidenza della Tubercolosi in Perù dopo l’adozione del Programma DOTS.
Gli incoraggianti risultati ottenuti con la strategia DOTS furono presto annullati soprattutto per la comparsa dei ceppi farmaco-resistenti responsabili di epidemie silenti nei soggetti senza risorse economiche, specialmente nelle regioni ad alta incidenza di AIDS, paesi in guerra o impoveriti. L’elevato costo per il trattamento della Tubercolosi Multiple-Drug-Resistant (MDRTB) aveva indotto le autorità sanitarie delle nazioni più povere ad ignorare il problema.

La scoperta della regione RD1 ha aperto nuovi scenari per la lotta alla tubercolosi.
Fortunatamente nel 1998 è stato sequenziato l’intero genoma del Mycobacterium tuberculosis, questo ha consentito di individuare una regione particolare nel DNA del batterio: La regione RD1, un frammento di genoma di 10,7 kb che codifica per numerosi geni, tra cui in particolare Esat-6 e cfp10. Tale regione è assente nel ceppo vaccinico M. bovis-BCG ed è stato dimostrato come l’attenuazione di quest’ultimo sia dovuta all’assenza di RD1>>.
Remo Barnabei
Dirigente Biologo presso la Unità Operativa Complessa Medicina di Laboratorio
Ospedale “S. Salvatore” – L’ Aquila




 La individuazione dei casi di malattia con l’esame microscopico dell’espettorato dei pazienti che si presentano alle strutture sanitarie provviste di laboratori diagnostici efficienti (Fig. 25);
La individuazione dei casi di malattia con l’esame microscopico dell’espettorato dei pazienti che si presentano alle strutture sanitarie provviste di laboratori diagnostici efficienti (Fig. 25); 
 Short-course chemotherapy – Utilizzo di schemi terapeutici standardizzati di breve durata (6 – 8 mesi) con trattamento effettuato con la supervisione di un sanitario o di un soggetto designato (Fig. 26);
Short-course chemotherapy – Utilizzo di schemi terapeutici standardizzati di breve durata (6 – 8 mesi) con trattamento effettuato con la supervisione di un sanitario o di un soggetto designato (Fig. 26); 